疫苗被认为是过去几个世纪以来最成功的医学疗法之一,它们旨在利用人体免疫系统并产生针对特定疾病的持久保护。
传统疫苗依赖于使用非活性病原体来引发免疫反应。然而,许多这些制剂具有引起过敏或自身免疫反应的高风险。多肽疫苗越来越被认为是规避这一问题的一种经济有效且安全的方法。
一、多肽疫苗设计
疫苗开发过程是一个具有挑战性的多步骤过程,涉及多个关键阶段(图1)。多肽疫苗的开发涉及三个主要步骤:(1)识别免疫原性肽表位;(2)优化肽表位,以提高有效性和长期免疫力;(3)使用佐剂或某些递送系统进一步提高肽表位的免疫原性(图2)。
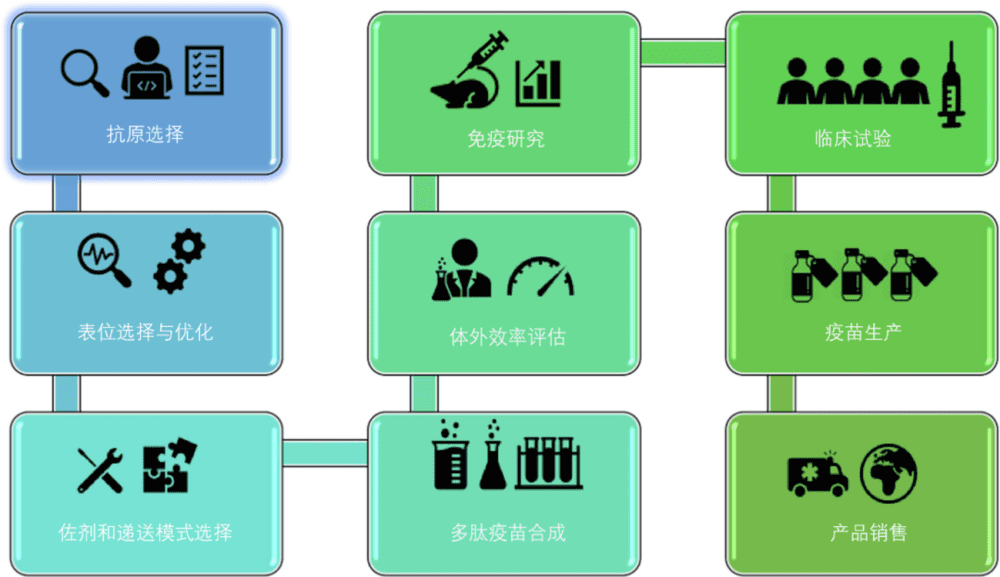
图1. 疫苗开发过程的示意图。(图片来源:Drug Discovery Today)

图2. 多肽疫苗设计步骤。(图片来源:Drug Discovery Today)
1. 表位预测
表位(或抗原决定簇)是免疫细胞识别的抗原的一部分。它们通常有 5-15 个氨基酸残基或1-6个糖残基。它们可以是线性的(连续的)或构象的,这取决于它们的结构以及与其抗体表面上存在的互补位的相互作用。在线性表位中,残基连续存在;而在构象表位中,构成表位的残基通过抗原的结构折叠在空间上凑在一起。表位预测是多肽疫苗设计流程中最初和最关键的步骤之一。各种方法,包括计算和免疫信息学方法、组合技术、诱变、生物物理学方法和结合分析,被用于鉴定表位。
各种数据库、网络服务器和算法可用于选择和识别候选表位,从而大大减少了实验性表位预测过程所花费的时间。在这种计算机方法中,来自目标病原体的抗原蛋白的一级氨基酸序列或3D结构被用作输入,然后分析是否存在能够与MHC(major histocompatibility complex,主要组织相容性复合体)分子结合的序列(称为表位),MHC在人类中被称为人类白细胞抗原(HLA, 又称移植抗原)。免疫表位数据库(IEDB,Immune Epitope Database)是最常见的表位预测数据库,可免费访问并包含用于表位预测和分析的工具集合。
2. 评估表位抗原性和免疫原性
预测的多肽表位的免疫原性可以通过两种体内方法进行分析:1)使用 HLA 转基因小鼠的体内免疫原性分析;2)使用人 APC(Antigen-presenting cells, 抗原呈递细胞)的抗原性测试。[1]
3. 表位优化
CTL(细胞毒性T淋巴细胞)免疫反应的激活不需要表位的特定构象(它们是线性的)。相比之下,B细胞激活需要表位的构象与其天然抗原相似。超过90%的B细胞表位是不连续的,它们需要维持天然结构才能结合B细胞活化产生的抗体。
为了保持这种构象,有时会对表位进行化学修饰或延长长度。例如,通过在相距较远的两个氨基酸的侧链之间引入接头的装订技术将肽锁定为α螺旋构象。[2] 在肽的不同氨基酸侧链之间引入人工化学键,可以使肽折叠成所需的构象。[3] 另一种有助于促进天然构象的方法,是在表位的侧翼添加额外的辅助序列,例如将GCN4酵母蛋白链接到短肽的C和N末端时,可以促成表位的α-螺旋结构的形成。[4]
Pan HLA-DR-binding epitope(PADRE)是一种用于刺激抗体介导的B细胞反应的辅助肽,在多项临床试验表现出了安全性和高效性。[5] PADRE由D-丙氨酸、L-环己基丙氨酸和氨基己酸组成。将β-氨基酸添加到表位是另一种增强“多肽-MHC 结合”亲和力的策略,可稳定多肽。[6]
二、增强多肽免疫效力
通过改进多肽大小或结合特性、直接激活APC或与佐剂一起激活,或使用有效的肽递送系统,通过促进内吞和吞噬作用来提高多肽疫苗的免疫效力。在肽疫苗中引入翻译后修饰也有可能进一步增强其功效。
1. 佐剂的使用
佐剂是与疫苗共同给药以刺激抗原提高免疫效力的物质。它们减少抗原剂量,引起快速诱导并增强 B 和 T 细胞的持久性。[7] 大多数佐剂在给药部位诱导局部炎症,从而募集各种细胞因子和趋化因子[8] 并刺激APC上的CCR7表达,以促进抗原迁移至淋巴结。最常见的佐剂通常是Toll样受体(TLR)激动剂 、C型凝集素受体 (CLR)激动剂,以及核苷酸结合寡聚化结构域(NOD)样受体(NLR)激动剂。
植物来源的低聚糖、菊糖的佐剂可以在人类中诱导两种免疫反应。[9] 多聚肌动蛋白A(PAA)已被用作多肽癌疫苗的有效佐剂。[10] 最常见的用作佐剂的碳水化合物及其衍生物包括甘露糖、葡聚糖、壳聚糖、透明质酸、皂苷、α-半乳糖苷神经酰胺和胞壁酰二肽(MDP, Muramyl Dipeptide)的聚合形式。
三、多肽疫苗针对的适应症
1. 流感
上个世纪,人类流感大流行导致5000万至1亿人死亡。由于流感病毒的巨大序列多样性和高突变率,开发有效的流感疫苗具有挑战性。一个靶点是流感血凝素(HA),这是一个糖蛋白家族,可使病毒进入宿主细胞。为了试图规避序列多样性,疫苗设计侧重于高度保守的结构域,尤其是那些被广泛中和抗体靶向的病毒包膜糖蛋白。由于血凝素HA2的“主干”区域高度保守,因此它代表了一个极好的目标。[11]
2. 肝炎病毒
丙型肝炎病毒(HCV)感染可导致肝病,例如肝硬化或肝细胞癌。有效的HCV疫苗的开发一直受到病毒变异性的阻碍,特别是T细胞靶向的表位内的序列变异。大多数针对HCV的抗体与E2糖蛋白表位发生反应。已经开发出一种新型肽疫苗 IC41,它包含五种含有HCV T细胞表位和佐剂聚(l-精氨酸)的合成肽,但T细胞反应太小,无法在大多数患者的HCV RNA中产生显著差异,因此需要进一步优化。[12]
3. 艾滋病
抗HIV病毒的疗法主要基于小分子抗逆转录病毒药物,可以显著改善病情的影响。例如36元多肽enfuvirtide(商品名Fuzeon®),可抑制gp41 HIV病毒外壳蛋白与细胞膜的融合,从而阻止病毒进入细胞。[13] 从疫苗角度来看,HIV-1病毒刺突膜糖蛋白gp120(188)的V3(HIV 包膜可变区3)环成为中和抗体的目标,因此已被确定为基于多肽的疫苗设计的候选者。[14]
4. SARS-CoV-2 和相关冠状病毒
由 SARS-CoV-2病毒引起的全球COVID-19大流行刺激了基于mRNA和腺病毒载体等疫苗的快速开发。但基于多肽的SARS-CoV-2疫苗尚未投入使用。现在已经对 SARS-CoV-2蛋白进行了测序,并且有可能确定它的刺突蛋白与靶细胞结合所涉及的关键区域,这些区域代表了治疗干预的潜在目标。
5. 癌症免疫治疗多肽
免疫肿瘤学中治疗癌症的免疫反应是研发热点,目的是激活癌细胞所利用的免疫抑制逃避机制。主要焦点是调整 T 细胞的反应,因为这些细胞能够清除肿瘤。与正常健康细胞相比,癌细胞的特征在于某些蛋白质的过度表达或突变,它们因此成为免疫疗法的目标。比较突出的肿瘤相关抗原包括:粘蛋白1(MUC1)、人表皮生长因子受体2(HER-2)、癌睾丸抗原1(NY-ESO-1)、T细胞识别的黑色素瘤抗原1(Melan-A或MART-1)、前列腺特异性抗原(PSA)等。
6. 抗真菌多肽疫苗
传统疫苗已被用于预防病毒和细菌感染。有趣的是,在抗真菌疗法的开发中发现了更大的挑战。真菌仍然被认为是全世界死亡的主要原因。根除侵袭性真菌感染通常需要数月至数年的连续给药,这通常会导致耐药变体的风险加剧。此外,许多新出现的真菌疾病是由多重耐药真菌菌株引起的,例如 2009 年首次报道的耳念珠菌。除了这些障碍之外,批准用于治疗的抗真菌药物数量有限,并且已知其中许多会引起严重的副作用。
耐药性的高发生率和抗真菌药物的固有毒性,激发了人们对开发抗真菌疫苗的兴趣。然而,真菌细胞的遗传复杂性继续带来多重挑战。科学家们仍然不完全了解抗真菌体液免疫反应,因此很难识别和选择合适的表位甚至抗原来进行适当的疫苗接种策略。
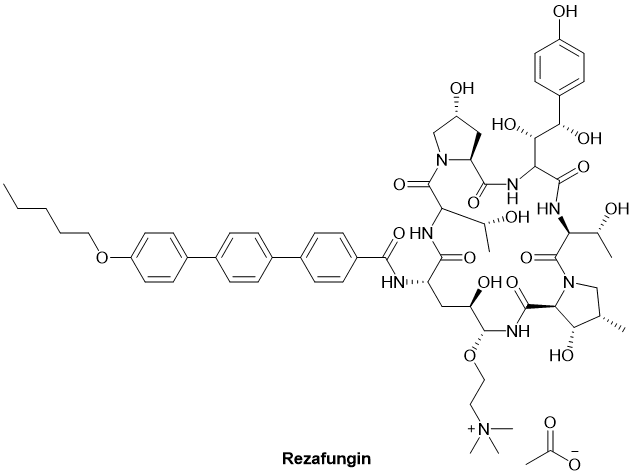
图3. Rezufugin化学结构
尽管如此,多肽抗真菌药物却在2023年第一季度实现了突破。2023年3月22日, FDA批准了Cidara和Melinta的Rezzayo™(注射用rezafungin)用于治疗18岁或以上患者的念珠菌血症和侵袭性念珠菌病。Rezafungin也成为十多年来首个获得FDA批准的新棘白菌素(echinocandin)。Rezafungin是一个六元多肽,抑制真菌细胞壁中的1,3-β-D-葡聚糖合酶复合物,可破坏包括念珠菌属在内的真菌物种的细胞壁。尽管不属于多肽疫苗,但多肽在抗真菌过程中起到的作用受到了业内人士的高度重视。
四、肽疫苗的优势和局限性
肽疫苗被认作疫苗开发中最有前途的趋势,但是使用肽进行免疫并不是一个新概念。肽的使用使疫苗能够针对非常特定的表位,同时最大限度地降低过敏或自身免疫反应的风险。但除了特异性和安全性方面的优势外,多肽疫苗还通过降低疫苗的生产成本和交货时间提供了明显的成本和供应优势。
然而,基于这些最小序列开发疫苗并非没有挑战。多肽通常缺乏免疫原性,因此,它们经常不能诱导有效的免疫反应。此外,这些分子的药代动力学决定了它们的不稳定性和较差的类药性,因为它们很容易在成功引发免疫反应之前就被广泛存在的蛋白酶降解。
在过去的几十年里,科学家们设计了很多策略来克服这些限制。多肽的偶联是迄今为止开发的最成功的策略之一。例如,多肽可以与蛋白质(例如KLH或BSA)结合,这种结合有助于提高它们的稳定性和免疫原性。另一种增加肽稳定性和免疫原性的策略在于多聚体肽疫苗的开发。使用针对同一表位的多肽的多个拷贝,或针对同一抗原的不同表位的组合,比使用未偶联的多肽本身更有效。
总结来说,多肽疫苗的优势可以体现在以下方面:
安全性:多肽疫苗通常被认为是安全的,因为它们由短链氨基酸组成,不含活的或减毒的病原体。即使是免疫系统较弱的个体,也不存在引发所针对疾病的风险,而这正是病毒基质疫苗的潜在安全性问题所在。
特异性:肽疫苗具有高度特异性。它们可以经过精确设计,针对特定的病原体、菌株或变种。这种特异性对于快速进化的病原体引起的疾病尤其重要,例如流感和艾滋病毒。
降低副作用风险:由于肽疫苗不含某些疫苗中包含的潜在反应原成分,因此它们不太可能引起不良反应或副作用。
易于生产:与传统疫苗相比,肽疫苗的生产相对容易且具有成本效益,特别是在应对快速变化的病原体时。生产过程可以标准化,不需要复杂的活体培养。
无逆转风险:减毒活疫苗有逆转为毒力形式的风险。肽疫苗不会造成这种风险,因为它们不含活病原体。
定制:研究人员可以为特定人群甚至个人定制肽疫苗。在个性化医疗中,可以识别肿瘤特异性肽,并创建针对患者独特癌症的个性化癌症疫苗。
稳定性:与其他一些疫苗类型(例如需要严格冷链储存的活疫苗)相比,肽疫苗通常很稳定,并且保质期更长。
减少交叉反应:多肽疫苗可以最大限度地减少与宿主组织的交叉反应,从而降低自身免疫反应的风险。
重新接种:由于多肽疫苗不含活病原体,因此可以进行重新接种,而无需担心接受者的免疫状态。
免疫监测:由于特定表位已知,多肽疫苗通常提供更直接的方法来监测和测量免疫反应。这可以帮助评估疫苗功效。
特殊人群的安全性:多肽疫苗可以更安全地用于较高风险的人群,例如孕妇和免疫功能低下的个体。
无病原体逃逸的风险:与活疫苗不同,多肽疫苗不存在病原体突变或进化以逃避疫苗诱导的免疫力的风险。
多肽疫苗的局限性主要表现在以下方面:
有限的免疫原性:与全蛋白或减毒活疫苗相比,肽本身的免疫原性可能有限。它们可能不会引起强烈或持久的免疫反应,这可能导致需要加强剂量。
HLA限制:肽疫苗通常通过人类白细胞抗原(HLA,human leukocyte antigen)分子呈递给免疫系统。不同的个体有不同的HLA类型,并非所有肽都能有效结合所有HLA类型。这可能会限制多肽疫苗的普遍适用性,并且在某些情况下需要个性化的方法。
表位的鉴定:鉴定给定病原体的最具免疫原性和保守的表位可能是一个复杂且耗时的过程。它可能需要广泛的研究和测序。
MHC超型覆盖:实现广泛的人群覆盖可能需要设计涵盖多种MHC(主要组织相容性复合体)超型的疫苗,这会增加疫苗开发的复杂性。
不完整的保护:多肽疫苗可能无法提供与全病原体疫苗一样全面的保护。例如它们在预防粘膜表面感染方面可能效果较差。这一点和上述的有限的免疫原性相关联。
佐剂要求:在某些情况下,肽疫苗可能需要佐剂或递送系统来增强其免疫原性,这会增加疫苗配方的复杂性。
表位的多样性:一些病原体具有多种表位,因此为多肽疫苗选择最有效的表位具有挑战性。
高剂量:多肽疫苗可能需要加强剂量才能随着时间的推移维持免疫力,这可能会导致更高的成本和供应量挑战。
治疗时机:在某些情况下,多肽疫苗可能需要在疾病进展的特定阶段施用才能发挥最大功效,从而限制了它们作为预防性疫苗的用途。
尽管存在上述限制,研究人员仍在积极研究,试图攻克这些挑战,提高肽疫苗功效。这些努力包括佐剂的开发、多肽设计的优化,以及癌症疫苗的个性化方法。多肽疫苗应该为预防和治疗传染病和癌症提供宝贵工具。
五、总结
寻找最小免疫原性序列的努力创造出了新一代疫苗,称为多肽疫苗。许多研究人员认为这些疫苗是人类和动物免疫的未来。多肽疫苗的优势在于显著降低生产成本、过敏和自身免疫反应的风险,同时保护人类免受严重疾病的威胁。
然而,开发合适的肽疫苗仍然特别具有挑战性。发生这种情况是因为许多这些最小的肽序列本身不能诱导有效的免疫反应。许多研究人员提出利用其他分子和其他表位结合作为规避此问题的方法。这一基本原理继续推动许多此类疫苗的开发,或许新一代的拟肽类物质将成功撞线,成为多肽疫苗的未来主力军。
参考文献:
[1] Livingston, B. et al. A rational strategy to design multiepitope immunogens based on multiple Th lymphocyte epitopes. J Immunol, 168 (2002), pp. 5499-5506
[2] Lau, Y. H. et al. Peptide stapling techniques based on different macrocyclisation chemistries
Chem Soc Rev. 2015, 44, 91-102.
[3] Bird, G. H. et al. Stapled HIV-1 peptides recapitulate antigenic structures and engage broadly neutralizing antibodies. Nat Struct Mol Biol. 2014, 21, 1058-1067.
[4] Cooper, J. A. et al. Mapping of conformational B cell epitopes within alpha-helical coiled coil proteins. Mol Immunol. 1997, 34, 433-440.
[5] Overholser, J. et al. Anti-Tumor Effects of Peptide Therapeutic and Peptide Vaccine Antibody Co-targeting HER-1 and HER-2 in Esophageal Cancer (EC) and HER-1 and IGF-1R in Triple-Negative Breast Cancer (TNBC). Vaccines. 2015, 3, 519-534.
[6] Webb, A. I. et al. T cell determinants incorporating beta-amino acid residues are protease resistant and remain immunogenic in vivo. Curr Med Chem. 2002, 9, 811-822.
[7] Maisonneuve, C. et al. Unleashing the potential of NOD- and Toll-like agonists as vaccine adjuvants. Proc Natl Acad Sci USA. 2014, 111, 12294-12299.
[8] Mosca, F. et al. E. Molecular and cellular signatures of human vaccine adjuvants.
Proc Natl Acad Sci USA. 2008, 105, 10501-10506.
[9] Silva, D. G. et al. Inulin-derived adjuvants efficiently promote both Th1 and Th2 immune responses. Immunol Cell Biol. 2004, 82, 611-616.
[10] Wang, W. et al. Polyactin A is a novel and potent immunological adjuvant for peptide-based cancer vaccine. Int Immunopharmacol. 2018, 54, 95-102.
[11] Impagliazzo, A. et al. A stable trimeric influenza hemagglutinin stem as a broadly protective immunogen. Science. 2015, 349, 1301– 1306.
[12] Klade, C. S. et al. Therapeutic vaccination of chronic hepatitis C nonresponder patients with the peptide vaccine IC41. Gastroenterol. 2008, 134, 1385–1395.
[13] Lalezari, J. P. et al. TORO 1 Study Group Enfuvirtide, an HIV-1 fusion inhibitor, for drug-resistant HIV infection in North and South America. N. Engl. J. Med. 2003, 348, 2175– 2185.
[14] Malonis, R. J. et al. Peptide-Based Vaccines: Current Progress and Future Challenges. Chem. Rev. 2020, 120, 3210–3229.
[General] Hamley, I. W. Peptides for Vaccine Development. ACS Appl. Bio Mater. 2022, 5, 3, 905–944.
[General] Kalita, P. et al. Methodological advances in the design of peptide-based vaccines. Drug Discovery Today. 2022, 27, 1367-1380.
[General] Reis, A. Are peptide vaccines providing a safer and more cost-effective alternative to conventional vaccines in protecting against life-threatening and chronic diseases? Proteogenix. 31, 10, 2019.
本文来自微信公众号:同写意Biotech(ID:TXYBiotech),作者:杨翼

