本文来自微信公众号:同写意Biotech(ID:TXYBiotech),作者:杨翼,原文标题:《抗流感病毒药物与市场分析》,题图来自:视觉中国
面目可憎的SARS-CoV-19尚未被人类完全征服,阴魂不散的流感病毒又开始肆虐。人类与病毒的斗争,就这么在“科学的进步—病毒的变异与耐药性”这个循环中螺旋上升。季节性流感病毒的周期性传播,令抗流感病毒药物开发的重要性再次凸显出来。
24年前上市的奥司他韦仍然是抗流感病毒药物的中流砥柱,尽管首创新药巴洛沙韦充实了抗流感药物的队伍,但它的上市也是5年之前的事情了。在领教了SARS-CoV-19病毒的残暴之后,人们需要在流感药物的开发上取得突破。
一、季节性流感分类
季节性流感(Seasonal influenza)是由流行于世界各地的流感病毒引起的急性呼吸道传染病。季节性流感病毒有4种类型,A、B、C和D型(中文对应甲、乙、丙、丁型流感)。A型和B型流感病毒传播并引起季节性流行病(seasonal epidemics)。
根据病毒表面的血凝素(HA, hemagglutinin)和神经氨酸酶(NA, neuraminidase)的组合,甲型流感病毒进一步分为不同的亚型。目前在人类中传播的是亚型A(H1N1)和A(H3N2)流感病毒。A(H1N1)流感病毒也被写为A(H1N1)pdm09,因为它在2009年引起了大流行,取代了2009年之前传播的季节性甲型流感(H1N1)病毒。
已知目前只有A型流感病毒引起大流行。B型流感病毒不分为亚型,但可以分为谱系。当前流行的B型流感病毒属于B/Yamagata或B/Victoria谱系。C型流感病毒检测频率较低,通常引起轻度感染,因此不具有公共卫生重要性。D型流感病毒主要影响牛,并不会感染或导致人类患病。[1]
二、流感治疗
无并发症的季节性流感患者,如果出现症状,就待在家中,为降低病毒的传播尽一份绵薄之力。凭借自我监测的方法决定是否需要就医。
患有与流感相关的严重或进展性临床疾病,即肺炎、败血症或慢性基础疾病恶化的临床综合征的患者,应尽快接受抗病毒药物治疗。最常见的抗流感病毒药物是神经氨酸酶抑制剂(Neuraminidase inhibitors)奥司他韦(oseltamivir)。理想情况下,应在出现症状48小时之内服用,以最大化疗效。建议治疗至少5天,但可以延长至临床改善令人满意为止。
需要注意的是,针对流感,不应该使用皮质类固醇(corticosteroid,例如泼尼松、可的松、和氢化可的松等),除非有其他原因(例如哮喘和其他特定情况),因为皮质类固醇药物可能导致病毒清除时间延长、免疫抑制导致的细菌或真菌二重感染。
目前流行的所有流感病毒都对金刚烷类抗病毒药物(Adamantane antivirals,如金刚烷胺amantadine和金刚乙胺rimantadine)具有耐药性,因此不推荐将这些药物用于单药治疗。[1]
三、抗流感病毒药物
抗流感病毒药物中的主力军分为金刚烷类、神经氨酸酶抑制剂类,以及聚合酶抑制剂类等几大板块(表1)。[2] 美国疾病控制与预防中心推荐的获FDA批准的抗流感药物有四种:Rapivab (peramivir),Relenza(zanamivir),Tamiflu (oseltamivir phosphate)和Xofluza(baloxavir marboxil)。[3]
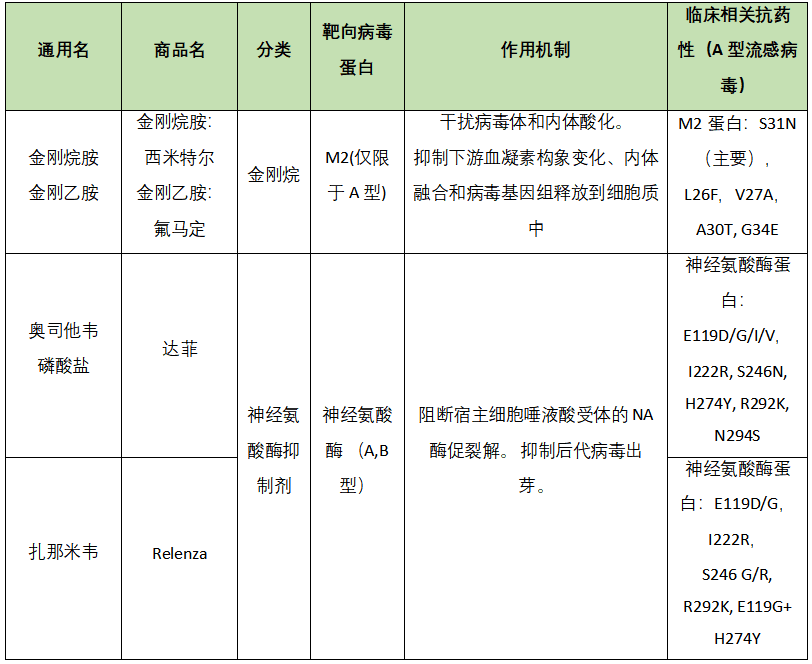
1. 神经氨酸酶抑制剂(Neuraminidase inhibitors)
神经氨酸酶抑制剂(NAI)靶向神经氨酸酶(NA)糖蛋白,这是人体内仅次于血凝素(HA)的最丰富的表面糖蛋白。神经氨酸酶抑制剂通过抑制宿主细胞中新出现的病毒粒子出芽,以及防止病毒传播所必需的酶活性来实现抗病毒疗效。[4]
最常见的四种神经氨酸酶抑制剂药物是奥司他韦oseltamivir、扎那米韦zanamivir、帕拉米韦peramivir和拉尼米韦laninamivir(图1)。
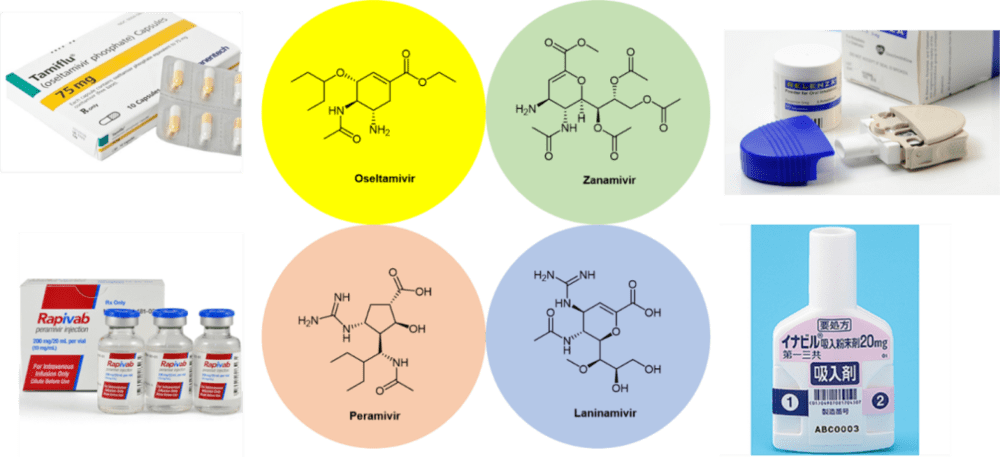
尽管结构相似,但它们在治疗方案、给药途径和耐药性方面存在明显差异。最广泛使用的神经氨酸酶抑制剂药物是奥司他韦(商品名:达菲Tamiflu),成人的治疗方案是75mg剂量,每天两次,持续5天。由于扎那米韦(商品名Relenza)的口服生物利用度较低(<5%),因此它被批准作为一种吸入药物,每次5mg,每天两次,持续5天。
2019年,静脉注射的扎那米韦(商品名Dectova)获得欧盟授权,在特殊情况下使用(例如在对其他抗流感药物产生耐药的情况下)。增加生物利用度和半衰期的努力促成了帕拉米韦(商品名:Rapivab/Rapiacta/PeramiFlu)的开发,通过静脉输注以单次600mg剂量给药;以及拉尼米韦(商品名Inavir),一种更持久的神经氨酸酶抑制剂,在单次鼻腔吸入剂量后显示出治疗效果。[5] 帕拉米韦和拉尼米韦获准在全球少数国家使用,而奥司他韦和扎那米韦在地域上获得更广泛的批准。
不同的神经氨酸酶抑制剂显示出不同的功效,这主要取决于感染患者的流感病毒的亚型/谱系。例如奥司他韦对甲型(H1N1)、甲型(H3N2)和乙型病毒引起的季节性无并发症流感效果较为明显。但抗病毒治疗的效果,可能会掣肘于流感病毒对神经氨酸酶抑制剂产生的耐药性。不同神经氨酸酶抑制剂的耐药情况不同。
针对常见神经氨酸酶抑制剂的耐药性问题,人们现在将目光对准了新兴的在研药物。前有至少有两种新型神经氨酸酶抑制剂和一种神经氨酸酶阻滞剂正处于1期和2期开发阶段。
HNC042(广州市恒诺康医药科技有限公司及黑龙江珍宝岛药业股份有限公司)在临床前研究中显示出对野生型和耐奥司他韦NA-H274Y病毒的有效抑制活性。在美国的 1 期试验中,HNC042显示出良好的安全性和耐受性,以及线性药代动力学(NCT04603989)。HNC042用于预防和治疗流感,尤其是需要住院治疗的重症患者。
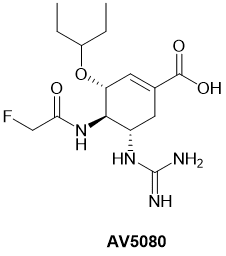
AV5080(ChemRar,俄罗斯,Viriom,美国,图2)的临床前评估揭示了对多种流感病毒的活性,包括奥司他韦耐药株。口服AV5080在动物中表现出良好的物理化学和代谢特性以及良好的药代动力学特征。[6]
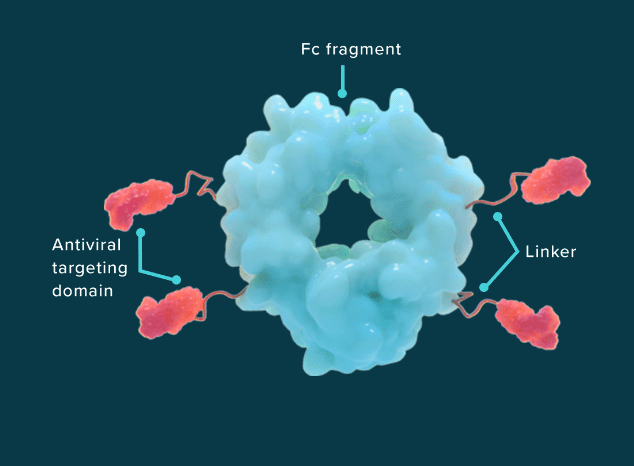
CD388(Cidara Therapeutics Inc.,美国)是一种长效神经氨酸酶阻滞剂,其结构通过将流感病毒的神经氨酸酶偶联到由人类抗体片段(Fc)的专有变体组成的效应域,从而实现两种截然不同且互补的机制(图3)。这种预防和治疗病毒感染的全新方法有望在整个流感季节提供普遍保护。通过针对病毒高度保守的区域,CD388可以潜在地保护个体免受所有流感毒株的侵害,包括季节性和大流行性甲型流感、乙型流感和具有临床特征的主要耐药病毒(NCT05523089)。
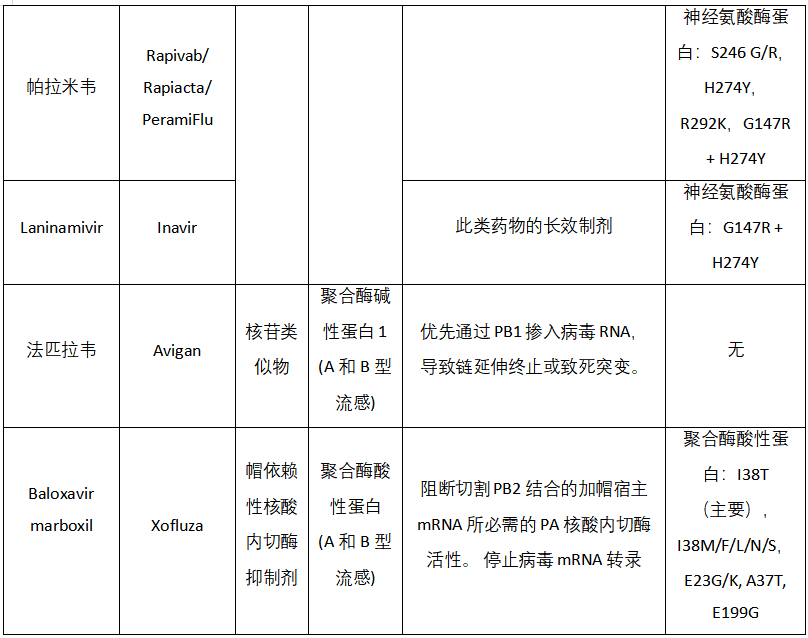
2. 聚合酶抑制剂(Polymerase Inhibitors)
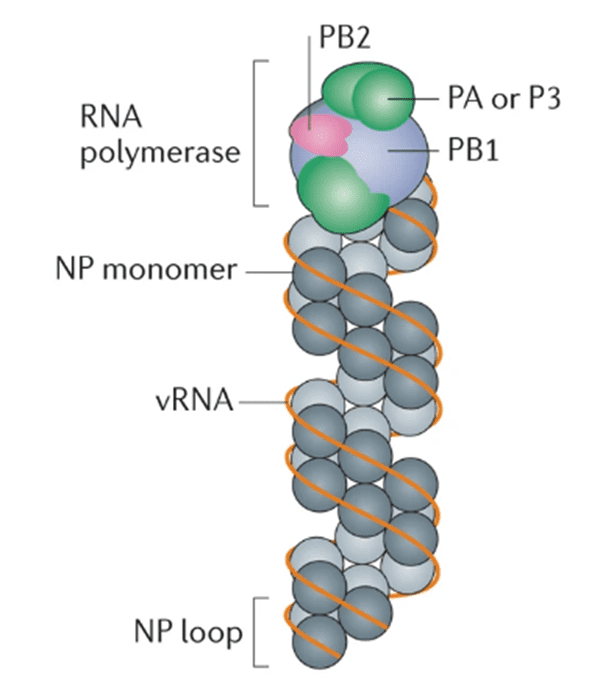
流感病毒RNA聚合酶对病毒基因转录和基因组复制至关重要,使其成为定向药物设计的主要目标。他们在甲型、乙型、丙型和丁型流感病毒中高度保守。[7] 流感病毒 RNA 聚合酶由三个亚基组成:甲型和乙型流感病毒中的聚合酶碱性蛋白1 (PB1)、聚合酶碱性蛋白2(PB2)和聚合酶酸性蛋白(PA),或丙型和D型流感病毒中的聚合酶3蛋白(P3)(图4)。
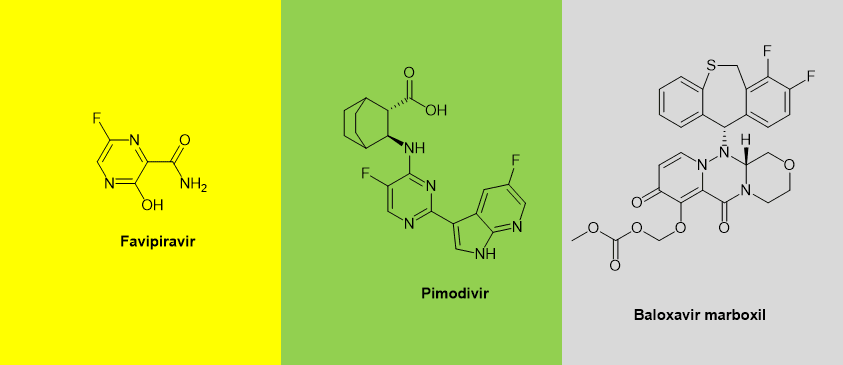
与RNA结合、切割和延伸的聚合酶活性位点在各种类型的流感病毒中是保守的,这就是为什RNA依赖型的RNA聚合酶被认为是抗病毒剂的靶标。最近开发了几种针对每个亚基的聚合酶抑制剂,包括PB1抑制剂法匹拉韦favipiravir、PB2 抑制剂匹莫地韦pimodivir和PA抑制剂巴洛沙韦马波西尔 baloxavir marboxil(图5)。
其中baloxavir marboxil是一种相对较新的药物,属于帽依赖性核酸内切酶抑制剂(cap-dependent endonuclease inhibitor, CENI),是近20年来首创的新作用机制的抗流感病毒新药,由日本盐野义(Shionogi)制药株式会社首先研制,没有等效的仿制药,已证明对于健康成人与奥司他韦具有相似的症状缓解时间和更大的病毒载量降低。[8] 一项回顾性研究表明,与神经氨酸酶抑制剂相比,baloxavir marboxil可能减少住院治疗率。[9]
Baloxavir marboxil、Favipiravir和Pimodivir的耐药性问题以及其它缺陷,突出表明了人们需要开发其他广泛抑制A型和B型流感病毒的聚合酶靶向分子。
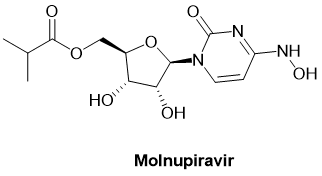
各种PB2靶向小分子的临床前研究正在进行中,[10] 其中至少一个(CC-42344) 处于第 1 阶段(NCT05202379),另一个(ZSP1273)处于第3阶段研究(NCT04024137)(图7)。Favipiravir的核苷抑制剂替代品,如 molnupiravir(图6),由于对各种RNA病毒有效,可能对治疗流感有一定好处,但它们也可能具有与Favipiravir相似的致畸副作用,因此其开发商默克最终放弃了针对流感病毒的开发,转而瞄准了Covid-19的治疗。基于核苷和非核苷的PB1抑制剂的开发正在进行临床前阶段,[11] 但目前尚无临床试验。
Baloxavir marboxil显然为开发聚合酶抑制剂型抗流感病毒药物提供了广阔思路,多项专利和体外研究都集中在Baloxavir marboxil骨架的化合物或变体。[12] 尽管有些在小鼠身上显示出有前途的体外疗效和药效学,[13] 但AL-749等候选药物并没有通过1期测试。
帽依赖性核酸内切酶抑制剂TG-1000 (东阳光药业)和 GP681(江西青峰和银杏树药业合作开发)最近完成了2期试验(NCT04706468、NCT04736758),并且正在进行ZX-7101A 1期研究的招募(NCT05217732)。破坏聚合酶复合物组分之间重要蛋白质-蛋白质相互作用的各种小分子和多肽,包括PA和PB1之间或PB1和PB2之间的关键接触,正处于临床前开发阶段。[14]
四、抗流感病毒药物全球市场
根据Growth Plus Reports发布的最新报告,到2030年,全球流感药物市场预计将达到15.1亿美元,并在预测期内以4.8%的复合年增长率增长。流感病例每年都会激增,预计将推动流感药物市场的持续增长。[15]
北美占据全球流感药物市场的大部分份额。流感的高诊断率、更广泛的药物发现和开发基础、治疗方法的广泛可用性,以及更显著的医疗支出,有助于北美市场对于流感药物的主导地位。亚太地区拥有全球第二大流感药物市场份额。高患病率、政府控制疾病的举措,以及医疗保健支出的增加影响了这一增长。
由于疾病发病率增加,以及普通人群中存在相当大的流感相关风险因素,预计欧洲市场也将出现显著增长。NCBI(美国国家生物技术信息中心)的一项研究表明,每年冬天在28个欧盟国家中,有 27600 例呼吸道死亡与季节性流感有关,其中88%是65岁以上的人群。这个年龄组的死亡率大约是65岁及以下人群的35倍。
在流感药物开发和销售中的主要参与者包括:Sanofi, Lupin, Teva, Shionogi, Macleods, Alvogen, AstraZaneca, BioCryst, La Roche, Novartis, Vitaris等。
五、总结
虽然没有SARS-CoV-2病毒那么面目狰狞,但流感病毒同样夺去很多人的生命,治疗流感仍然是人类面临的一个艰巨挑战。同其它抗病毒药物一样,流感药物的开发面临着病毒耐药性的困难。Baloxavir marboxil是一种首创新药,它对某些奥司他韦耐药菌株表现出活性,并且在安全性和有效性方面与最近用于治疗流感的已知药物没有显著差异。Baloxavir marboxil的上市也为使用两种不同作用机制的药物进行联合治疗带来了新的机会。虽然尚未进行此类研究进行系统展开,但这为流感治疗提供了一个宝贵的新方向。
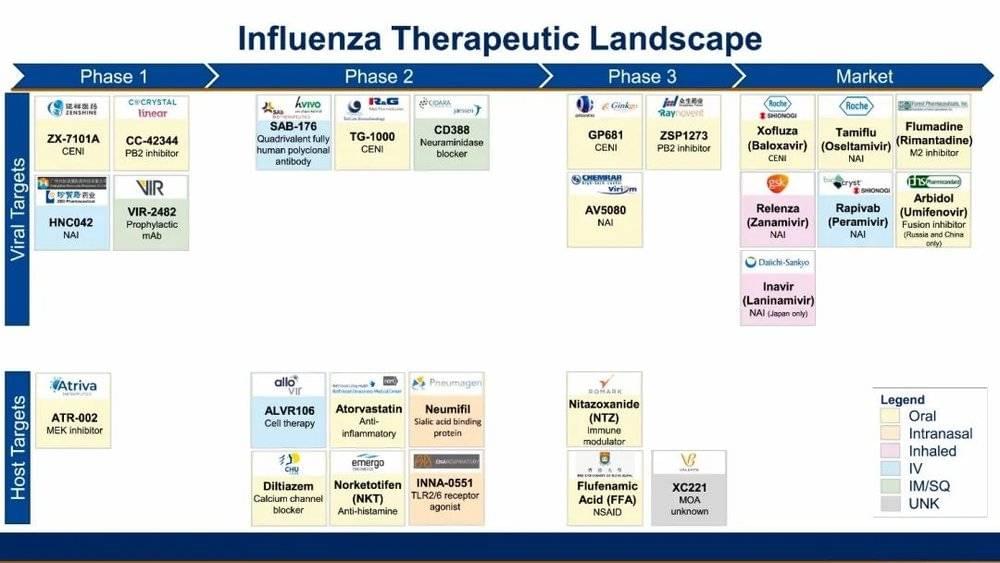
除了Baloxavir marboxil之外,还有很多在研药处于不同的临床阶段(图7),它们将在药理学、抗药性、药代动力学等方面进行优化,站在目前为数不多的流感药物的肩膀上,展开对流感病毒不懈的斗争。
参考文献:
[1] WHO. Influenza (Seasonal). 12, 01, 2023. ↑[] Jones, J. C. et al. Influenza antivirals and their role in pandemic preparedness. Antiviral Research. 2023, 210, 105499.
[2] Influenza (Flu) Antiviral Drugs and Related Information. FDA. 08, 12, 2022.
[3] Monto, A. S. et al. Influenza pandemics: history and lessons learned. Webster, R. G. et al (Eds.), Textbook of Influenza (2 ed.), Wiley Blackwell, West Sussex, United Kingdom (2013), pp. 20-36
[4] Sugaya, N. et al. Long-acting neuraminidase inhibitor laninamivir octanoate (CS-8958) versus oseltamivir as treatment for children with influenza virus infection. Antimicrob. Agents Chemother. 2010, 54, 2575-2582
[5] Ivachtchenko, A. V. et al. Novel oral anti-influenza drug candidate AV5080. J. Antimicrob. Chemother. 2014, 69, 1892-1902.
[6] Peng, Q. et al. Structural insight into RNA synthesis by influenza D polymerase. Nat Microbiol. 2019, 4, 1750–1759.
[7] Hayden, F. G. et al. Baloxavir marboxil for uncomplicated influenza in adults and adolescentsN. Engl. J. Med. 2018, 379, 913-923.
[8] Komeda, T. et al. Comparison of hospitalization incidence in influenza outpatients treated with baloxavir marboxil or neuraminidase inhibitors: a health insurance claims database studyClin. Infect. Dis., 2021, 73, e1181-e1190.
[9] Chen, W. et al. Approaches for discovery of small-molecular antivirals targeting to influenza A virus PB2 subunit. Drug Discov. Today. 2022, 27, 1545-1553.
[10] Hou, L. et al. Contemporary medicinal chemistry strategies for the discovery and optimization of influenza inhibitors targeting vRNP constituent proteins. Acta Pharm. Sin. B. 2022, 12, 1805-1824.
[11] Stevaert, A. et al. The influenza virus polymerase complex: an update on its structure, functions, and significance for antiviral drug design. Med. Res. Rev. 2016, 36, 1127-1173.
[12] Ivashchenko, A. A. et al. Synthesis, inhibitory activity and oral dosing formulation of AV5124, the structural analogue of influenza virus endonuclease inhibitor baloxavir. J. Antimicrob. Chemother. 2021, 76, 1010-1018.
[13] Massari, S. et al. Inhibition of influenza virus polymerase by interfering with its protein-protein interactions. ACS Infect. Dis. 2021, 7, 1332-1350.
[14] Influenza Medication Market – Global Outlook & Forecast 2022-2030. Growth Plus. 11, 10, 2022.
本文来自微信公众号:同写意Biotech(ID:TXYBiotech),作者:杨翼

