本文来自微信公众号:深蓝观 (ID:mic-sh366),作者:吴妮,编辑:王晨、高翼,原文标题:《当Biotech开始被退货》,题图来自:视觉中国
最近半年,尤其是最近半个月,医药圈的好消息大多是国内药企将自己的在研药物“license out”给国外药企。不仅包括康方等biotech,还包括恒瑞、石药等老牌传统药企。
License out的增多,不管对方是国际巨头,还是国外中小型Biotech,不管卖的价格如何,在业内人士来看:“是好事,意味着中国Biotech的进步。”
与此同时,这类好消息不一定都能走到最终,“逆向”的消息同时也传来。前不久,礼来在PD-1竞争格局激烈之下,退回了信达信迪利单抗的海外权益。而这一次,国内另一家明星公司诺诚健华的重磅药物和国际巨头渤健上演“分手事件”。
无论是信达,还是诺诚健华,两家都很“机智”地把这称之为“收回海外权益”。毕竟首付款一分不少,而海外市场才是星辰大海,如今又回到手里。这种资本主义巨头在创新药寒冬里免费送温暖的好事就这样发生在了中国的制药公司身上。
只是,当时轰轰烈烈标榜的“重磅国际化”的估值,如今是不是该计提一下减值呢?
不被看好的合作,意料之中的分手
2月15日(北京时间),渤健通知诺诚健华,为终止(to terminate for convenience)双方就诺诚健华的明星产品BTK抑制剂奥布替尼的全球开发和商业化达成的合作和许可。几个小时后,在美东时间的2月15日,渤健公布了2022年“销售额大跌9.7%”的业绩。
而一年半前,2021年的7月,渤健和诺诚健华的这一合作一度在圈内颇为震动。1.25亿美元首付款,最多8.125亿美元的潜在临床开发里程碑和商业里程碑付款,以及净销售额在百分之十几范围内从低至高的分层特许权使用费,而且合作方是神经系统疾病领域的一哥渤健——双方合作的纽带是奥布替尼潜在适应症多发性硬化。
这笔首付款造就了诺诚健华的业绩高光,2021年诺诚健华营业收入暴增至10.43亿元。
作为科学家施一公创办的明星公司——诺诚健华一诞生就在聚光灯下。有知名科学家光环的加持,融资极其顺利。但成也光环,败也光环。以至于当发现在研药物和创始人的专业领域不甚契合时,背后对高管团队的质疑声也不绝于耳。
即使在2020年12月25日,诺诚健华首个商业化产品(也是这次“退货”风波的主角奥布替尼),在国内上市,获批的适应症是两项血液肿瘤时,有不少观点谈到BTK是一个成熟的靶点,做肿瘤药物是“me- too” ,创新性不足。
但当诺诚健华将奥布替尼的管线布局拓展至自身免疫性疾病领域时,当适应症涉及多发性硬化、免疫性血小板减少症、系统性红斑狼疮、视神经脊髓炎、类风湿关节炎等自免性疾病,那么如果临床数据好最终成药,那么在适应症上算成为“First-in-class”,而且也有成熟且迫切的市场需求等在前面。当时,也有一些业内科学家提出质疑,虽然在机理上BTK抑制剂治疗自免疾病说的通,但“不够强,做不出来的可能性大。”
不过,很多人没有想到的是,自免领域巨头渤健,在刚换了CEO时,竟然和诺诚健华就这款药合作。“当时质疑这家公司(诺诚健华)的人,也闭嘴不说什么了。”很可能,这场合作,渤健钱紧一点,不那么急的话,也不会促成。
在渤健打完1.25亿美金首付款,临床试验进展到二期时,合作忽然终止。除了肝毒性损伤导致FDA终止临床试验外,一些业内人士猜测,临床数据很可能不够好。
对于渤健来说,当年这场有人评价为“病急乱投医”的合作,包含新任CEO上任赶紧引进项目的急躁,1.25亿美金收不回来的首付款是代价,将药物研发领域九死一生的“赌场”性质又演绎了一遍,但随着业绩的下跌,渤健还将在漫漫寻药路上试运气。
对于诺诚健华,找寻下一个合作者是当务之急。但这次合作的终止,除非“随后的临床试验有非常好的数据”才能找到合作者,但这种可能性极为微小。如果没有资金进来,很可能奥布替尼在自免领域的临床试验就此不再继续。
对一开始融资就异常顺利、且上市融资几十亿元的诺诚健华来说,这个消息不是好消息,但也不是毁灭性的坏消息。毕竟,奥布替尼在国内已有适应症上市。但如果换一家biotech,当唯一一款产品在需要大量烧钱的阶段时,合作的被终止就等于提前死亡。
“不是所有的赌局的主角是诺诚健华。”在无比考验长期主义的生物制药领域,比起license out刚开始,市场反应的急不可待的欣喜,随后的“被退货”反倒更值得警惕。
而随着中国创新药领域持续近两年的寒冬而言,以往,像诺诚健华那样有一个知名科学家发起就融资极其顺利的情况,现在已不多见。“现在,顶尖有名气的科学家只在自己专业领域再创业才有说服力,如果只是一个名人挂名的这种公司,现在肯定不会再融到钱了。”一位当初没有选择投资诺诚健华的投资人评论。
为什么合作终止?
合作终止消息一出,大家开始推测原因。官方公告中的“为便利而终止”,意味着被授权方无条件单方解除合同,好像什么都没说,又好像什么都说了,业内解读不一。
2022年底,由于观察到肝损伤病例,FDA叫停奥布替尼用于治疗多发性硬化症实施部份临床,在美国进行的II期研究将不会开展新的患者招募。肝损伤风险目前无解,在诺诚健华之前,赛诺菲和默克的BTK抑制剂都出现同样的情况。这或许是渤健”退货“的原因之一。
BTK抑制剂虽然在几大血液瘤里的治疗都已经很成熟了(奥布替尼2020年在中国也获批了慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、以及复发/难治性套细胞淋巴瘤两项适应症),但是渤健看上的是MS这个自生免疫症的领域,这是一个很新、很有挑战性的细分适应症。
因为它对于安全性的要求是变高的,肿瘤病人只要药物有效,对于安全性的容忍度是可以降低的,但是对于需要长期用药的自免病人,不可避免对安全性的要求就很高——所以不是说肿瘤上获批了,别的适应症就能获批,相反,如果在自免的适应症获批了,至少在安全性上对肿瘤来讲不会是个问题。
所以,多位投资人和业内人士推测,此次合作中止,最主要的原因多半是奥布替尼II期临床数据不太乐观。毕竟,此前渤健虽然在阿尔兹海默、核酸类药物以及ALS等领域的研发上接连受挫,昨天刚公布业绩(2022年营收-9.7%),成绩并不理想,但MS仍是渤健非常重视的领域,即便战略调整,也不会“放弃”或者“轻视”这一领域。不过,能不能拿出更多的资金来继续这个带着一定风险性的项目,也需要去抉择。
诺诚健华对肝损伤风险有自己的解释。
诺诚健华称,多发性硬化患者对肝脏的毒性非常敏感,目前已获批26个治疗MS的药物中有24款药物都有肝功能相关的问题。奥布替尼的不良反应表现为肝酶增加,发生肝酶增加的时间主要在前两个月,两个月之后出现肝酶增加的患者没有增加。诺诚健华认为,肝酶增加是reversible(可逆的),患者早期只要通过肝酶检测就能够prevent(预防),受影响的患者很少。
至于临床数据,按照GCP要求还不能分享。能够知道的是,在FDA叫停前,奥布替尼的II期实验已经完成80%,受此影响的患者很少。诺诚健华重新接手后,决定不再继续入组,计划在今年二季度完成24周的interim的数据分析,然后揭盲、公布数据。
数据情况决定了诺诚健华下一步的决定,如果数据比较好,诺诚健华会积极推进III期实验。
在临床进行的过程中,诺诚健华会继续在国际市场寻找商业化合作伙伴。
震动的后续
终止授权已经很常见,但此事一出还是让人颇为震动。因为奥布替尼之于诺诚健华的重要性,远超其他。
自2021年底被纳入国家医保目录,奥布替尼销售额持续快速增长,占据诺诚健华营收的90%以上。2022年第三季度,诺诚健华营收1.9亿元,其中奥布替尼销售额为 1.83亿元。2022年1~9月诺诚健华营收4.4亿元,奥布替尼销售额为4.00亿元。
奥布替尼的销售额虽然足够支撑诺诚健华的运营,但放在整个BTK抑制剂赛道微不足道。强生/艾伯维的一代BTK抑制剂伊布替尼已突破百亿美元销量,占据着全球大部分BTK抑制剂市场份额。
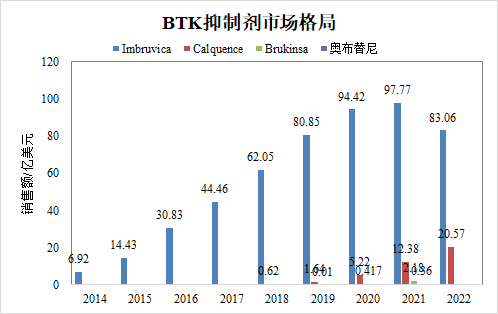
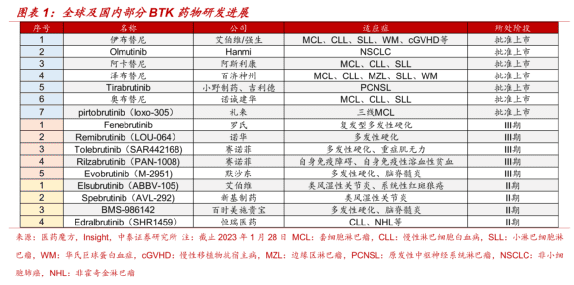
二代BTK抑制剂中,还有阿斯利康的阿卡替尼、百济神州的泽布替尼等强劲对手,都覆盖了MCL、CLL/SLL等大适应症。此外,罗氏、诺华、赛诺菲、默沙东等MNC的BTK分子已经进入三期临床,覆盖共价以及非共价BTK抑制剂。
可以说,BTK领域的竞争格局已经被全球最顶级的TOP药企瓜分完毕,程度可以用激烈来形容。对于一家刚起步的中国biotech来讲,以一己之力和这些公司抗衡几乎是螳臂当车。所以,另辟蹊径成了诺诚健华值得下赌注的出路。
资金是最不用愁的。诺诚健华从建立开始就不缺融资,上市后更是如此。
虽然2022年诺诚健华续亏9.1亿,但去年科创板上市后募资29.2亿。根据2022年三季报,诺诚健华货币资金约有86.68亿元,现金流相对充沛。
该愁的是临床数据。除了奥布替尼,另一款商业化产品Tafasitamab目前仅获批在海南博鳌作为临床急需进口药品使用。其他在研产品中最快的ICP-192和ICP-723处于临床II期,预计2024~2025年才能上市。如果奥布替尼错过200多亿美元的MS市场,诺诚健华的预期或将失去支撑。因此,这场分手会让诺诚健华少一个增长点,但不会就此消亡。
而如今的市场不会再有下一个诺诚健华。
一位投资人谈到,“创始人是一个技术派,跟BTK靶点这个领域,几乎是没有太多的关系。作用大多是名气加持,此外在临床试验上有推进作用。以往,这种创始人融资是顺利的。”
他的后半句是,下一步,这样的公司不会再出现。
一位研究美国生物制药的人士分析,在比较成熟的美国市场,投资人会有专业上的独立判断,不会被所谓的光环影响。而且,业内在操作上都有共识,Biotech都得靠时间慢慢积累,资金可以加快进度,但时间肯定是需要的。“高举高打的公司,肯定不可能批量制造奇迹,一款药物开发动10~20年的技术积累是常态,以互联网投资的方式做药肯定是找死。”
当业绩下滑的巨头,带着病急乱投医的心情找的“license out”,和“试一下也没什么”的赌一下的公司,分手是必然的结果。
而下一步,中国biotech的这种“重磅国际合作”或许不会再是国际化、研发/出海实力的代名词。中国的Biotech也需要新的东西来证明自己,比如,对标全球更优的临床数据;再比如,销售额。
本文来自微信公众号:深蓝观 (ID:mic-sh366),作者:吴妮,编辑:王晨、高翼

