面对国内医药市场的持续内卷,不少药企将出海看成了破局的方向,这种做法与当年日本药企的选择如出一辙。
目标出海并没有错,但却必须建立在强大的创新能力之上,如果没有产品层面的创新作为支撑,那么最终注定将会进入到另一层内卷循环之中。只要产品竞争力强了,那么全球化自然也就是一件水到渠成的事情。
既然创新是中国药企出海的唯一出路,那么是否意味着这条路没有捷径可走呢?其实也并非如此,孤儿药策略实则就是一条中国药企出海的捷径。
针对孤儿药的布局,实则已经成为观测企业战略的一个绝佳切面,对于投资者判断企业的价值亦大有裨益。中国创新药出海的“第一步”,实则从成为孤儿药开始。
一、暗渡陈仓的MNC们
所谓孤儿药,指的是那些针对罕见病人群的小众药物(在美国是指患病人群小于20万的疾病),由于这些药物市场规模较小,导致药企研发回报率较低,为了让这些患者有药可医,美国FDA在1983年通过了孤儿药法案,从税收减免、免申请费、研发资助、加快审批、市场独占权等多个层面激励研发。

图:美国孤儿药优势,来源:中信证券
孤儿药的政策优势是显而易见的,尤其是对于尚处于创新药发展初期的我国药企而言,成为孤儿药更是能直接降低企业经营压力,最大限度地提升药品的出海成功概率。
FDA设立孤儿药的初衷是为了让罕见病患者有药可医,可巨大的政策红利却让孤儿药的定位逐渐变味,伴随越来越多MNC(跨国药企)的入局,孤儿药已经成为一种药企争夺市场的常规策略。
税收减免、免申请费等优惠措施对于MNC吸引力不大,最让它们心动的则是FDA的快速审批通道。众所周知,创新药是一个拼速度的行业,孤儿药的快速审批通道能够大幅提升药物的上市速度,尤其在失败率较高临床三期试验中,孤儿药所需的临床规模明显更小,FDA的审批也将更加宽松。
成为孤儿药后,这也意味着这款药物的获批速度得到大幅提升,这才是MNC看重孤儿药的核心原因。或许有投资者持有不同看法,孤儿药受众者少,就算提前获批又能获得多少商业化价值呢?这样的想法是较为单纯的,因为医生用药时是可以“超适应症”的,只要营销部门市场教育得当,其他适应症临床进度跟上,那么完全可以依靠“超适应症”创造营收。这种患者自愿用药的情况是合理合法的,例如康方生物去年国内上市的卡度尼利单抗就因疗效出色,出现很多“超适应症”情况。
正是因为孤儿药背后巨大的商业利益,MNC在研发一款重磅新药的时候,往往会将适应症切割为很细分的类别,竭力向罕见病的方向靠拢,争取利用孤儿药快速通道率先获批,然后再利用适应症扩增或超适应症来扩大市场。
2022年全球营收TOP 10的药物中,Humira、Keytruda、Revlimid都曾经是孤儿药,随着后续适应症的扩增,已经成为全球营收第一梯度药物,足以向市场证明,孤儿药也是可以成为“药王”的。
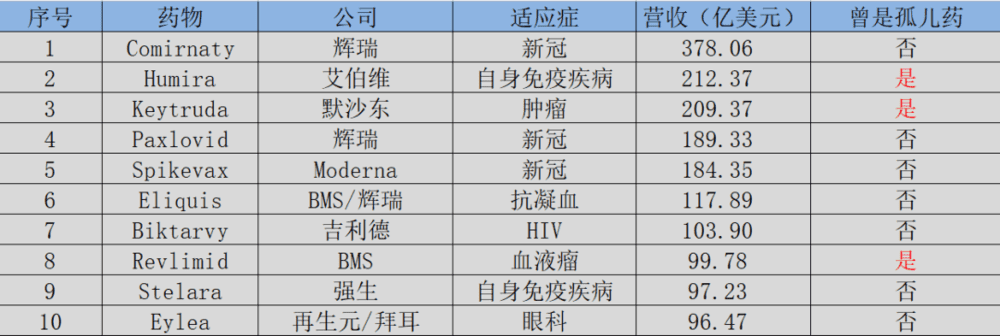
图:2022年全球营收TOP 10药物,来源:锦缎研究院
尽管获批非孤儿药适应症后,药物就会失去孤儿药的政策庇护,但这对于MNC药企而言几乎不值一提。能够更早的、更快地抢占市场,这才是MNC孤儿药策略的核心。
MNC药企的孤儿药策略,表明上响应了FDA关注罕见病患者的号召,但实际上却是为了将自身利益最大化。
二、孤儿药对中国药企的利好
对于孤儿药政策,MNC药企已经研究得十分透彻。但于中国药企而言,孤儿药的意义却不仅限于此,背后实则蕴含更深层次的三层重磅利好。
(1)适应症的地区性差异
孤儿药泛指针对罕见病的药物,但世界不同地区对于罕见病的定义却大相径庭。如美国市场定义罕见病要求患者数小于20万,而日本市场罕见病的患者数门槛却降低至5万人,澳大利亚更是2000人以下才是罕见病。
基于罕见病定义宽松程度的不同,孤儿药在全球也有着不同定义,并非全球通用概念。再加上各国疾病发生率的差异,这就使得孤儿药布局的策略性进一步提升。
如在美国,肝癌患者总数仅为几万人,是绝对意义上的罕见病;而在中国市场,肝癌患者数却接近40万人。这就意味着,国内的大癌种药物,在美国符合孤儿药的标准,其中的预期差不言自明。类似的情况还出现在肺癌、鼻咽癌等疾病之上,如果能够善用这种适应症地区性差异的话,那么对于中国药企的出海会有事半功倍的效果。
(2)美国示范效应
美国市场具有全球最完善的药物审批体系,是具有全球示范效应的。
无论药品销售有怎样的成绩,但只要获得FDA的批准,往往就意味着其拥有较强的市场信誉度。毕竟FDA是目前全球安全、质量、有效性等方面的天花板,世界上很多国家都是盯着FDA审批药物的。FDA的审批就好像是一个免检标识,如果产品顺利通过,那么进入其他市场的难度也将骤然下降。
例如百济神州的BTK抑制剂百悦泽就是很好的一个例子,其在2019年11月于美国获批上市后,很快就在加拿大、澳大利亚、俄罗斯、欧盟等其他地区获批上市,如今其商业版图已经覆盖全球50个国家和地区。如果没有FDA的获批,那么相信百悦泽将不会有如此高效的国家化效率。
获得FDA审批的药物,在其他国家监管部门获批更加容易、国际化合作更加方便,患者也更加信赖这款产品。
(3)竞争门槛大幅降低
对于财大气粗的MNC公司而言,FDA给予的财务政策可能不值一提,但对于刚起步的中国创新药企来说,这却有着极大的财务价值。
首先,获批孤儿药的产品将享受50%的临床研究和测试的税务减免,同时还将省掉数百万美元的NDA审批费,以及不菲的孤儿药研发财政补助。这些财务上的减免加到一起,极有可能为药企节省千万美元级别的支出,这对于尚未拥有持续盈利能力的中国创新药企而言,大幅缓解了药物开发压力。
此外,在失败率最高的临床三期试验中,孤儿药临床试验要求大幅放宽。不仅患者样本数大幅减少,而且还往往是单臂试验,降低了临床试验的花费。甚至有时候FDA还会对某些孤儿药特殊照顾,进一步减免临床试验例数,帮助这些药物获批上市。
这些临床阶段中的激励,帮助孤儿药的临床试验成本大幅下降,进而缩小了中国创新药企与MNC之间的资本差距。
三、孤儿药已经成为一种标签
百济神州泽布替尼和传奇生物西达基奥仑赛是目前国内药企出海的最佳范本,而它们无一例外的都是孤儿药身份。巨大的政策红利之下,孤儿药俨然成为中国药企出海的最佳路径。
纵览国内创新药企,它们对于孤儿药的关注已经越来越多,甚至各家的明星产品几乎都获得了FDA孤儿药的身份。这种趋势无疑降低了投资者对于药企管线的研判难度,一款创新药能否顺利出海,甚至能够成为明星药物,首先要取决于它能否获得FDA孤儿药的资格。换个角度而言,孤儿药正在转变为中国创新药的一种出海标签,不是孤儿药身份想要出海,难度堪比登天。
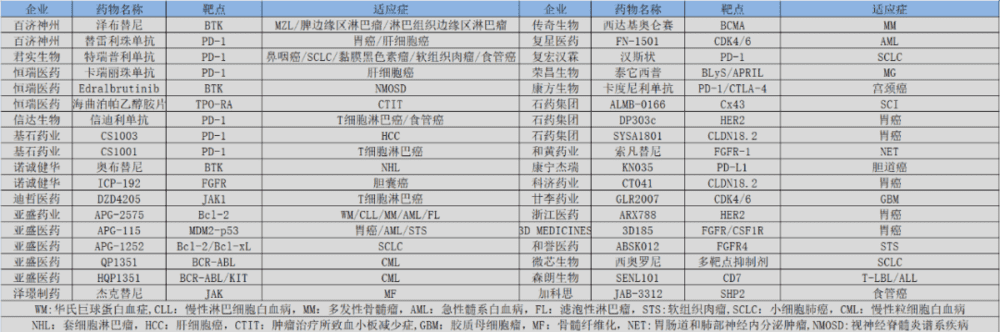
图:国内重点孤儿药一览,来源:锦缎研究院
不过,获得孤儿药资格却并不意味着胜利,恰恰相反这仅是一个开始。不同于获批上市是商业化的起点,即使管线刚刚立项不久,药企也可以向FDA申请孤儿药资格,这背后无关药效和研发。
所有投资者都知道,创新药研发九死一生,这就意味着注定有大批孤儿药无法最终获批上市,即使FDA降低了孤儿药的上市难度,但也依然需要面对严峻的研发挑战。获得孤儿药资格,只能从侧面说明药企志存高远,从立项之初就聚焦全球市场,但这个预期能否实现,亦或者多久能够实现,其实依然还是一个未知数。
尽管如此,可孤儿药依然是一项值得中国药企深度钻研的产业政策,其能够显著降低优质管线的出海成本。对于投资者而言,孤儿药则成为衡量药物价值的简易标签,如果药企想要布局全球,那么孤儿药资格将是它们必须迈出的第一步。
本文来自微信公众号:医曜(ID:yiyao-jinduan006),作者:林药师

