本文来自微信公众号:学术经纬 (ID:Global_Academia),作者:学术经纬,原文标题:《减肥易反弹?有办法了!最新〈自然〉揭示热门抗肥胖靶点的作用机制》,头图来自:pixabay
随着全世界肥胖人群持续增多,越来越多的人面临患上糖尿病、心血管疾病和脂肪肝等疾病风险。为了从源头解决肥胖衍生的疾病,许多研究都在追寻安全有效且长期有效的减肥药物。
当前肥胖治疗的药物主要是通过抑制食欲达到减重目的,一些备受瞩目的减肥药物(如司美格鲁肽)已经可以使超重或肥胖症人士的体重下降幅度超过15%,甚至20%。然而,现有的手段也并不完美,停止治疗后很容易体重反弹。如何避免反弹,长期保持战果,成为了治疗肥胖的瓶颈问题。
这就要从体重反弹的机制来了解。机体为了应对长期饮食摄入的减少和体重降低,会代偿性地降低能量消耗,这种代偿性的能量消耗降低被称为“适应性生热效应”,是停止治疗后体重反弹的一个主要原因。然而目前还没有哪种减肥药物是通过增加能量消耗来降低体重的。
好消息是,本周顶尖学术期刊《自然》新发表的一项研究中,加拿大麦克马斯特大学(McMaster University)Gregory Steinberg教授课题组王冬冬博士(唯一第一作者)领导的GDF15研究项目发表成果“GDF15 promotes weight loss by enhancing energy expenditure in muscle”。研究团队发现了可以在节食减肥期间促进能量消耗的关键机制,为开发新的减肥疗法解决体重反弹问题提供了可能性。

这种新机制的核心在于一种内分泌激素,名为生长分化因子15(growth differentiation factor-15,GDF15)。
GDF15是新近很受关注的一种抗肥胖靶点,可以降低体重、改善胰岛素抵抗和非酒精性脂肪肝(NAFLD)。然而GDF15究竟如何发挥作用,机制并不明确。
已有的一些研究猜测,GDF15通过抑制食欲来发挥生物学作用。这种激素能向后脑的两个区域传递控制食物摄入信号,以此让我们减少进食。负责此次研究的Steinberg教授曾在2019年带领团队发现,二甲双胍用于降血糖的同时可以控制食欲、减轻体重,就是通过升高GDF15水平来起作用。这一结论也得到了其他几项研究的佐证。
不过,GDF15仅仅是一种“厌食细胞因子”吗?“众所周知,饮食的摄入、体重和能量消耗之间是相互影响、动态关联的。因此,GDF15抑制食欲是否是其发挥生物学作用的唯一机制?如果不是,GDF15是通过哪些新机制发挥生物学作用?”王冬冬博士说道。

▲王冬冬博士(左)和Gregory Steinberg教授是本研究的第一作者和通讯作者(图片来源:参考资料[2];Credit:McMaster University)
在此次新研究中,王冬冬博士领导团队,基于细胞、转基因动物和人体研究,利用基因敲除、PET-CT、RNA测序、线粒体/肌纤维呼吸测试、孟德尔随机化分析等方法,对GDF15发挥生物学作用的机制展开了系统研究。
研究中,作者给一批肥胖小鼠配对设置了热量相同的“减肥餐”,但其中一半小鼠同时给予重组GDF15。根据他们的观察,在前期(10-14天),GDF15给药组和其配对喂养组有相同的降低体重作用;然而在后期,只抑制饮食的对照组体重基本维持不变,而GDF15给药组仍然在显著掉秤,而且“刷脂”效果明显,降低的主要是体脂量。
进一步分析表明,GDF15改善胰岛素抵抗和NAFLD也并不是依赖于抑制饮食。肝脏的RNA测序结果显示,GDF15能显著改善肝纤维形成的相关机制。

▲通过设置配对喂养组的小鼠实验表明,抑制食欲并非是GDF15生物学作用的唯一机制(图片来源:参考资料[1])
这一发现无疑打破了对GDF15的传统认知。既然GDF15发挥生物学作用的机制并不是完全通过抑制食欲,那其机制又是什么呢?
接下来,研究团队开展了多项实验测定了小鼠的能量消耗,分别比较了不同的环境温度、昼夜节律、喂食时间等因素的影响,都发现GDF15可以阻止代偿性的能量消耗降低,也就是造成体重反弹的适应性生热效应。
进一步探索发现,GDF15是通过GFRAL-β肾上腺素能受体轴维持能量消耗。若在小鼠中敲除GDF15的受体GFRAL,GDF15维持能量消耗和降低体重的作用以及对NAFLD的改善作用完全被抵消。而敲除交感神经系统(SNS)中的β-肾上腺素受体也会完全抵消GDF15维持能量消耗和降低体重的作用。
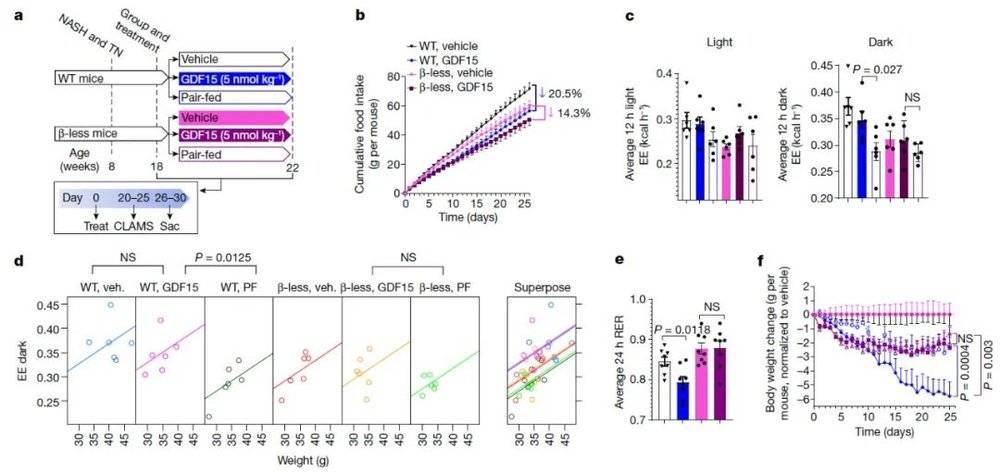
▲同时敲除β受体1、2、3(Beta-less)的小鼠完全抵消了GDF15维持能量消耗和降低体重的作用(图片来源:参考资料[1])
有趣的是,研究人员测定了受交感神经系统影响的脂肪组织,发现GDF15并没有调节脂肪生热作用,PET-CT扫描结果则显示脂肪、心脏、肝脏和肾脏的氧化代谢也都没有受GDF15影响。
最终,研究人员通过一系列实验找到了GDF15阻止代偿性能量消耗降低的靶点:肌肉组织。具体来说,GDF15调节β肾上腺素受体信号通路和肌肉生热基因,在肌肉组织中增加了钙离子介导的无效呼吸循环,抵抗控制饮食导致的能量消耗降低。
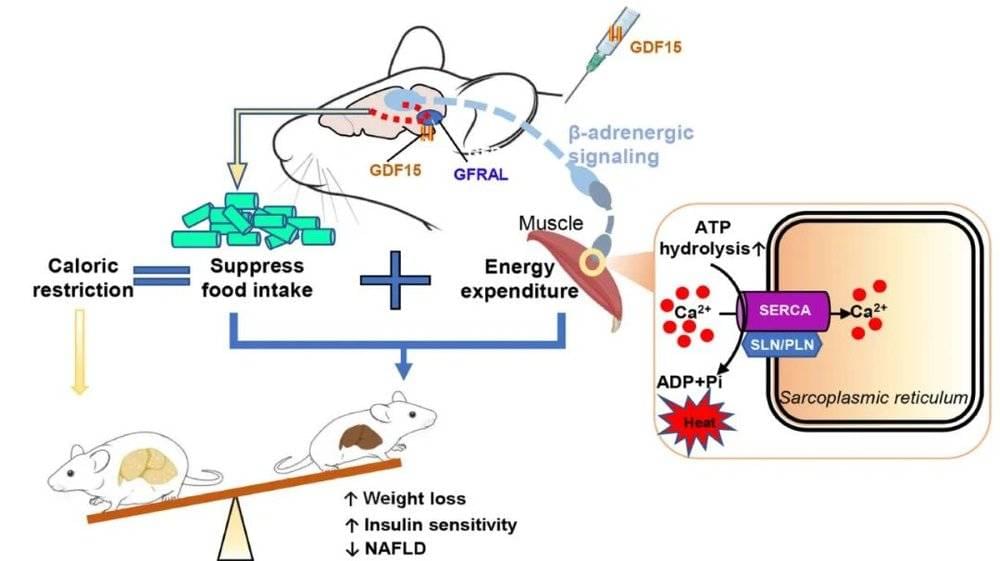
▲研究示意图(图片来源:研究作者提供)
为了探索GDF15的这些生物学效应是否能够转化到人类模型,研究团队还在三个完全独立的临床人群中测定了GDF15这些信号通路。
他们发现,血浆中GDF15水平和基础代谢率(RER)呈正相关关系,但不显著。研究人员分析可能是由于GDF15增加肌肉的钙离子无效循环,而RER是在静息状态下测定的。在GTEx数据库中,GDF15高表达组中的肌肉SLN等钙离子无效循环基因表达显著增高。最后,使用两样本孟德尔随机化方法分析了32859份样本脂肪肝与GDF15的关系,结果表明GDF15降低了人类肝脂肪水平。
Steinberg教授表示,后续还需要更多的研究在人类确认这些发现,进一步了解GDF15水平如何影响人体肌肉能量燃烧,其结果也将有助于我们理解为什么不同人通过节食减肥有不同的效果。
随着科学家们对GDF15的研究逐渐深入,或许在不久的将来,我们就有新的方法——例如将GDF15与已有的抑制食欲的减肥药相结合,帮助努力控制节食的人群不仅能有效减重,还能更长久地巩固来之不易的减肥成果。
参考资料:
[1] Dongdong Wang et al., GDF15 promotes weight loss by enhancing energy expenditure in muscle. Nature (2023) Doi:10.1038/s41586-023-06249-4
[2] McMaster University team discovers hormonal pathway that increases calorie burning during weight loss. Retrieved June 28, 2023 from https://www.eurekalert.org/news-releases/993710
本文来自微信公众号:学术经纬 (ID:Global_Academia),作者:学术经纬

