本文来自微信公众号:学术经纬(ID:Global_Academia),作者:药明康德内容团队,原文标题:《别熬夜了!只有睡觉,才能拯救你正在断裂的DNA》,头图来自:unsplash
我们为什么要睡觉?
毫无疑问,睡眠是人类最基本的需求。先不说连续几天不睡觉这种可能致死的极端情况,即使是长期睡眠不足,也已经与阿尔茨海默病、肥胖、癌症、学习能力下降等等一系列问题紧密联系在一起。我们需要睡眠,似乎不难理解。
但当我们从演化的角度思考,却发现这是一个仍有待破解的难题。从线虫、果蝇到我们人类,睡眠对于所有拥有神经系统的动物来说都是不可或缺的。但不要忘了,这些动物时刻都是生存竞争的一环。在睡眠时,丧失警惕的动物更容易被捕食,那么它们为什么即使是冒着死亡的风险也要睡觉?
在一项发表于Molecular Cell的新研究中,来自以色列的研究团队在斑马鱼中找到了睡眠的新作用,这也使得我们距离揭开睡眠之谜又近了一步。

我们的一个直观感受是,保持清醒状态的时间越长,就越容易困倦、想要睡觉。科学家用“稳态睡眠压力”来表示动物对睡眠的需求。这种睡眠压力在清醒状态下增加,入睡之后减少。那么,是什么导致睡眠压力增加至临界点,让我们不得不去睡觉;夜间入睡时,这种压力又是怎样减少的?
此前的研究为我们提供了线索——同样在清醒与睡眠状态之间交替的,是机体内的DNA损伤与修复。
清醒状态下,受紫外线照射、神经元活动、辐射、氧化应激等因素的影响,DNA损伤在包括神经元在内的细胞内积累,这其中就包含了DNA双链断裂。如果这样的损伤积累下去,会对机体健康造成严重影响,诱发认知衰退、癌症等疾病。
好在,机体内还有DNA修复机制。无论是睡眠还是清醒状态下,每个细胞内的修复系统都在持续修好断裂的DNA。但在清醒状态下,神经元中的DNA损伤依旧持续积累,这会导致损伤积累到危险的水平。这一事实也提醒人们:起到决定性作用的,或许是睡眠阶段的高效修复。
为了寻找睡眠与DNA损伤/修复的确切关系,研究团队利用经典模式动物斑马鱼进行了一系列实验。为此,他们通过能导致神经元异常兴奋的药剂,使得斑马鱼保持在清醒状态。随后,他们检测了斑马鱼神经元中DNA双链断裂的情况。
实验结果显示,清醒时神经元中DNA双链断裂显著增多。随着DNA损伤的积累,个体对于睡眠的需求也在增加。而到了某个时刻,DNA损伤积累达到阈值时,在稳态睡眠压力的诱导下,斑马鱼就进入睡眠状态。
在明确了DNA损伤的积累是诱发睡眠的驱动力后,研究者进一步找到了斑马鱼为了减少睡眠压力与DNA损伤所需的最短睡眠时间:6个小时。6个小时的睡眠足够减轻DNA损伤;而不足6小时时,DNA损伤无法得到修复,这时斑马鱼会在白天继续睡觉。
那么,具体又是哪些分子与神经机制参与了这个过程?这项研究随后进行了深入的探讨。
研究人员通过荧光标记了修复蛋白,发现在睡眠状态下,Rad52和Ku80这两种修复蛋白在神经元中积累,帮助机体在无意识间修复损伤。
随后的研究发现,一种名为PARP1的蛋白质在相关神经机制中扮演者关键角色。作为DNA损伤修复系统的一部分,PARP1是最早响应的蛋白质之一。它标记了细胞中DNA损伤的位置,并召集所有相关系统来清除损伤。与DNA损伤一样,PARP1在断裂位点聚集的情况在清醒时更多见;睡眠时则较为减少。
研究团队在控制斑马鱼过量表达PARP1时,也促进了与睡眠相关的修复;相反,抑制PARP1则关闭了进行DNA修复的信号,这时斑马鱼根本没有意识到自己困了,也不会去睡觉。在随后的研究中,这支团队还对小鼠进行了实验,发现PARP1起到类似的效果。这也进一步证实了在斑马鱼中的发现。
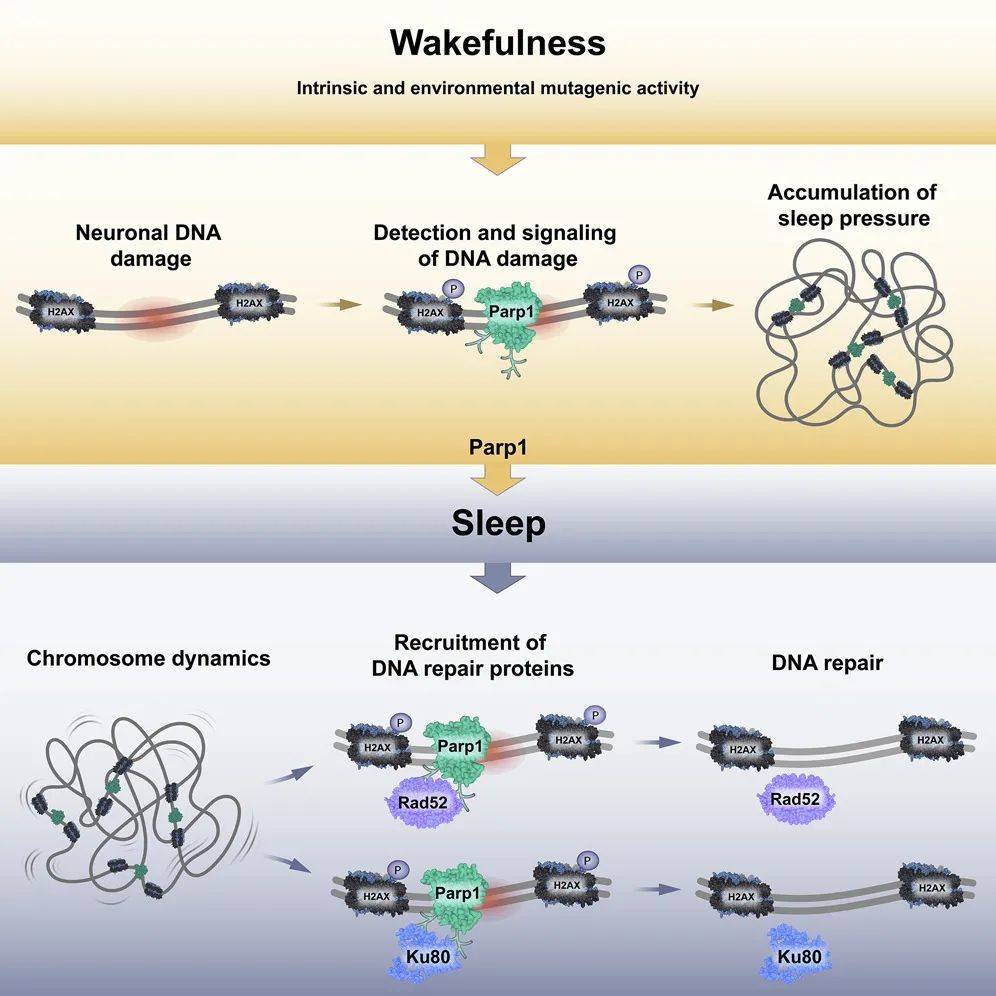
这项研究的通讯作者,以色列巴伊兰大学的Lior Appelbaum教授表示:“PARP1到达特定的阈值时,会驱使个体去睡觉,同时告诉大脑:你需要睡觉了。否则,你会积累过量的DNA损伤。”Appelbaum教授指出,了解PARP1如何明确对于睡眠的需求,是研究团队的下一个目标。
而对于我们来说,保持充足睡眠的又一个重要原因被揭开了。为了你的DNA完整与机体健康,今晚还继续熬夜吗?
参考资料:
[1] David Zada et al., Parp1 promotes sleep, which enhances DNA repair in neurons. Molecular Cell https://doi.org/10.1016/j.molcel.2021.10.026 (2021).
[2] How do we know we're tired?. Retrieved Nov 18, 2021 from https://www.eurekalert.org/news-releases/934950
本文来自微信公众号:学术经纬(ID:Global_Academia),作者:药明康德内容团队

