本文来自微信公众号:学术经纬(ID:Global_Academia),药明康德内容团队编辑,原文标题:《同日三篇重磅论文!基因编辑领域迎来新突破》,头图来自:视觉中国
今日,三篇关于基因编辑的重要论文上线,向我们展示了这一领域的无限可能。其中两篇发表于《自然-生物技术》的论文拓展了现有技术的边界,有望将所能编辑的基因长度扩展一百倍!而另一篇在《细胞》杂志上发表的论文,则进一步对一项基因编辑技术进行了改良。这些发现的问世,宣告了基因编辑又往前迈了一大步。
而说到这些进展,则离不开一个名字——刘如谦(David Liu)。

先导编辑
时间回溯到2019年10月22日。两年前,刘如谦教授团队在《自然》杂志上发表了一篇重要论文,带来了一种叫做“先导编辑”(prime editing)的全新基因编辑技术。论文上线后引来业内的点赞和热议,被认为是“极为重要”的成果。

在这项技术诞生之前,传统的CRISPR基因编辑技术会使用Cas9蛋白,在目标DNA上切出口子,造成双链DNA断裂。随后,DNA会利用同源重组等方法,在修复过程中对基因组进行编辑。
这一方法虽然有效,但很粗暴。打个比方,这就好像一页书上有错别字,为了修正书上的错误,要把这整页书给撕下来,再重新粘上一页那样。可以想象,这样的工作谈不上优雅,也容易产生潜在的问题。
![传统的CRISPR-Cas9基因编辑方法示意图(图片来源:J LEVIN W [CC BY-SA 4.0 (https://creativecommons.org/licenses/by-sa/4.0)])<br>](https://i.aiapi.me/h/2021/10/15/Oct_15_2021_02_57_20_21265210411792740.jpeg)
而先导编辑则不同。它的核心是一种由经改造的Cas9蛋白与逆转录酶(reverse transcriptase)融合而成的特殊蛋白,另一个关键是一种特殊的gRNA——pegRNA(pe是先导编辑的缩写)。它不但能够结合想要进行编辑的特定DNA区域,还自带“修改模板”。Cas9-逆转录酶融合蛋白会在pegRNA的引导下,精准地切开一条DNA链,然后根据模板,合成含有正确序列的DNA。细胞内的DNA修复机制会自动把这段新合成的序列整合进基因组。
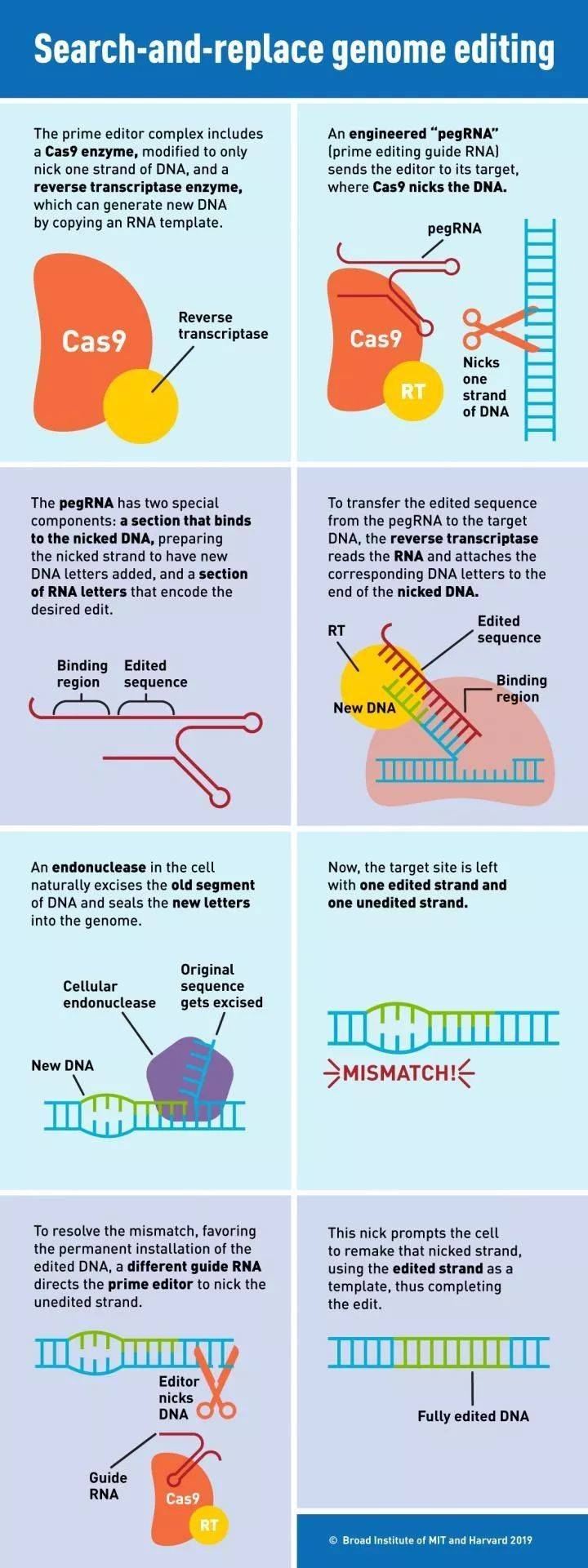
在多种人类细胞中,研究人员们证实了这一系统的编辑能力。此外,它的编辑潜力在小鼠神经元里也得到了证实。除了对单个碱基进行修改之外,这一系统还能够插入或删除特定的DNA序列。根据论文,研究人员们最多可以插入44个碱基,或是删除80个碱基。
这对于治疗人类遗传病有着重要意义。据估计,大约89%的已知人类致病变异,有望通过这一新型基因编辑技术来修复。
从一百到一万
先导编辑在问世后得到了广泛的应用,然而却有一个瓶颈尚未突破——它只能对有限长度的基因进行删除。如果一段序列超过100个碱基,就会影响这套系统的编辑效率。
今日两篇发表在《自然-生物技术》上的论文则突破了这一瓶颈。两支独立的团队各自开发了优化的先导编辑系统,可一次性精准切除至多10000个碱基!这大大拓展了先导编辑的应用场景。

第一项研究来自马萨诸塞大学的薛文教授课题组。与先导编辑中使用的改造Cas9蛋白不同,他们使用了具有完整功能的Cas9蛋白,再将其与逆转录酶融合在一起。这样的融合蛋白一次能切开两条DNA链。
同时,他们也额外加入了一条pegRNA(共两条),靶向DNA上互补的序列。而逆转录酶合成的两段新DNA则形成互补的黏性末端。当这两个末端相结合时,就可以将原本位于中间的大段DNA给删除掉。这一技术至多能删去将近一万个碱基。
![本技术的图示(图片来源:参考资料[1])<br>](https://i.aiapi.me/h/2021/10/15/Oct_15_2021_02_57_27_21265217540136730.png)
薛文教授指出,有大约14%的突变类型涉及到大段的插入、复制、或是复杂的DNA重组。这些难以用传统的CRISPR技术去解决。而这一工具有望为带有这些突变的患者带来希望。
尽管这一技术目前无法应用于人类,但研究人员们在小鼠中做了概念验证实验。在一种由于大段DNA插入引起的酪氨酸血症小鼠中,研究人员们应用这套新型先导编辑,成功治疗了它们的疾病。在挪走一段长达1300多碱基的致病序列后,小鼠能成功产生原本缺乏的蛋白,恢复健康。相比之下,对照组小鼠则饱受肝脏损伤的困扰。

第二项研究来自华盛顿大学的Jay Shendure教授课题组。与第一项研究略有不同,研究人员们还是使用了先导编辑最初使用的特殊Cas9蛋白,即每次能切开一条DNA。但在两条pegRNA的作用下,它同样能达成删除中间序列的效果。
在人类的肾脏细胞中,研究人员们做了一系列删除测试,范围从20个碱基到10000个碱基不等。尽管编辑效率还不是非常高,但这些实验的积极结果验证了这一技术的可行性。更关键的是,编辑的成功与否,并不取决于删除序列的长短,更多取决于选择的序列。这也进一步表明进行大段DNA删除的可行性。
![本技术的图示(图片来源:参考资料[2])<br>](https://i.aiapi.me/h/2021/10/15/Oct_15_2021_02_57_32_21265222397016999.png)
研究人员们指出,我们的基因组里有大段所谓的“垃圾DNA”。它们虽然不编码蛋白,但在基因调控上起到了非常重要的作用。这款新型基因编辑工具的问世,将让我们更好地研究这些调控序列的作用。
提高编辑效率
有意思的是,在这两篇重要论文诞生的当天,最初开发先导编辑的刘如谦教授团队也在《细胞》杂志发文,进一步对这款重要工具进行改良。

这篇论文提到,尽管先导编辑能精准地切开DNA,但我们对影响编辑效率的细胞因素还知之甚少。在本研究中,科学家们使用基于CRISPR干扰(CRISPRi)的技术,进行了大规模的筛选,发现DNA的错配修复会影响到先导编辑,产生预期外的插入/删除突变。
为此,研究人员们开发了更先进的先导编辑系统,能瞬时表达抑制DNA错配修复的蛋白,以提高编辑效率。分析表明,与早期的先导编辑系统相比,新系统的编辑效率要高出2.0到7.7倍。
![本研究的图示(图片来源:参考资料[3])<br>](https://i.aiapi.me/h/2021/10/15/Oct_15_2021_02_57_34_21265225268657866.jpeg)
而通过优化先导编辑所需的蛋白,他们还能进一步在海拉细胞系中提高先导编辑的效率,幅度达到2.8倍。
刘如谦教授今日在社交媒体上连发12条消息,向大家兴奋地介绍他们团队的发现。他指出,在七种哺乳动物细胞的191种编辑里,新型先导编辑系统都带来了显著的编辑改善。这些发现也丰富了我们对于先导编辑的认知。
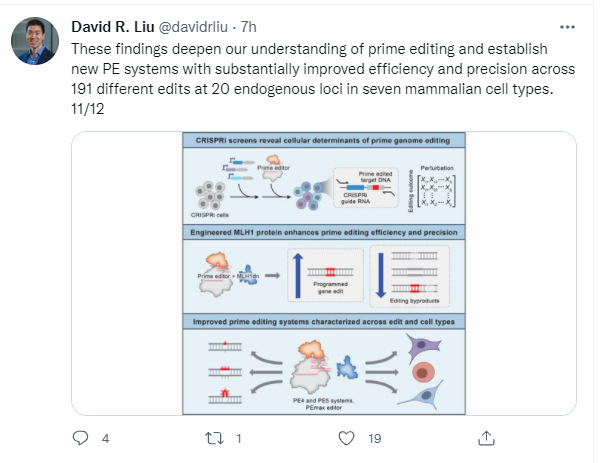
关于两篇《自然-生物技术》论文对于先导编辑的衍生应用,刘如谦教授给了很高的评价。他认为这是先导编辑的“优雅变体”,能拓展精准编辑的长度,矫正大量已知的致病基因插入。无论对基础科研,或是合成生物学的应用,都有很高的价值。
CRISPR基因编辑技术自诞生以来,已经改变了生物技术领域的格局。也正是因为其重要性,它在去年斩获了诺奖的殊荣。今日的这三篇论文,让我们看到了基因编辑的未来无限可能。我们也期待这项技术能得到进一步完善,最终更好地造福人类!
参考资料:
[1] Jiang, T., Zhang, XO., Weng, Z. et al. Deletion and replacement of long genomic sequences using prime editing. Nat Biotechnol (2021). https://doi.org/10.1038/s41587-021-01026-y
[2] Choi, J., Chen, W., Suiter, C.C. et al. Precise genomic deletions using paired prime editing. Nat Biotechnol (2021). https://doi.org/10.1038/s41587-021-01025-z
[3] Peter J. Chen et al., (2021), Enhanced prime editing systems by manipulating cellular determinants of editing outcomes, Cell, DOI:https://doi.org/10.1016/j.cell.2021.09.018
[4] New CRISPR tools could fix diseases caused by large DNA rearrangements, scientists report, Retrieved October 14, 2021, from https://www.statnews.com/2021/10/14/new-crispr-tools-could-fix-diseases-caused-by-large-dna-rearrangements-scientists-report/
本文来自微信公众号:学术经纬(ID:Global_Academia),药明康德内容团队编辑

