
作为人类首款获批上市的 mRNA 疫苗,它有着极高的有效率,也伴随着吸引眼球的不良反应报道……近几个月来,BNT162b2 一直处于社交舆论风头浪尖,关于它的赞誉或争议从来就没有停歇过。
甚至看到这里,你可能对 BNT162b2 还感到很陌生,因为你更常听到的名字叫「辉瑞疫苗」。
而我今天想和大家聊的是,这款 mRNA 疫苗背后的中国力量。
一款疫苗从理论设计到临床试验,需要太多科学家的智慧与付出。
我们说一些中国科学家的故事,没有他们的努力,或许这款 mRNA 疫苗会推迟上市,甚至中道崩殂。
病毒序列
mRNA 疫苗是一种全新的疫苗,它的疫苗设计原理和我们现有的疫苗(比如减毒活疫苗、灭活疫苗等)都不太一样。
这里我们引用美国 CDC 对 mRNA 疫苗的介绍:为了触发免疫反应,许多疫苗会将一种减弱或灭活的病毒(或细菌)注入人体内。但 mRNA 疫苗并非如此,该疫苗教会我们的细胞如何制造出一种蛋白质,甚至一种蛋白质片段,从而触发我们体内的免疫反应。
以往开发针对某种病毒的疫苗,必须先获得病毒株,因为病毒株是抗原的基础。然而,mRNA 疫苗只需要抗原的基因序列即可。对于新冠病毒来说,mRNA 疫苗只需将编码新冠病毒S蛋白的 mRNA 送到我们的细胞内,通过人体细胞制作 S 蛋白。
这就是 mRNA 疫苗的最大优势之一了:不需要获得病毒株,只需要病毒的基因组序列。
2019 年 12 月 26 日,上海市公共卫生临床中心收集到一千公里外、来自武汉市中心医院的不明原因肺炎患者标本一份。
2020 年 1 月 5 日凌晨,研究团队从样本中检测出一种新型 SARS 样冠状病毒(就是今天肆虐全球的新冠病毒),并通过测序获得了病毒的全基因组序列。
1 月 11 日,第一个新冠病毒的完整基因组序列公布。
 新冠病毒基因组序列(图源:genebank)
新冠病毒基因组序列(图源:genebank)自此,全世界的科研人员第一次看到了这个日后在全球感染数千万人的病毒的真面目,各国的科研人员立刻行动起来,无论是研发疫苗还是研发病毒的检测试剂盒,新冠病毒的基因组序列都极为重要。
无论身处地球哪个角落,mRNA 疫苗的研发人员并不需要想方设法获得新冠病毒株本身,只需要公布的基因序列,就可以快速设计出 mRNA 疫苗,将原本需要至少数月的时间压缩至两周以内。
晚一天公布序列,疫苗可能就晚一天出来,就又会有几十万人感染上新冠病毒。
疫苗抗原
对于 mRNA 疫苗来说,获得基因组序列,这只是万里长征的第一步。
接下来的问题就是,我们应该选择什么样的抗原来研发疫苗?
新冠病毒上面主要四种结构蛋白,分别是刺突蛋白(Spike Protein,简写是 S)、膜蛋白(M)、包膜蛋白(E)和核衣壳蛋白(N)。
当新冠病毒入侵人体之后,由于它本身有几种不同的蛋白,因此人体会产生不同的抗体。然而,并非所有的抗体都有抗病毒的作用。
比如新冠病毒表面的 M 蛋白和 E 蛋白,这两种蛋白并不介导病毒与人体细胞表面受体的结合,因此相应抗体与它俩结合后,很可能也不影响病毒进入细胞。
基于科学家们以往对于其他冠状病毒的研究积累,新冠病毒的 S 蛋白由于介导了新冠病毒和人体细胞表面 ACE2 受体的结合,最有可能包含最主要的中和抗体表位。针对 S 蛋白的中和抗体可以阻止新冠病毒与受体的结合,从而真正阻止病毒入侵人体细胞。
新冠病毒传染性更强的一个原因,也在于它的 S 蛋白与 ACE2 受体的结合能力远强于 SARS 病毒。
因此新冠疫苗的设计,就要从 S 蛋白开始。
在侵犯细胞的过程中,S 蛋白会出现构象的变化,表现为病毒与细胞融合前和融合后的构象是不同的。
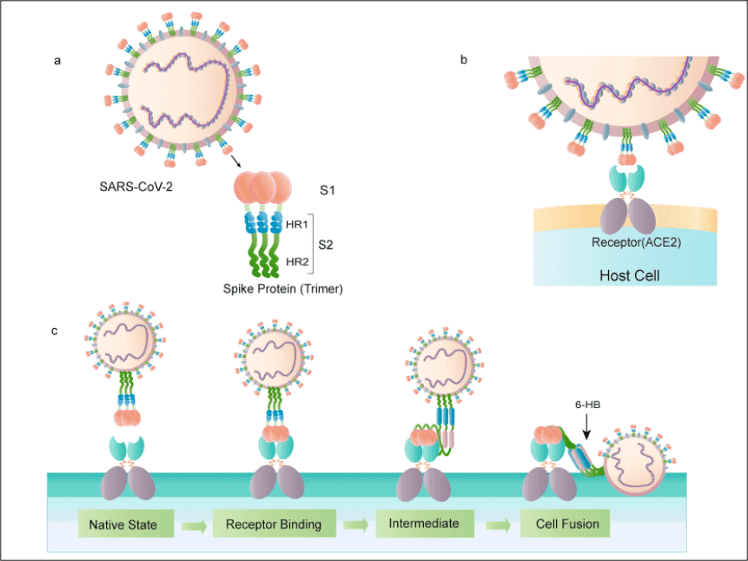 新冠病毒 S 蛋白示意图(doi:10.1038/s41401-020-0485-4)
新冠病毒 S 蛋白示意图(doi:10.1038/s41401-020-0485-4)无论是 SARS、MERS 这两种高致病性冠状病毒,还是现在的新冠病毒,它们的 S 蛋白都存在一个重要问题——结构极不稳定。
S 蛋白构象的改变是导致低表达量和低稳定性的主要原因,可能会导致免疫原性降低,使得疫苗无法产生足够的中和抗体滴度。
这个问题,最终通过一个技术的发明而得以解决。科研人员发现,通过添加 2 个脯氨酸(Proline)突变,就能稳定住冠状病毒的 S 蛋白。
这项技术,简称为 S-2P。它就像在蛋白中加入了钢筋支架,使得蛋白质不容易变形。这样 S 蛋白在进入人体以后,就会长久地维持活性状态(融合前构象),激发免疫系统产生更有效的免疫反应,即针对融合前构象的中和抗体才能在病毒与细胞融合之前结合以阻断入侵;如果蛋白构象变成融合后构象,即便能诱导出很好的抗体反应,抗体的中和效力也将大大降低。
在 I / II 期的临床试验当中,BNT162b2 疫苗在志愿者体内诱导出的中和抗体滴度相当于康复者血清的 3 倍左右,也得益于 S-2P 技术的运用。
而这个重要技术的发明人之一,是 McLellan 实验室的中国科学家王年爽博士。
王年爽博士发明的 S-2P,对今天许多国家的新冠疫苗开发都非常重要,多种不同技术路线的新冠疫苗都用到了这一技术,包括两种 mRNA 疫苗(BNT162b2、mRNA-1273)、强生的腺病毒载体疫苗和 Novavax 的基因重组蛋白疫苗、Sanofi Pasteur 和 GSK 联合开发的重组蛋白疫苗。
一名中国科学家的辛勤工作成果,未来将被运用到了全球数十亿支疫苗当中。
 王年爽等人的研究论文
王年爽等人的研究论文临床试验
对于 mRNA 疫苗而言,病毒序列有了,合适的抗原也找到了,接下来最重要的一件事,就是临床试验了。
唯有通过设计严格的临床试验,并且这些数据获得药监部门的认可,疫苗才能最终上市。
我们上面提到,你对 BNT162b2 的名字感到陌生,是因为你更常听到的名字叫「辉瑞疫苗」。实际上,BNT162b2 是全球协作的产物,是德国、美国和中国科研人员共同努力的成果。
BNT162b2 的研发来自于德国 BioNTech 公司(这点你从疫苗的名字就能看出),而中国复星与美国辉瑞都是德国 BioNTech 疫苗的合作方,复星负责大中华区的疫苗销售试验开发,辉瑞负责大中华区以外的所有国家与区的销售。
BioNTech 是一家位于德国美因茨的生物公司,创始人 Ugur Sahin 和 ÖzlemTüreci 是一对来自土耳其的移民夫妻,这家公司专注于免疫治疗,主要技术包括 mRNA 疫苗、基因治疗以及单克隆抗体等技术。(关于这对夫妻的故事可以回顾丁香园往期文章:身价飙升 300 亿:这对医生夫妻一个月内连整 20 种新冠疫苗)
2020 年 1 月,在获得新冠病毒的基因组序列后,BioNTech 就启动了光速(Lightspeed)计划,开始了对新冠 mRNA 疫苗的研发工作。
在这个时候,来自中国的科研人员就已经注意到,mRNA 疫苗可能会在这次疫情当中起到重要的作用,因为相对于传统疫苗 mRNA 疫苗具有一些显著优势:
不带病毒成分,没有感染风险
研发效率高,能快速应对病毒突变
具有体液免疫和细胞免疫双重机制,免疫原性强
于是在 2 月初,正在美国波士顿的中国科学家回爱民博士就与 BioNTech 的 Ugur Sahin 博士见面,协商中德两国共同开发新冠 mRNA 疫苗事宜。
3 月 13 日,经过双方科研人员的努力,复星与 BioNTech 签署了正式的合作协议,而此时距离双方首次见面仅仅过去 6 周时间。
根据协议条款,BioNTech 主要负责该疫苗的技术研发,而复星负责疫苗在中国的临床试验开展、合规注册等工作,推动该疫苗在包括中国大陆和港澳台地区的上市。
四天之后,辉瑞也与 BioNTech 签订了合作协议,辉瑞负责该疫苗在大中华区以外的市场。
在 BioNTech 最早选择出的四种候选疫苗中,除了 BNT162b2,还有另外三种分别是 BNT162a1、BNT162b1 和 BNT162c2,这四种候选疫苗的主要区别在于抗原靶点和剂数,比如 BNT162b1 设计的抗原靶点是 RBD 三聚体,而 BNT162b2 用的则是使用 S-2P 技术的 S 蛋白全长。
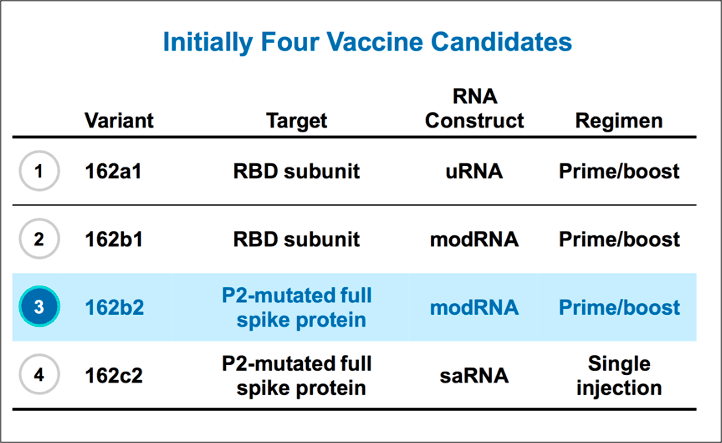
BioNTech 最早选择出的四种候选疫苗
从复星科学家最初接触 BioNTech,到在中国开展动物试验(小鼠攻毒试验),仅仅花了不到 3 个月时间;7 月 18 日,BNT162b1 在中国的 I 期临床试验启动;11 月 24 日,BNT162b2 在中国的 II 期临床试验启动。
相比以前动辄数年的 I / II 期临床试验,mRNA 疫苗在中国能够这么快推进,并且是严格、完整遵循临床试验流程的推进,离不开中德双方科学家的共同努力。
合作
2020 年 1 月 25 日,农历庚子年正月初一,这可能是大多数中国人一生中印象最深刻的一个春节,全国各地多支医疗队紧急增援湖北。
2021 年 1 月 25 日,得益于中国科学家过于一年来的不懈努力,BNT162b2 最终在 1 月 25 日于中国香港紧急获批,让中国人在抗疫战争中又多了一种非常重要的武器。
最后,mRNA 新冠疫苗能成功在大中华区的落地,我们要感谢所有为此努力过的中国科学家们,以及监管部门对于 mRNA 疫苗这种新事物的快速审批。
抗疫胜利并非依靠个人英雄主义,抗疫胜利终将是集体主义的成果。
如同张文宏医生所说:「不仅仅是医生、护士,乃至居委会干部、民众、警察、海关、道口,是无数的抗疫民众组成的免疫屏障,阻挡了疾病的蔓延。每个人都是战士,都是英雄,这才是真正的群体免疫。」
今天,全球新冠确诊累计病例数超过 1 亿,我们需要前所未有的合作。
人类共同的敌人是新冠病毒,而人类唯一的竞争对手,是时间。(策划:gyouza)
致谢:本文经 中国科学院微生物学博士、知名科学博主 @二手的科学家 专业审核
【注】
中国科学院微生物学博士 @二手的科学家 审核意见:
新冠 mRNA 疫苗的研发离不开各国科学家和各国监管部门的紧密合作,同时,也离不开基础科研的长期积累。
上文中提到的「S-2P 技术」,正是一群科学家多年来将结构生物学和疫苗研发紧密结合的产物,而并非新冠病毒爆发后才有的一蹴而就。
这里补充一个小故事。
上世纪 60 年代,呼吸道合胞病毒(RSV)灭活疫苗在临床试验中的失败,让 RSV 疫苗的研发一蹶不振。直到 2013 年,科学家发现 RSV 的主要抗原 F 蛋白,存在融合前和融合后的构象,而融合前的不稳定构象,才能诱导更有效中和性保护抗体。这篇文章里面也有很多中国科学家,通讯作者 Barney Graham 博士同样需要我们记住。
2017 年,王年爽博士作为第一作者之一以及 Barney Graham 团队应用结构生物学技术在 SARS 和 MERS 病毒的 S 蛋白中发现,两个脯氨酸的替换(S-2P 或 S-PP)不仅可以稳定 S 蛋白的融合前构象,且融合前构象的 S 蛋白可以在小鼠中诱导更高滴度的中和抗体。
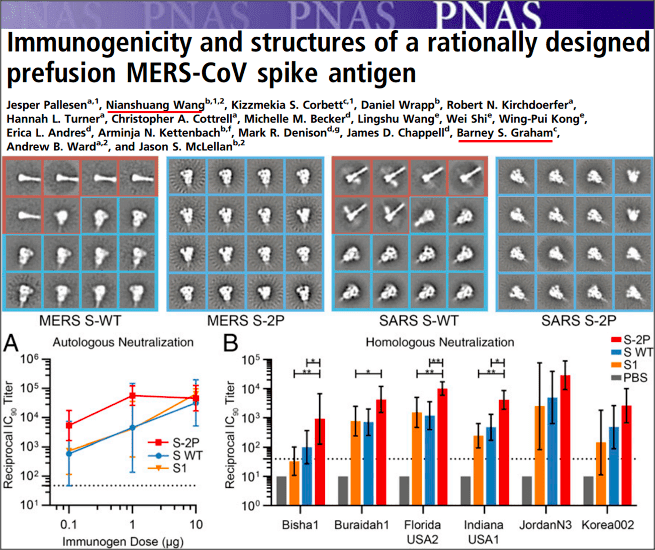
2020 年,Barney Graham 团队和 Moderna 公司紧密合作,最终将基础研究转化为了造福人类的上市产品。
从 RSV 疫苗的失败到发现抗原构象变化对于疫苗效力的显著影响,从 SARS、MERS 的研究到新冠病毒的应用,积累了几十年的基础研究,才造就了 mRNA 新冠疫苗的开发速度。
我们呼吁未来我们的社会能为基础的科学研究更多一些包容,更多一些时间。

