11月16日,Vertex制药公司和
CRISPR Therapeutics成立于2013年,由诺奖得主Emmanuelle Charpentier、Rodger Novak和Shaun Foy联合创办。

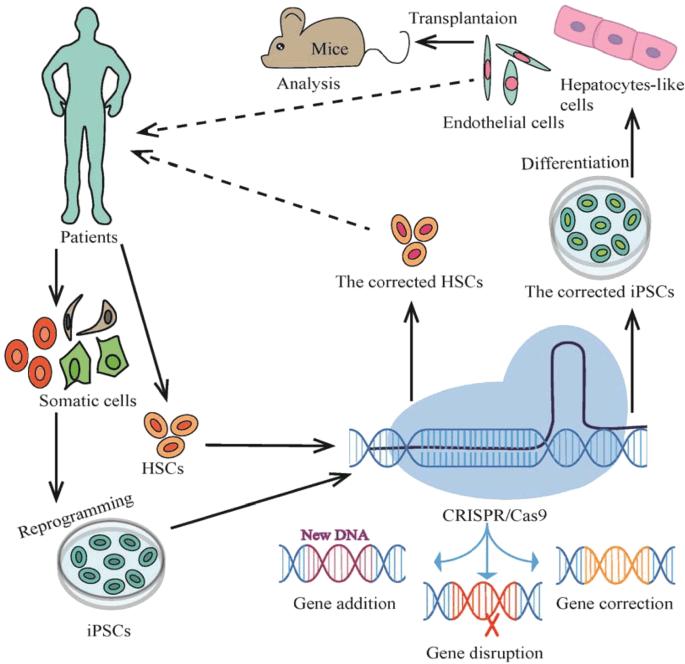
CASGEVY是一种CRISPR/Cas9基因编辑疗法,用于治疗镰状细胞病(SCD)和输血依赖性β地中海贫血(TDT)。
它适用于治疗12岁及以上患有复发性血管闭塞危象的镰状细胞病患者,这些患者具有βS/βS、βS/β+或βS/β0基因型,适合造血干细胞移植并且没有人类白细胞抗原匹配的相关造血干细胞供体。
CASGEVY同样适用于治疗12岁及以上适合造血干细胞移植且无法获得与人类白细胞抗原相匹配的相关造血干细胞供体的患者的输血依赖性β地中海贫血。
尽管在英国符合该疗法的患者估计只有2000个,但背后的意义重大。因为它让人们看到监管部门对创新疗法的态度。
“今天是科学和医学领域历史性的一天:CASGEVY在
“我希望这是这项诺奖技术众多应用中的第一个,可以造福符合条件的患有严重疾病的患者”,CRISPR Therapeutics董事长兼首席执行官Samarth Kulkarni表示。
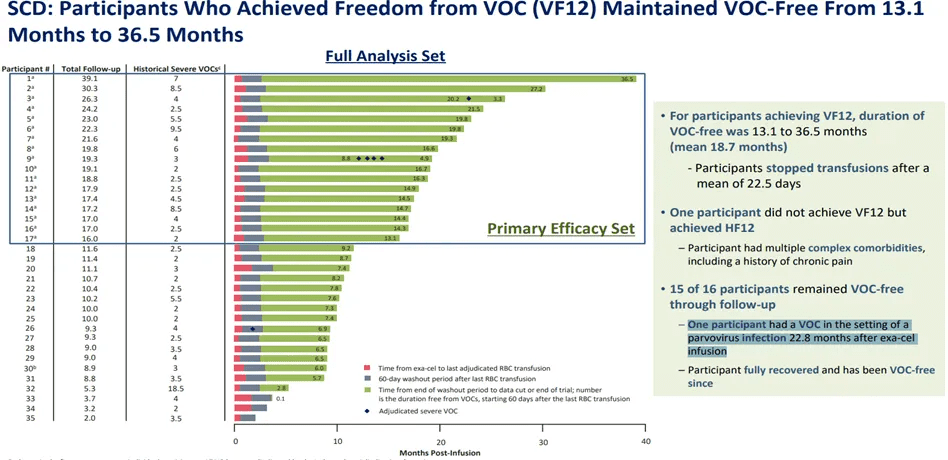
CASGEVY治疗效果怎么样?
在CASGEVY治疗SCD和TDT的两项全球临床试验中,试验达到了各自的主要终点——即至少连续12个月摆脱严重VOC或独立于输血。一旦实现,这些患者有望终生受益。在这些正在进行的研究中,迄今为止接受CASGEVY治疗的97名SCD和TDT患者的安全性总体上与白消安(Busulfan)和造血干细胞移植的清髓性调节一致。
“这项授权为符合条件、正在等待创新疗法的患者提供了一个新的选择,我期待患者尽快获得这种疗法。”伦敦帝国理工学院教授Josu de la Fuente表示,他是CLIMB-111和CLIMB-121研究的首席研究员。
关于镰状细胞病
镰状细胞病(SCD)是一种遗传性血液疾病,会影响红细胞,而红细胞对于将氧气输送到身体的所有器官和组织至关重要。由于血细胞畸形或“镰状”,SCD会导致严重疼痛、器官损伤和寿命缩短。患有SCD的人可能会经历痛苦的血管堵塞,也称为血管闭塞危象(VOC),这可能导致急性胸部综合征、中风、黄疸和心力衰竭症状。个体还可能出现贫血,这可能导致终末器官损伤和过早死亡。血管闭塞危象是SCD的标志,通常会导致严重的疼痛。
目前,SCD的标准治疗方案主要是对症治疗,不能充分解决疾病负担或减轻慢性护理的需要。大多数情况下,治疗的重点是缓解疼痛、尽量减少器官损伤、保持水分和退烧,需要药物治疗,有时需要每月输血和经常去医院就诊。SCD的唯一治疗方法是来自匹配捐献者的干细胞移植,但这种选择仅适用于一小部分SCD患者。SCD需要终身治疗并大量使用医疗保健资源,最终导致预期寿命缩短、终生收入和生产力下降。在
关于β地中海贫血
β地中海贫血是一种遗传性血液疾病,会影响红细胞。红细胞缺乏,也称为贫血,是β地中海贫血的主要表现。由于这种贫血,患有β地中海贫血的人可能会感到疲劳和呼吸急促,婴儿可能会出现发育迟缓、黄疸等问题。β地中海贫血的并发症还包括脾脏、肝脏和/或心脏肿大;骨骼畸形;以及青春期延迟。
β地中海贫血的治疗是个性化的,取决于每个人所经历的疾病的严重程度。许多人必须定期输血才能将健康的捐赠血液输送到身体中。这需要多次去医院就诊,并且还会导致不健康的铁积聚。如今,来自匹配捐献者的干细胞移植是一种治疗选择,但仅适用于一小部分β地中海贫血患者。β地中海贫血需要终身治疗并大量使用医疗保健资源,最终导致预期寿命缩短、生活质量下降以及终生收入和生产力下降。在
关于CASGEVY疗法
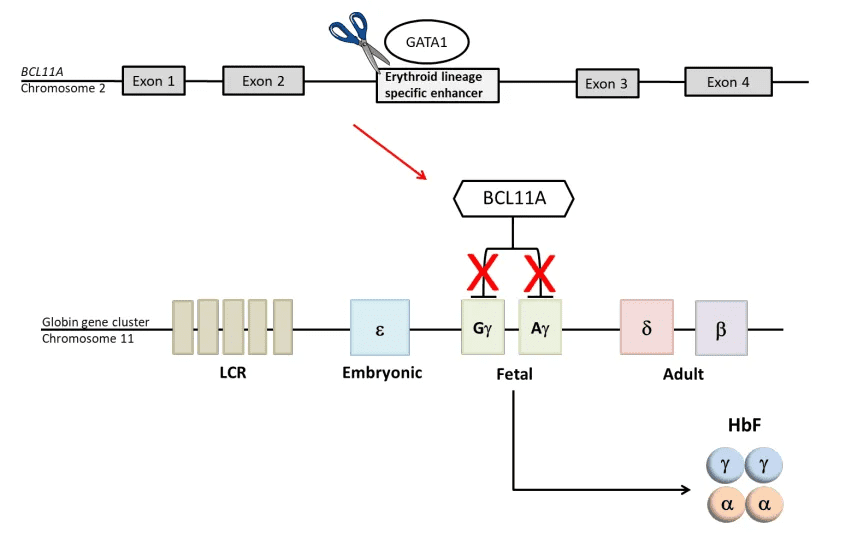
exa-cel的工作原理
CASGEVY是一种转基因自体CD34+细胞富集群,其中含有通过CRISPR/Cas9在BCL11A基因的红系特异性增强子区域进行离体编辑的人类造血干细胞和祖细胞。正在进行的关键试验的最新数据已于2023年6月在
本文来自微信公众号:深究科学 (ID:deepscience),作者:常春藤

