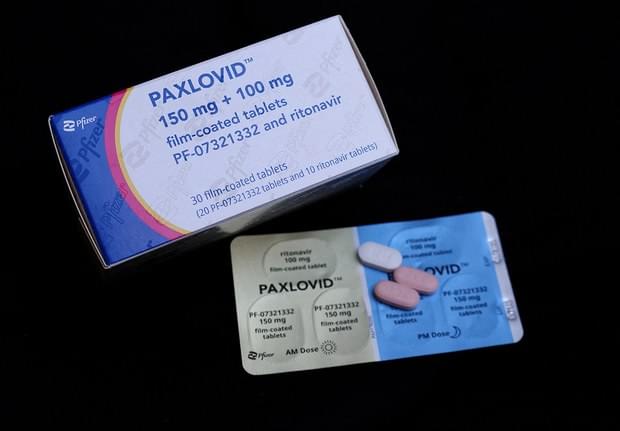
Paxlovid医保谈判出局后,沉寂许久的“专利强制许可”再次成为社会关注的热点,一些医疗界、法律界人士呼吁中国首次施行“专利强制许可”,以满足重大突发公共卫生危机发生时,我国对特效专利药品的紧迫需求。
撰文 | 汪航、燕小六
1月8日,2022年国家医保药品目录谈判工作正式结束,备受关注的辉瑞新冠口服药Paxlovid最终因报价高未能入选。这意味着,临时医保报销政策到期后,即今年3月31日以后,患者需自费购买该药品。
作为一款治疗新冠的药物,Paxlovid于2022年2月在国内获批上市,相继被纳入我国第九版、第十版新冠诊疗方案,用于治疗发病5天以内的轻、中型且伴有进展为重症高风险因素的成年患者。在北京协和医院、四川华西医院等机构发布的新冠诊治方案或推荐中,Paxlovid均被列为抗病毒治疗的推荐药物。
在多地进入新冠重症高峰的大背景下,Paxlovid受到市场追捧,且“一药难求”。当前,Paxlovid已在多地社区卫生中心可以开具,临时医保报销政策实施期间,医保支付价格为1890元/盒,按报销比例90%计算,患者仅需自付189元。但在一些非正规渠道,每盒甚至被炒到了上万元。
此次医保谈判出局后,对多数人而言,每疗程约2000元的价格并不便宜。对此,知名微博大v“成都下水道”公开呼吁,行使“药品专利强制许可”的权利,生产中国版Paxlovid仿制药。
这一提议近期已在医疗界、法律界中引起广泛讨论。稍早前,刘书庆等4名律师公开请求国家卫健委对Paxlovid扩大进口量,并要求辉瑞同意在国内销售仿制药,否则“应当实施专利的强制许可”。
“专利强制许可”是指政府强制给予除专利权人之外的第三人实施某项专利的权利,而Paxlovid的强制许可国际上也已有先例,如印度政府已在去年批准印度公司强制仿制此药,并在印度紧急用于对抗COVID-19流行。
《中华人民共和国专利法》第五十四条规定,在国家出现紧急状态或者非常情况时,或者为了公共利益的目的,国务院专利行政部门可以给予实施发明专利或者实用新型专利的强制许可。不过,我国的“专利强制许可”至今仍处于“零实践”。
在此背景下,如何看待部分临床医生和行业专家对Paxlovid实施“专利强制许可”的呼吁?如今是否已经满足启用的时机和条件?“医学界”就此请教了中国药科大学药品监管科学研究院执行院长、国家药物政策与医药产业经济研究中心执行副主任邵蓉、复旦大学公共卫生学院教授胡善联和上海大邦律师事务所合伙人、专利律师袁洋。
以下为专家们对相关问题的回答:
医学界 : Paxlovid因报价高未能成功进入医保,对此,有临床医生和行业专家表示,可参照印度合理合规地使用WTO所赋予的权利,生产中国版P药,您如何看这一建议?
邵蓉:启动专利强制许可需要特别审慎对待。截至目前,我国放开疫情管控措施已经有一个月了,应当评估国家利益和公共利益是否出现紧迫状态、P药的临床价值、市场是否有类似治疗药物替代、是否有正在临床研究和审批的类似药物加快上市,等等,综合评估国情现状后才能决定是否启动强制许可。因为专利强制许可一定程度上是对法律原则的变通,一个国家随意/轻易/经常启动专利强制许可,不断挑战、破坏法治尊严,一定会导致创新者信赖危机。试想,如果创新者对我们不信赖的话,会否影响未来的创新产品、创新技术进入我国?如果是,这个影响是无法估量的。
事实上,P药医保谈判没有成功,涉及到谁支付、支付多少的问题,确实一定程度上因为这个负担问题影响了部分患者对该药的可及性,但还不足以成为提起专利强制许可的必然理由。所以应当全面评估后,审慎决定是否专利强制许可。
胡善联:新药研发是艰辛而漫长的,其获批上市后会有一个专利权期限,可能8-10年。在此期限内,新药售价高,不能仿制。那么,为确保发展中国家在重大的公共卫生事件中,能够获得新药,国际上有两种做法。
第一种做法叫“平行进口”,是指第三人在未经专利权持有人许可的情况下,将在一国市场经持有人许可或经其同意销售的专利药品,进口到另外一个国家销售的行为。第二种就是申请“专利强制许可”。即,我不遵照你的专利要求,强制仿制相关药物,简称为“强仿”。
2021年11月,药品专利池(Medicines Patent Pool, MPP)许可协议宣布,与Paxlovid原研药企辉瑞达成协议。辉瑞同意将这个药的专利放入专利池,允许其他国家和地区的仿制药制造商生产,且不会对低收入国家的药物销售、收取特许权使用费。这意味着从那时起,Paxlovid就没有公共专利了。
2022年3月17日,MPP宣布,与全球35家企业签订许可协议、委托生产Paxlovid仿制药。其中有5家中国企业,有的仅获授权、生产原料药,也有的可同时生产原料药和仿制药。这些药物会供给全球95个中低收入国家和地区,覆盖全球约53%人口。中国不在这一供给名单中。
如果中国现在强仿Paxlovid,好处是在公共卫生事件中,我们能改善国民健康、提高药物可及性。反过来说,这会对整个世界的贸易造成较大影响,有损中国的大国形象。目前,我们致力于改善中国的营商环境,为了一个药、损失世界市场,得不偿失。
医学界: 截至目前,药品专利强制许可在我国仍处于零实施状态,您认为背后可能有哪些原因?如何评估启用的时机和条件?
邵蓉:我国的药品专利强制许可制度是专利法规定的,但在实践中仍处于“真空状态”,总体上还是非常谨慎的,需要科学和理性的态度。除了刚才提到的挑战法治尊严、有损法治声誉外,还要考虑我们自身的发展,轻易/随意/经常启动专利强制许可,会严重影响创新者创新的积极性,对我国医药企业研发和创新的能力提升产生消极影响。
如果想要启动专利强制许可,首先,必须要对国家利益和公共利益的紧迫性进行全方位的评估和认证,这一过程必须非常缜密,即如果不采取这一措施,国家利益和社会公共是不是会面临更大的重创?
其次,还要考虑我国是不是已经有了类似的药物,包括临床研究管线中的药物,用临床数据说话,将临床研究中的药物和上市注册的药优先审评、附条件批准推向市场,以满足多方需要,解决供给不足的问题。尤其对于Paxlovid相同作用机理的药品,如果有一定的临床数据支持,药监部门可以附条件批准,促早日上市,惠及更多患者。
胡善联:十多年前,世界卫生组织有代表到中国访问,曾到我们单位,征求我对“强仿”的意见。当时,中国就专利保护等形成法律依据,但至今都没做过“强仿”。同期,印度对不少高价进口药物做过“强仿”。由此,很多国家对印度进出口药物要求严格,认为其市场不够规范,不遵照专利法。
回到Paxlovid上,Paxlovid对轻度和中度新冠病毒感染者门诊患者有一定治疗效果,包括减少死亡和住院,但不是神药。就我国最新版布的第十版诊疗方案,Paxlovid是其中一个药,但不是唯一的治疗药物。
更重要的是,我国致力于新冠治疗药物研发,如VV116、SIM0417等国产药几个月后或可能获批、上市。在这种情况下,“强仿”Paxlovid仍需要几个月时间,还需要进行生物等效性试验,证明疗效后才能上市。假如我们的仿制药效果不好,那也没有强仿的必要。
袁洋:Paxlovid是新药,2021年申请专利。在新冠疫情的非常情况下,是为了公共利益的目的,若实施“强制许可”,应当适用《中华人民共和国专利法(2020修正)》第54条的规定,即“在国家出现紧急状态或者非常情况时,或者为了公共利益的目的,国务院专利行政部门可以给予实施发明专利或者实用新型专利的强制许可。”
“专利强制许可”是协商不成的最后手段。目前就Paxlovid的谈判卡在价格,而非不让用,仍有协商空间。需要注意的是,“专利强制许可”主要为满足国内市场,相关药品可在国内销售。若出口,专利受当地法律规制。
邵蓉:仿制药授权,应该更多是市场主体的市场行为,也就是辉瑞跟仿制者之间达成协议,药监局负责审批。一般来讲,行政部门不会主动出面去和辉瑞谈市场权益,如果那样的话,就说明是急迫状态了,启动强制许可的可能性反而更大。所以我认为提起仿制药授权并不是药监局的职责。
胡善联:接下来还是应该走自己的路。一方面,继续通过价格谈判、推动Paxlovid实现降价。这次它没有进入医保,主要还是价格较高。再次谈判后,价格会降到多少,能不能降到千元以下,存在难度。其次,药品定价需要考虑、平衡国际价格。
要重要的是,等到国产新冠药上市,通过头对头的非劣效试验临床效果如果和Paxlovid差不多,有利于推动Paxlovid降价。甚至,我们可以不需要引进这一药物。
另一方面,我们可以推动药物谈判。既然中国已经有5个药企在生产,我们是否可以协商取消中国仿制的专利费,或允许MPP协议生产的仿制药在中国销售。这个谈判不仅涉及医保,还涉及工信部、整个医药工业系统的参与。
最后要说的是,即使不进医保,民众仍可以通过市场自费购买使用这一药物。

