出品 | 虎嗅医疗组
作者 | 陈广晶
题图|视图中国
恒瑞医药的“出海”神话没能打动投资者。
延续昨天的跌停,4月26日恒瑞医药报收27.74元/股,总市值1770亿元,相比2021年底6100亿元的高点,已经跌到了脚踝。
上周五恒瑞医药突击发布了2021年年报和2022年一季报,从数据上看一个比一个惨。不过,昔日“研发一哥”已经打好了预防针,药剂还是“创新”“研发”——2021年该公司研发投入62亿元,创下新高;销售人员削减近4000人,增加研究人员约700人,在欧洲和日本都建立起了研发团队……
在此之前,恒瑞医药副总经理、全球研发总裁张连山还接受媒体采访,透露恒瑞医药的“长期主义”计划,官网更是直接亮出了“打造跨国制药集团”的野心。
然而实际上,从恒瑞医药的2021年年报看,过去一年里,备受青睐的创新药销售额下滑,反而是被“嫌弃”的集采药品有亮眼表现。
可以看到,该公司主打产品中,有三个品种的销量在逆势大涨,其中第二批集采中标的紫杉醇白蛋白,销售总量达到213.33万瓶,按照其中选价格780元/瓶计算,总销售额已经达到16亿元,相比2018年1400多万元,市场已经增长了100%以上。
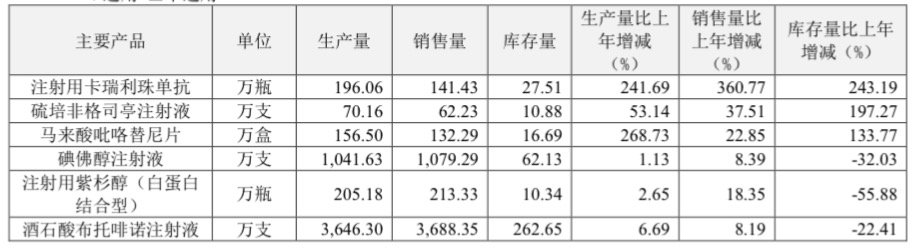
来自:恒瑞医药2021年年报
从中国制药企业之光,到一步步失去投资者信心,恒瑞医药让更多人体会到,什么叫没有“至暗”只有“更暗”。而在他们的远大抱负之下,潜在的支柱已经显现。
“续命”良药
创新药的“蓝图”虽然令人振奋,但是“烧钱”的项目,而集采中标药品换回来的,可是真金白银的现金流。在今天创新药融资遇冷的情况下,“现金为王”已成为共识,对于身处其中的药企,这些钱是足以续命的。
从恒瑞医药2021年年报看,仅第三批和第五批集采的14个药品就拿回了63亿元,加上紫杉醇白蛋白拿回的16亿元,集采仿制药支撑起了79亿元市场。这些钱也让恒瑞医药有底气一口气将研发投入加码到超62亿元,还布局海内外的研发管线。
其中,紫杉醇白蛋白又具有特殊性。该产品仿制难度更高,原研药占据了市场主导,恒瑞医药的产品在国内第三个上市,已经失去了市场先机。集采帮助这个产品,市场规模迅速蹿升。
根据恒瑞公开信息,2019年该产品全国销售量只有65.79万瓶,到2021年,已经突破了213万瓶,带来了16亿元以上的收入,且仍有增长趋势。
无论恒瑞医药承认与否,被“嫌弃”的集采为其提供着关键的给养,甚至可以说是“生命线”。
在恒瑞的创新药发展“蓝图”中,集采中标的紫杉醇白蛋白,也占据了一席之地,联合卡瑞利珠、法米替尼、吉西他滨、吡咯替尼/帕托珠单抗等治疗肿瘤方案,都在推进研究中。
这意味着,无论口头上怎么说,恒瑞已经越来越重视集采,也更重视集采产品联合采购、开发,都是不争的事实。特别是,与紫杉醇白蛋白这一类的首仿、难仿及改良型新药。在年报中,该公司也在强调,这类产品将成为仿制药市场未来的增长点。
实际上,国家药品集采低价背后,是企业产能、生产效率、成本控制,以及供应链把控等综合能力的比拼。行业人士认为,未来集采只有头部企业才能参与。
从龙头企业的经验看,集采以价换量,也确实是一个市场先机。没有上市的制药巨头,扬子江药业、齐鲁制药都在这一领域发力。
不得不说,虽然是靠仿制药起家,但是恒瑞医药对外形象一直是专注研发的传统药企。从这个意义上讲,“研发一哥”的名头也正在成为恒瑞医药的“偶像包袱”。这或许也是他们面对集采未能没能及时、果断作出反应的原因。
从观望到势在必得
在2021年的年报中,恒瑞医药不厌其详地描述了创新药版图,以及研发方面的巨大投入。
而针对集采仿制药,只提到了2018年集采以来,该公司一共28个品种名列其中,有18个品种中选。
谈及收入情况,也只是说2020年11月份开始执行的第三批集采,该公司有6个仿制药涉及,销售收入总共19亿元,同比下滑了55%;2021年9月份陆续进入执行阶段的第五批集采涉及的8个产品营收44亿元,同比下滑了37%。
这样的表述,也直指这些产品是导致营收、利润下滑的真凶。
事实上,这也在一定程度上,反映出了恒瑞医药对集采的态度。
从官方公布的资料来看,从第一批国家药品集中带量采购,也就是“4+7”试点扩围之时,恒瑞医药在是否跟进集采就十分犹豫。在首批集采中,他们只有厄贝沙坦和盐酸右美托咪定两个产品被纳入其中。
从结果看,厄贝沙坦以次高价中选,大品种盐酸右美托咪定直接丢标。后者是恒瑞医药销量最大的产品。2009年该药在国内率先上市后,销售额连年增长,到2018年占到了全国市场的81%,年贡献8亿元以上营收。
然而在扩围之时,这个大品种却没能及时通过一致性评价,连下场竞争的机会都没有。扬子江药业的产品中选价格133元/支,而当时,恒瑞医药这个品种,在地方采购价是最低已经可以压到123元/支。
这也意味着,恒瑞有实力,但是对集采仍然持观望态度。要知道,扬子江药业的盐酸右美托咪定早在2018年就已经通过了一致性评价。而恒瑞对如此重要的大品种,却并不积极推进一致性评价。
从第一批集采到第五批集采的报价情况看,恒瑞医药对集采的态度逐渐发生变化。虎嗅梳理发现,在前四批集采中,恒瑞医药的中标价格普遍在中间价位或最高价位,丢标的情况几乎在每一次集采中都会出现。
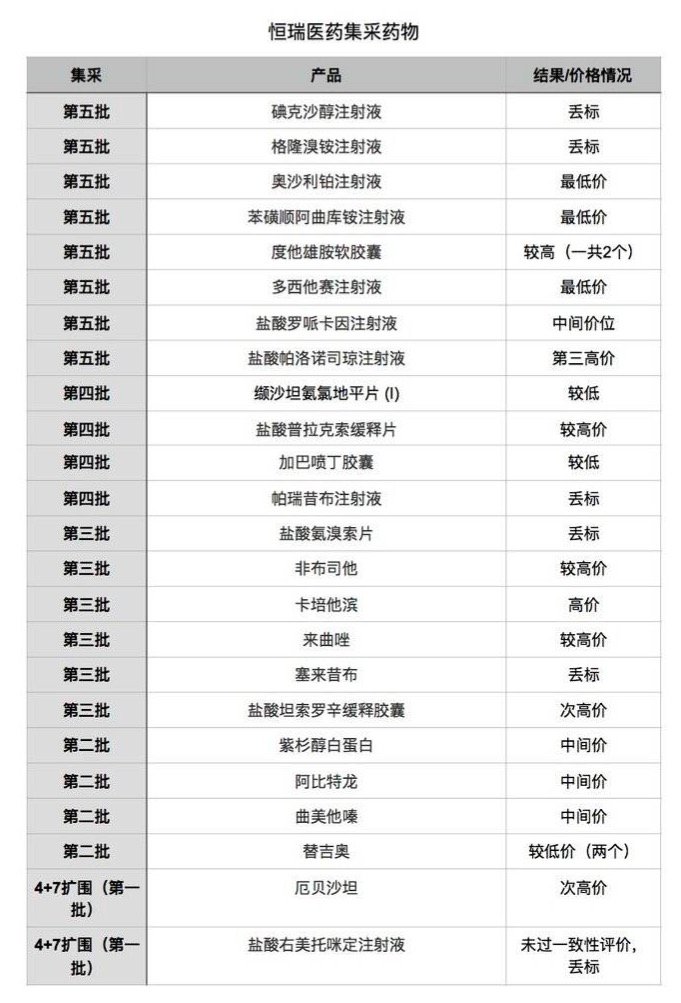
来自:恒瑞医药2021年年报
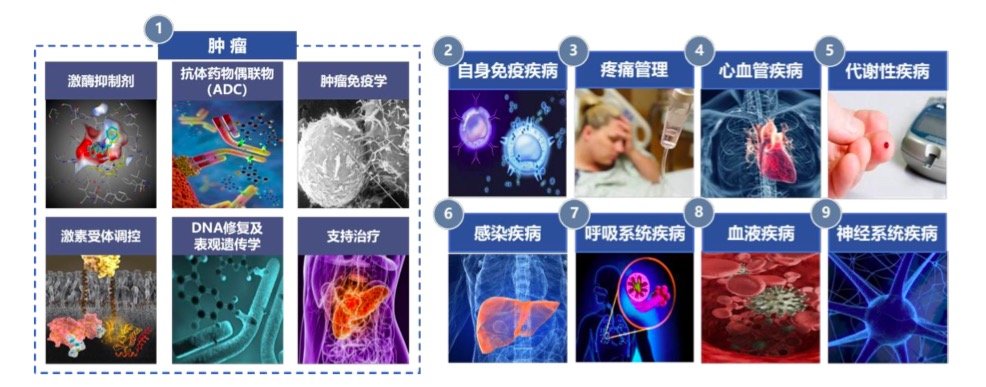
时下炙手可热的赛道,如激酶抑制剂、抗体药物偶联物(ADC )、肿瘤免疫、激素受体调控、DNA 修复及表观遗传、支持治疗等都有涉及。
可以看到,2018年恒瑞医药投入较大的品种除了PD-1等少数metoo类创新药,其余绝大部分还是仿制药。而到2021年,不仅已有10多个First-in-class、Best-in-class双/多特异性抗体在研,而且还建立了7个技术平台,覆盖ADC、AI-分子设计、基因治疗等。
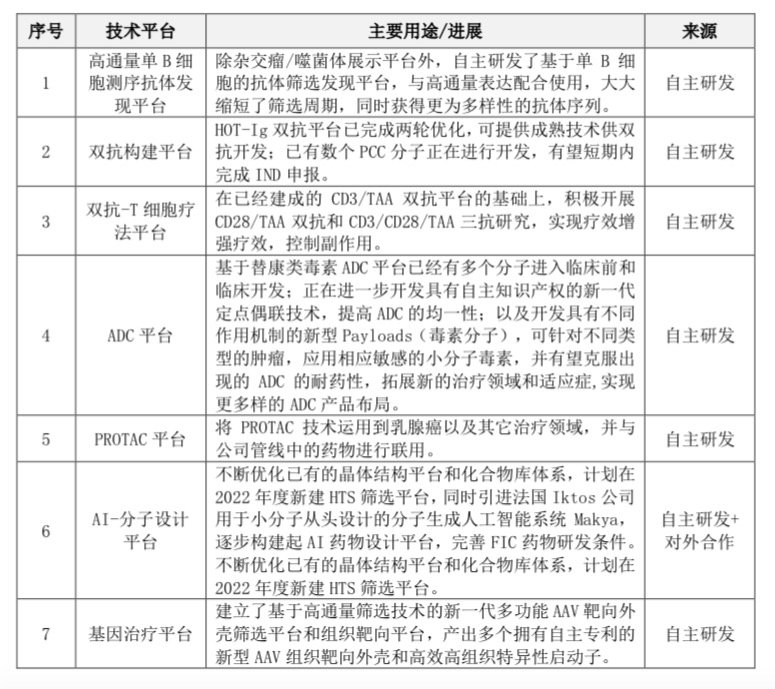
来自:恒瑞医药2021年年报
有行业协会负责人接受E药经理人采访时指出,恒瑞医药的这些平台已经基本囊括了新兴的技术,可能还有更多不知道的平台。“恒瑞如果想孤注一掷地去做一个东西,可能全中国也没人能做得过他”。
从2021年10月恒瑞医药研发日上,刚刚回归的董事长孙飘扬对创新和国际化的定义,他们已经做好“脱胎换骨”的准备。
除了探索全新靶点、充分发掘在研靶点在多种适应症的潜力,探索全新适应症,围绕具体疾病领域布局多种不同作用机理的产品,以及多种平台技术支持深度研究,甚至构建海外团队之外,他们也不排斥通过加强与生物医药公司的合作,license-in等方式,来完善产品结构。
原国家药监局首席科学家何如意也曾表示,就中国医药行业发展阶段来说,license in是快速补充管线的一种方式。恒瑞医药的管线中也有3个此类产品,都具有创新性和突破性。
不过,在巨大改变的同时,行业也注意到,恒瑞医药的研发管线中,不仅大多是跟随式的研究,选择的靶点比如HER2-ADC、CD20,也还是竞争者较多的领域。海外管线也有类似的问题。PD-L1/TGFβ等靶点已有海外巨头失利在前,能否突围成功还是存疑。
总体来说,行业人士认为其管线背后仍有路径依赖之嫌。
在30多年的发展中,恒瑞在小分子领域已经逐渐形成了“短期快速跟进”式的独特打法。
有行业人士告诉虎嗅,一般原研创新药刚进入二期临床,恒瑞的仿制项目就已经启动了。这一策略帮助恒瑞搭建起了一个由首仿品种、metoo类新药等组成的产品体系。以先发优势,快速占据了市场。
前述提到的盐酸右美托咪定,是恒瑞2009年在国内率先推出,最高年销售额超过7亿元。
2021年年报中提到的碘佛醇注射液、酒石酸布托啡诺,都是首仿药,销售额都超过亿元。根据年报公开数据测算,仅酒石酸布托啡诺在公立医院的销售额就在10亿元左右。
此外,盐酸左布比卡因、依托咪酯注射液、盐酸艾司氯胺酮、吸入用七氟烷、吸入地七氟烷和格隆溴铵,以及钆布醇注射液等,都是恒瑞医药的首仿产品。
2015年,药品审评审批制度改革之后,恒瑞医药也在尝试将这种方法移植到大分子、创新药研发领域。
虽然也成功推出了紫杉醇白蛋白、PD-1等重磅产品,但是先发优势已经不再明显。紫杉醇白蛋白在首仿之争中败给石药、PD-1上市时间更是远远晚于君实生物和信达生物。
客观事实是,2018年以来,中国医药市场环境发生了急剧的变化,更多融入国际市场的结果是,“拿来主义”已经不再适用。
从宏观上看,随着药品审评审批速度加快,进口原研药进入市场的速度更快,留给企业的窗口期更短。而且创新药研发的比拼已经进化到了药品开发能力、速度,以及靶点选择差异化的新时期,没有研发基础的本土药企要跟跨国药企、创新药同台竞技,胜算几何?
同时,中国已经不再缺医少药,反而还开始过剩,为了改善这一问题,而诞生的集采、医保谈判等新规,也都将市场引向对恒瑞等传统药企不利的方向。
此外,技术+人才,是恒瑞医药寻求突破的基础。从年报情况看,2021年恒瑞的研发团队规模已经增加到了5400多人,相比2018年的3000多人,几乎扩增了一倍。研究团队已经建到了美国、欧洲和日本等国。
尽管如此,核心研发人员的流失,还是给其后续研发走向增加了不确定性。特别是,在前不久,该公司的首席医学官邹建军离开并加入了君实生物。她2015年加入,实际上为恒瑞创新药研发打下了基础。
她在任期间,推动7款创新药、17个新适应症获批上市,包括硫培非格司亭、吡咯替尼、卡瑞利珠单抗、氟唑帕利、海曲泊帕乙醇胺、达尔西利、恒格列净。此外,还有3个产品——PD-L1、AR、DPP-4,在审评中,预计在2022年获批上市。
不利的环境、更具创新能力的竞争者,加上license-in环节的屡次失准,核心高管的离职,恒瑞的“老办法”还能不能奏效,是否可以推演到海外市场,都还是未知数。

