
图片来源:Pixabay
一些孩子不明原因去世的秘密,可能就藏在DNA里。
撰文 | 栗子
审校 | Clefable
有的孩子,不知道为什么就死了。
1997年夏天,劳拉·古尔德(Laura Gould)15个月大的女儿玛丽亚,在一天夜里发了烧。第二天早上,孩子的病情似乎已有所好转,会跟着电视手舞足蹈。中午玛丽亚睡着了,劳拉打算晚点带她去看医生。但是,孩子再也没有醒过来。
劳拉本人是一位物理治疗师(也称康复治疗师,针对患者的动作问题制定康复治疗方案,以改善身体功能),身为医务工作者,她觉得是自己忽略了女儿身上的什么症状,才错过了拯救孩子的机会。劳拉以为只要请教更专业的人,立刻就能知道自己错在哪里。
但当玛丽亚的遗体被送进法医办公室,尸检结果却显示不出她的死亡原因。在此之后,劳拉还求助过另外一些病理学家,他们也找不到任何解释。
劳拉无法接受没有答案的结局。她查过许多资料,也了解到婴儿猝死综合征(SIDS):指1岁以下看似健康的孩子突然死亡、且详细检查后仍然找不到死因的情况,案例大多发生在睡眠期间。这是婴儿死亡的主要来源之一,在1990年全球范围内共有大约22 000例。
不过,玛丽亚去世时已经1岁3个月。1岁以上的儿童不明原因猝死(SUDC)案例并不罕见,但远不像婴儿猝死综合征那样受关注。后来,劳拉和纽约大学的神经学家奥林·德文斯基(Orrin Devinsky)一起创建了“SUDC登记与研究合作组织”,想用更多的数据推动这个领域的研究,帮助人们了解那些儿童死亡案例背后的原因。
最近,来自纽约大学的研究团队,终于从基因当中找到了一丝线索。科学家们把成果发表在《美国科学院院刊》(PNAS),而劳拉是这篇研究的共同一作。
父母没有的基因,孩子却有
2014年,劳拉和德文斯基启用了SUDC登记表,开始收集1~18岁儿童不明原因猝死的病例,不仅采集儿童自身的生物样本,也采集他们父母的生物样本。
研究用到的样本,就来自这份登记表上的124名已故儿童,以及这些孩子在世的双亲。科学家分析了他们的DNA,希望从中找出可能致病的基因突变。通常来说,法医调查死亡原因时,不会分析死者的DNA,所以这样的“分子尸检”就有机会填补普通尸检的盲区。
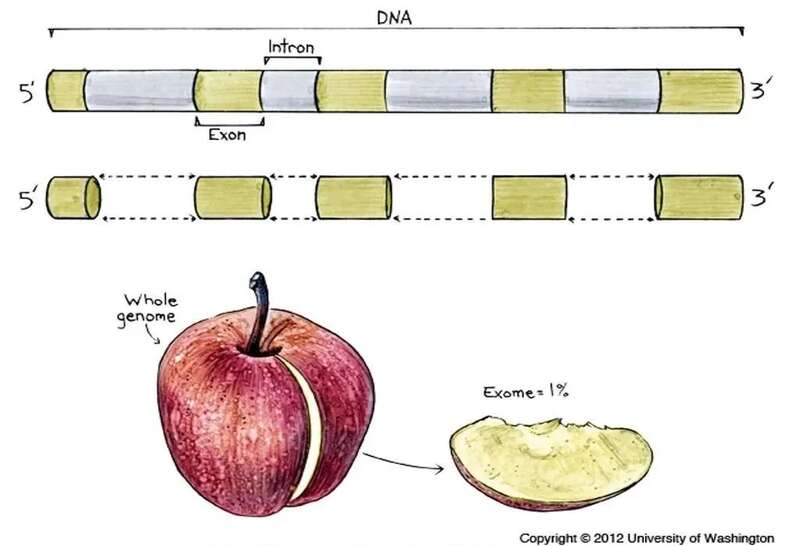
黄色是外显子,编码蛋白质,在全部DNA序列中只占1%;余下99%都是内含子,不表达蛋白质(图片来源:University of Washington)
DNA序列中有外显子和内含子,外显子负责编码蛋白质,内含子不编码蛋白质,只插在不同的外显子之间,把它们隔开。人体内各种重要的生理活动,都要靠蛋白质来完成,所以科学家更关心DNA中的外显子:如果有外显子发生突变,细胞制造出的蛋白质就有可能出现结构异常,一些原本正常的功能也会遭到破坏。
在外显子序列中,科学家着重观察了与心律失常、癫痫等疾病有关的137个基因。结果发现,在124位不明原因死亡的儿童当中,这些基因出现非同义突变的频率几乎是普通人的10倍,这个差距十分显著。
所谓非同义突变,是指DNA中的一个核苷酸改变,导致蛋白质中的一个氨基酸改变,这类情况大多有害,甚至致命;而如果一个核苷酸改变,对应的氨基酸没有改变,就是同义突变,不会影响蛋白质的结构和功能。
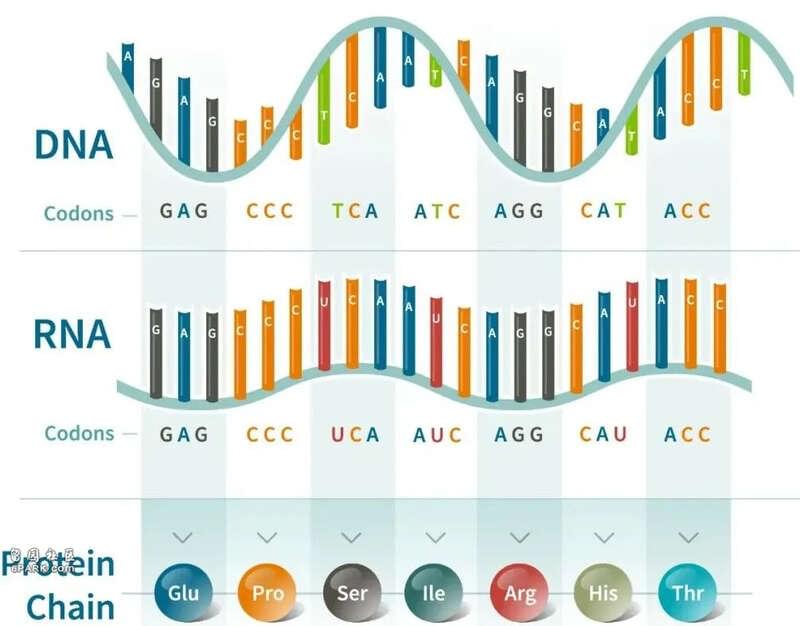
DNA里,核苷酸的碱基有ATCG四种,三个一组,排列方式共有4^3=64种;而人体里组成蛋白质的氨基酸只有20种,所以一些不同核苷酸的排列,会对应相同氨基酸,如图中GAG若变成GAA,对应的还是谷氨酸不变,但若变成GAT,对应的氨基酸会变成天冬氨酸(图片来源:Ancestry.com)
科学家认为,孩子们的死亡原因,很可能就藏在那些基因突变当中。那么,具体是些怎样的突变呢?
124人当中的11人,在一些与钙信号传导有关的基因出现了突变。钙信号在人体内的作用十分重大:钙离子进入神经元后,可以触发神经递质的释放,向另一个细胞传递信息;而钙离子进入心肌细胞后,可以让储存在“库房”的钙被释放到细胞质中,令细胞内钙离子浓度大增,从而使心肌收缩。
因此,一旦钙离子的工作流程受到影响,脑部和心脏的功能都可能出现损伤。比如,研究团队观察到RYR2基因突变,这是表达兰尼碱受体2的基因:兰尼碱受体2就像“库房的看守”,钙离子到了心肌细胞里,需要先激活这个受体,才能把库存的钙释放到细胞中,让心肌收缩。这个基因发生突变后,机体无法正常合成兰尼碱受体,儿童就可能出现心律失常,甚至心跳停止。
包含RYR2基因在内,科学家在孩子们身上找到了6个与钙信号传导相关的基因的突变,其中一些基因指向心脏疾病,另一些可能指向神经系统疾病(癫痫)。这些或许就是一部分儿童猝死的原因。
而当科学家对比了孩子与父母的DNA后发现,这些突变几乎都是新生突变(de novo mutations),就是父母DNA中没有的突变,却在孩子的DNA里出现了。发生这样的情况,可能是精子或卵细胞形成之前,在减数分裂的过程中,DNA复制错误,导致生殖细胞变异;也可能在胚胎发育的早期,受精卵本身出现了变异。
研究者说,既然突变是随机的,一对父母两次生育时,几乎不可能发生同样的致命突变。所以,假如SUDC发生在一个孩子身上,而父母想生第二孩子,这项研究也会为他们带来一些希望。
不只是个安慰
研究团队成员之一、纽约大学的神经学家钱永佑教授说:“我们这项研究是迄今为止同类研究当中规模最大的,并且首次证明了儿童不明原因猝死(SUDC)存在明确的遗传因素,填补了这个领域的一些空白。”
不过,在11人身上发现的规律,只能代表124人当中的9%。如果想找到更多儿童猝死的主要原因,还需要进一步的探索。而在这项研究发表后不久,波士顿儿童医院的科学家领衔的团队,也汇报了他们的新成果。
这项研究涉及32例儿童不明原因猝死(1岁以上)和320例婴儿猝死综合症(1岁以下),科学家们从中观察了294个与神经疾病、心脏疾病以及全身系统性疾病有关的基因。
在这个数据库里,共有73个案例同时包含孩子和父母的数据。研究团队在其中37个孩子身上,锁定了可能致命的突变:13个突变发生在与神经系统疾病相关的基因上,18个突变发生在与心脏问题有关的基因上,还有6个突变与系统性疾病有关。
而这些携带危险基因的孩子当中,有6位在1岁以上,也就是不明原因儿童死亡(SUDC)的案例,或许可以作为第一项研究的补充。
当然,两份研究成果加在一起,依然只能描绘出一小部分儿童猝死的原因,离画出整片图景还差得很远。但这无论如何都是一个好的开始。

劳拉等人的研究中,也用到了这些孩子的数据(图片来源:NYU Langone Health)
对那些失去孩子的父母来说,知道原因和不知道原因是完全不同的。在劳拉和同事们的努力下,小女孩克洛伊的家人终于了解,基因突变会影响她的心脏维持正常节律的能力。在得到这个答案之前,他们已经等了3年。
而如今的劳拉,不仅是玛丽亚的母亲,也是纽约大学格罗斯曼医学院的一位研究人员了。对像她一样的科学家来说,找到儿童不明原因猝死的原因,是通往治疗方案的第一步。如果能够提早发现基因当中的危险因素,就有机会对儿童潜在的健康问题进行及时的干预。
科学家们希望有一天,那些可能导致儿童猝死的基因,可以加入新生儿筛查列表。但在那之前,还有很长的路要走。毕竟,仅凭现在的研究成果,并不足以确切地说出,哪些基因突变一定会产生哪些后果。如果武断地判定一个儿童“有心律失常的风险”并加以干预,反而可能制造出更多的问题。

