注:国家医疗保障局网站1月8日消息,2022年国家医保药品目录谈判工作于2023年1月8日正式结束。其中,阿兹夫定片、清肺排毒颗粒谈判成功,Paxlovid因生产企业辉瑞投资有限公司报价高未能成功。
本文来自微信公众号:果壳硬科技(ID:guokr233),文章首发时间:2022年4月24日,作者:李拓、杨景诒,头图来自:视觉中国
谁能想到,一团尘封17年的小分子,能在科学家手中脱胎换骨,成为帕克洛韦德(Paxlovid,或名帕罗韦德),并有望给研发药企带来220亿美元的年收入。[1]
在本文中,果壳硬科技团队带你认识这款全球第一个获FDA批准的新冠口服药[2],尝试回答这些问题:帕克洛韦德是如何研发出来的?制造起来难吗?能结束疫情吗?还有哪些同类新冠口服药值得期待?
帕克洛韦德的故事可能相当久远,让我们先从猫聊起。
治猫病的“路线问题”
猫传染性腹膜炎(猫传腹),由一种冠状病毒FIPV(feline infectious peritonitis virus)引发,一度是猫的不治之症。本世纪初,人们开始研究使用一种代号GC376的药物来治疗该病。
GC376是一种3CL蛋白酶抑制剂,其作用原理是:通过抑制冠状病毒3CL蛋白酶(3C-like protease),从而抑制病毒蛋白的形成,最终使病毒合成和复制失败。
2018年,动保公司Anivive从堪萨斯州立大学动物学院的两名研究者张京玉(장경옥/Kyeong-Ok Chang)、金允贞(김윤정/Yunjeong Kim)手中买下专利,进行全球商业化开发。[3]
不过,这款GC376的商业化之路并不平坦。2015年的一项试验结果就表明,在注射了GC376之后,参与试验的20只猫仅有7只活了下来[4];2020年一项研究表明,GC376还需要与阿莫地喹合用[5]。这意味着,GC376对猫的实际效果一般。
于是,GC376很快让位于GS441524(俗称GS441)。
GS441是一种核酸类似物,其代谢产物可以竞争性地令病毒RNA复制出错,进而终止病毒复制,治疗猫传腹的效果更好。[6][7]
虽然GS441的发明者吉利德在2018年3月为该药申请了治疗猫传腹的专利(2020年6月公告,专利号US 20180296584 A1)[8],但认为该药更适合治疗埃博拉病毒和人类冠状病毒感染,因此也为该药申请了治疗丝状病毒感染(专利号US 20180311263 A1)[9]和冠状病毒感染的专利(专利号US 20170071964 A1)[10]。但吉利德至今没有将GS441作为兽药生产和销售,导致这款猫传腹“神药”,至今还是成为养猫人“黑市”抢手货。[11]
爱猫心切的人类治疗猫传腹的两种药,也代表了对抗冠状病毒的两条技术路线:一个是3CL蛋白抑制剂(GC376),另一个是核酸抑制剂(GS441)。新冠疫情爆发后,人们也从这两条技术路线中获取灵感。
沿着核酸抑制剂的路线,人们找到了GS441的药物前体GS5734,一种同样对猫传腹效果明显的药物分子,2020年,它被称为“瑞德西韦”(Remdesivir),广为人知;默沙东的莫努匹拉韦(Molnupiravir,或名莫匹拉韦)也是一种核酸抑制剂。只不过实践证明,瑞德西韦和莫努匹拉韦的抗新冠效果都不甚出色。
沿着GC376代表的3CL抑制剂的路线,辉瑞最终发现了帕克洛韦德(Paxlovid)组合疗法。
2022年4月22日,世界卫生组织更新新冠肺炎治疗指南,强烈推荐住院风险最高的轻中度新冠患者使用帕克洛韦德,同时更新指南,建议住院风险高的轻中度新冠患者使用瑞德西韦。[43]
帕克洛韦德略胜一筹。
一款明星新冠药的诞生
帕克洛韦德的研发并非从零开始,而是辉瑞研究人员翻检故纸堆的结果。
2002年底,“非典”(SARS)爆发,各大药企也针对SARS冠状病毒研发特效药,其中就有辉瑞。后者在2003年研发出一款候选药物,代号PF-00835231,但当研究人员准备进行临床试验时,SARS疫情得到了控制,开发计划也就此搁置。
17年后,新冠疫情爆发。2020年3月,辉瑞在与拜恩泰科开展mRNA新冠疫苗研发的同时,也启动了口服药的研发工作。研究人员发现,PF-00835231与“非典”病原SARS-CoV的结合位点,同样存在于新冠病原SARS-CoV-2,这意味着PF-00835231也许对新冠病毒同样有效(测试证明,确实如此),但静脉注射剂型太过繁琐,辉瑞决定将之改造成口服剂型。
PF-00835231富含氢键,口服后无法被肠胃吸收。因此难点就是:在不改变药物抗病毒特性的前提下消除氢键,并保证药物活性。辉瑞团队大胆且巧妙地使用了三氟乙酰胺,提高了药物生物利用率。
到2020年7月22日,适合口服的新候选药物诞生了,2020年9月1日,实验大鼠的药代动力学研究结果揭晓,才确定了这个代号PF-07321332的候选药物是辉瑞口服药的最终研究成果。[12]
PF-07321332被命名为奈玛特韦(Nirmatrelvir)。
2021年11月2日,辉瑞研究团队在《科学》杂志(Science)在线发表了辉瑞口服药PF-07321332的完整研究论文[13];两周后的11月16日,辉瑞将奈玛特韦(Nirmatrelvir)与利托那韦(Ritonavir)合为帕克洛韦德(Paxlovid),向FDA申请紧急使用授权。
2021年12月22日,帕克洛韦德成为首款获得FDA紧急批准的新冠口服药。
在获批前的11月18日,美国政府以52.9亿美元的价格向辉瑞订购了1000万疗程 [14];2022年1月4日,又向辉瑞追加1000万疗程订单。[15]
先来算一笔账:一盒帕克洛韦德为一疗程,为五天的口服量,包含五板药(每板供一天两次服用),每次150mg的两粒奈玛特韦和一粒100mg的利托那韦。也就是说,每一个疗程需服用1.5g奈玛特韦,1g利托那韦。因此美国政府2000万疗程的订单,共需30吨奈玛特韦。这只是成品规模,还不算全部步骤的原料。
一山放过一山拦,接下来,辉瑞要解决的问题是:如何大规模生产帕克洛韦德。
“金手指”在中国
30吨药多吗?
2020年7月,美国政府首次向辉瑞下单购买mRNA新冠疫苗,规模多达1亿剂[16]。相比之下,2000万疗程的口服药并不算很多。但从辉瑞的表态来看,这显然不容易。
拿到第二笔订单之后,辉瑞表示,即使加速,首批1000万的订单也要在2022年6月才能交付,第二批1000万疗程交付时间则为9月[15]。在2022年摩根大通医药年会(JPM)期间,辉瑞CEO阿尔伯特·伯拉(Albert Bourla)披露了更详细的产能和交付进度:2022年第一季度可制造600万~700万疗程,到二季度末,帕克洛韦德的总产量将达到3000万疗程,年底达到1.2亿疗程。[17]
宇宙药厂辉瑞遇到了什么问题?
帕克洛韦德包含两种成分:奈玛特韦和利托那韦。其组合原理是:虽然奈玛特韦可抑制新冠病毒蛋白的合成,但该药会被肝脏中一种名为CYP3A4的酶快速降解。这时就需要用利托那韦抑制CYP3A4的活性,进而将奈玛特韦的血药浓度维持在一定水平[18],以保证一日两次的治疗效果。
果壳硬科技团队发现,从专利分布和当前市场行情来看,利托那韦并不难造。
利托那韦最早由雅培(Abbott)的子公司雅培生命研发,1996年,FDA批准利托那韦注射液和胶囊用于治疗HIV感染[19],2013年,雅培生命拆分独立成新公司艾伯维(Abbvie),后者继承了利托那韦的专利,生产利托那韦片“艾治威”。
新冠大流行初期,洛匹那韦-利托那韦(即抗HIV组合药物“克力芝”)曾用于新冠治疗试验[20],但效果有争议。到2020年10月,牛津大学、英国国家卫生研究所等机构在《柳叶刀》发布的论文称,通过随机对照、开放标签的平行的试验表明,克力芝对新冠患者并无特效。[21]
利托那韦的专利已于2017年专利已到期[22],国内外有不少公司做出了相关仿制药。中国国家药监局官网显示,有三家国内药企分别生产利托那韦原料药(上海迪赛诺)、口服液(厦门万全万特)和片剂(江苏宣泰)。
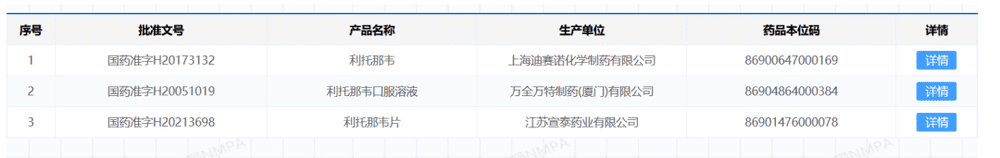
公告信息显示,仅歌礼制药一家通过江苏宣泰生产利托那韦,年产能就能达到5.3亿片[23],如果加上全球其它国家的仿制量,利托那韦的供应并不成问题。
不过,对全球药企来说,制造奈玛特韦是个全新的课题。
美联社报道援引辉瑞官方专家称,生产帕克洛韦德(主要是奈玛特韦)像搭积木,关键原料都在不同地区,制造商涉及超10个国家的20多个地点,其生产周期已从最初的9个月缩短至7个月。[24]
但奈玛特韦遇到的困难并不只是生产步骤之繁琐,还有供应链问题。《科学》专栏作者德克·劳(Derek Lowe)指出,这个生产链条可能会有不少问题:
不少生产步骤涉及Boc基团,即二碳酸二叔丁酯(DIBOC),但DIBOC的产能并没有那么多,因为它的上一级原料是叔丁醇钠,后者需要用叔丁醇和金属钠合成。[25]
这就是包括美国在内的绝大多数国家遇到的上游供应链瓶颈:没有足够多的金属钠。
生产金属钠需要大规模电解冶金产业。2020年,全球金属钠产能装置约16.05万吨。其中,中国装置产能为13.25万吨。仅中盐化工一家的金属钠产能就达到6.5万吨,占全球产能的40.5%。[26]
“基本上,如果你回溯任何一种药物的生产,直到最早的阶段,你几乎总是会找到一大堆离岸供应商。他们大多是中国人,不过也有一些印度人和其它国家。”德克·劳在其专栏文章中指出,“在美国不再具备这样的能力,因为让别人做这事儿要便宜得多。”[25]
因此,如果必须按辉瑞的公布的工艺路线图制造奈玛特韦,那么中国必然成为奈玛特韦上游原料的核心生产地。
那么,中国的原料和成品供应情况如何?
“神药”难造
辉瑞在《科学》杂志发布的论文显示,他们在实验室合成150g奈玛特韦,下图是他们给出的方法,至少需要8步——
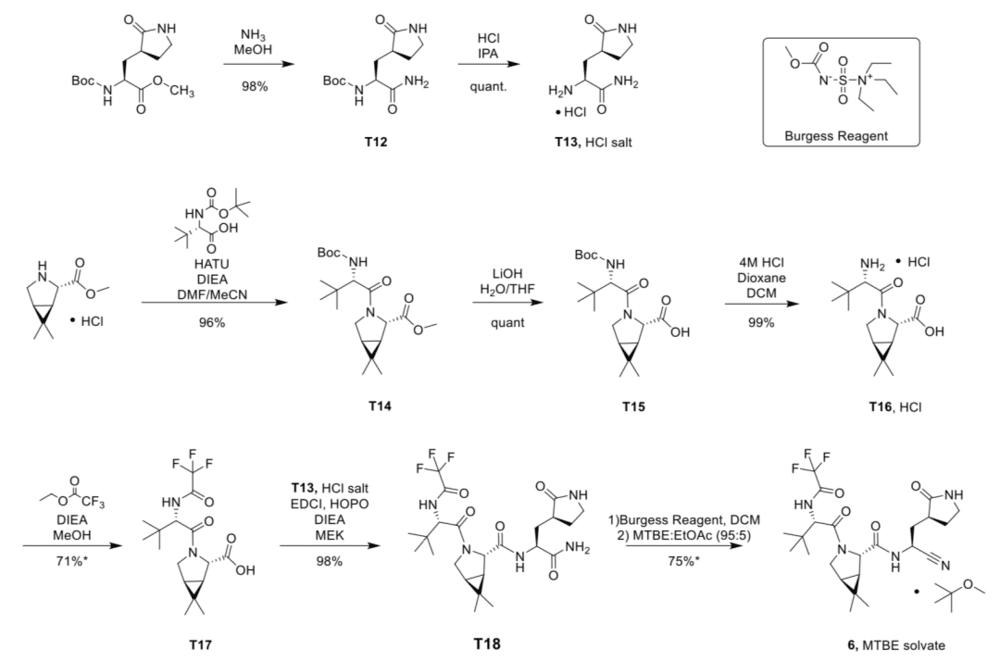
图源丨《科学》[5]
根据上图步骤,关键原料包括以下几种:
![按辉瑞2022年1.2亿疗程的需求,推算奈玛特韦(PF-07321332)关键原材料及供需情况,制表丨果壳硬科技团队,资料来源丨国泰君安证券<sup>[27]</sup><br>](https://i.aiapi.me/h/2023/01/08/Jan_08_2023_07_42_27_3995368273253997.png)
可以发现,若按辉瑞2022年1.2亿疗程的计划产能,仅中国的原料供应量就能满足六成以上的需求。少量供应缺口集中在关键原料SM1、SM2,以下分别讨论。
先来看SM1。民生证券研报指出,制造克级SM1的总收率为86%,高于制造公斤级的66%,但产业化难度更高,因此生产实践中仍需采用公斤级制造工艺。后者需要-120℃的工业级生产的低温和溴乙腈原料,因此生产难点在于超低温生产条件和氰化物原料的资质壁垒。[28]
不过,一位要求匿名的化工行业人士告诉果壳硬科技团队,在化工园区内,大型药企与本地政府通常关系良好。“对于新冠特效药这样的项目,本地更是会一路绿灯,环评、安评都不会有大问题。”因此如果需要,经济利益应能驱使国内供应商,完全补足现有缺口,进而满足T13产量。
再来看SM2。SM2的生产难度小于SM1,虽然目前直接供应量不足,但按奈玛特韦的今年总需求量,倒推SM2中间体卡隆酸酐的需求量约为454吨/年,该原料目前的供应量270吨/年,拟建产能则超过1000吨[27]。也就是说,SM2基本也不存在供应难题,只看在建生产线何时量产。
当然,以上反应产率、供应链需求量,只是相关研究机构按辉瑞官方文件做出的测算,这些都是理想状况,实际生产工艺可能大有不同。
某高校化工专业研究人员告诉果壳硬科技团队,目前国内舆论都基于辉瑞2021年11月发表的论文,来推测和拼凑奈玛特韦的供应链,而实际生产过程可能和辉瑞给出的流程有所差异,且并不排除辉瑞或已开发出更优工艺的可能性。
“科研论文给出的产率不可尽信。”前述匿名行业人士也指出,专利申请方真正使用的原料,可能隐藏在“包括但不限于××”之类语焉不详的描述句式中,因此完全按照化工产业的专利说明书仿制产品,效果并不够好。
“一般情况下,想要生产的产品,不会在专利、论文中给出实际的生产工艺。论文中的核磁、质谱等验证数据是真实的,但是合成过程中的关键技巧(比如分段升温、加料顺序等)可能会被隐瞒,对于不以合成过程为重点的文献尤为如此。”文献通常会给出一种可以实现合成路线的条件,研发人员通过优化,一般都能达到更高的产率。
“在做药化时的工艺路线,和最终在工厂里生产的工艺路线,可能千差万别。”前述高校化工专业研究人员表示,化学药物从研发到生产,工艺会“滚动优化”,他告诉果壳硬科技团队,“最终目标是尽可能以便宜的价格,尽可能高的产率,尽可能短的步骤,实现大量可重复的合成。”
目前,国内不少公司已经在尝试优化奈玛特韦中间体的生产流程,国家知识产权局官网显示,多家中国公司的奈玛特韦优化工艺专利,都在申请公示期。
总之,无需怀疑中国生产奈玛特韦的实力,但非化工行业金融从业者通过公开资料讨论供应链,也只能点到为止,指导投资更应慎之又慎。
但是,中国供应充足原料,就能顺利生产,及时供应吗?
骨感的3CL
3CL蛋白酶抑制剂的故事始于猫咪,声名大噪于奈玛特韦。与辉瑞同步,或受市场前景激励而投入研发的药企,让3CL赛道格外拥挤。
这里是果壳硬科技团队不完全统计的3CL新冠药的在研信息——
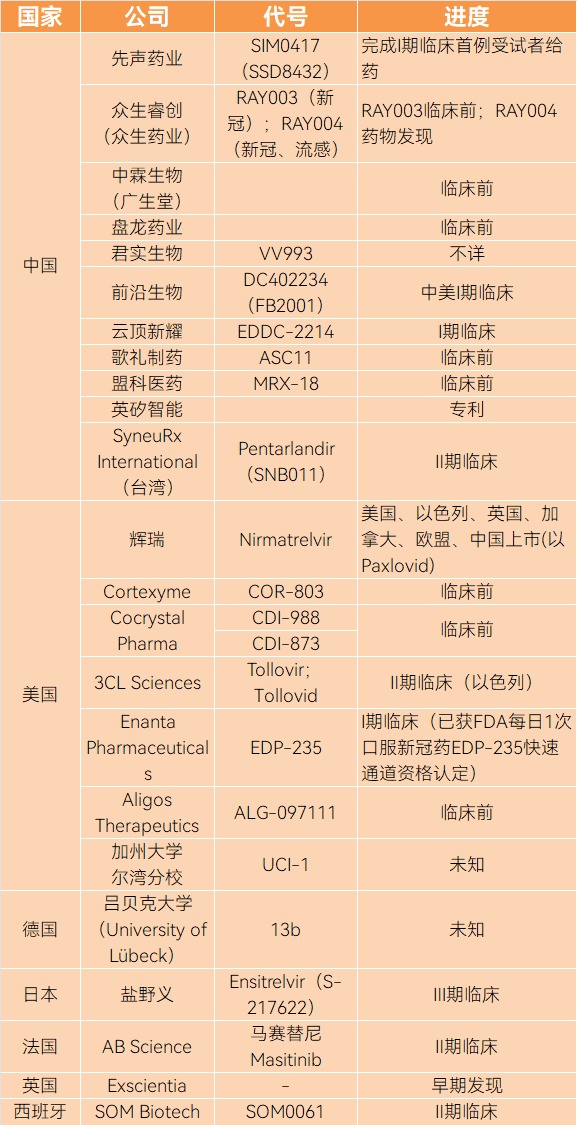
通观这些在研3CL新冠药,中美英等国的不少项目,都处于早期临床甚至未进入临床阶段。
实际上,辉瑞还曾同步研发另一款3CL蛋白抑制剂Lufotrelvir(奈玛特韦的磷酸前药,代号PF-07304814),不过辉瑞年报显示,该研究已在2022年2月终止。
其它如君实则为核酸抑制剂和3CL抑制剂(VV993)双路线推进(但截至4月20日,我们在CDE临床试验登记与信息平台及美国clinicaltrials均未查到VV993的相关信息);歌礼则企图复制辉瑞的成功路径,将在研ASC11与已大量仿制生产的利托那韦结合(我们同样未查询到该药的临床试验登记信息);盐野义的S-217622则无需利托那韦辅助,直接口服单药,由于Ⅱ/Ⅲ期临床数据不错(尽管可能存在致畸性),一旦获批,则将购买100万疗程的药物。[29]
这些在研的3CL新冠药物,市场前景如何?辉瑞过去一个季度的表现告诉我们,业绩不一定是敲敲计算器就算数的。
表面上,辉瑞可能从不会担心帕克洛韦德的销量,因为需求就摆在那。
由于能将高危患者住院率降低89%和死亡率降低88%[30],第一季度,全球各地都对帕克洛韦德翘首以待。而自获批至今,辉瑞已在中国寻找代工厂下单,还与MPP签协议授权中低收入国家的36家药企进行仿制[31],但仿制药面向的中低收入国家市场,不包括中国。
杜克大学全球健康创新中心数据显示,全球多个国家向辉瑞订购帕克洛韦德,其中美国政府订购了2000万疗程,其次是英国275万疗程,最低的比利时只有1万疗程。[32]
美国官方平台HealthData数据显示,截至2022年4月22日,全美有19207个药店可提供帕克洛韦德总量为632825疗程[33];韩国虽然订购了76.2万疗程,但2022年1~3月内有超970万人感染新冠,同期服用该药的仅有113783人[34];非洲的临床研究机构在向辉瑞索要试验药品时,直接吃了闭门羹。[35]
看起来辉瑞新冠口服药供不应求,然而,订购多少是一回事儿,到手多少是另一回事儿。实际情况是——好运并不常伴辉瑞。
2022年第一季度刚过完,产业分析师就对辉瑞新冠口服药帕克洛韦德的销售情况相当悲观:在一季度的美国市场,该药销售额或为6.2亿美元,还不及辉瑞此前19亿美元预估额的三分之一。[36]
为何会有如此之大的落差?
第一,太贵了。
再生元鸡尾酒抗体疗法REGEN-COV定价2100美元/剂,默沙东的口服药莫努匹拉韦(Molnupiravir)定价700美元/疗程,与这些昂贵的新冠药前辈们相比,辉瑞帕克洛韦德定价529美元/疗程(按美国政府第一批采购价),算是较“便宜”了[37],但依然是普通人难以承受的价格,政府采购前也得掂量一下。药品专利池(MPP)执行董事查尔斯·戈尔(Charles Gore)估计,帕克洛韦德的成本也不过20~25美元/疗程,未来可能下降至10美元/疗程。[38]
只要辉瑞还坚持高价,帕克洛韦德的销售数据就不会太好看。
第二,服药要求有些特别。
在说明书中,辉瑞建议患者在确诊后出现症状的五天内服用帕克洛韦德[39],但NPR援引卫生专家指出,由于医生在开处方前,要考虑患者常用药是否与帕克洛韦德相互作用(例如,利托那韦会导致肝脏损伤[40]),这导致一些患者无法按要求及时服药。
即便患者符合服药标准,也可能因为预约不到医生拿不到处方,或者拿到处方而附近药店又没货,导致“用时没有,不用时闲置”的窘况。[41]
第三,产能实在上不去。
辉瑞在2021年6月即开始筹备产能,并在2021年9月生产出第一批帕克洛韦德[24]。杜克大学全球健康创新中心数据显示,到2022年4月初,帕克洛韦德的总订单量为28822000疗程。[32]
![图源丨杜克大学全球健康创新中心 COVID-19 Therapeutics <sup>[32]</sup><br>](https://i.aiapi.me/h/2023/01/08/Jan_08_2023_07_42_37_3995378117337569.png)
虽然辉瑞已向多家中国CDMO公司派单,而MPP也授权36家公司进行仿制[31],但2022年上半年,帕克洛韦德将主要销往富国(而且远不够卖),至于仿制药,根据“无国界医生”组织的估计,可能要到2023年才能面市。[42]
从产能爬坡,到价格,再到全球分配,帕克洛韦德又将重复疫苗的故事:科技只能眼睁睁看着全世界因经济实力、医疗资源和认知水平的巨大差异,陷入又一轮不平等,无力改变。
终点未至
对深陷疫情泥潭的人类来说,帕克洛韦德带来了希望。但辉瑞新冠口服药的出现不是终点,我们依然需要通过切断传染途径(讲究卫生、社交隔离)、保护易感人群(打疫苗)、管理传染源(及时收治)的“传染病预防三环节”,备足弹药,综合抗疫。
唯有团结起来,回归常识,人类才能迎来真正的曙光。
References:
[1] 辉瑞2021年第四季度及全年财报https://s28.q4cdn.com/781576035/files/doc_financials/2021/q4/Q4-2021-PFE-Earnings-Release.pdf
[2] FDA:FDA Authorizes First Oral Antiviral for Treatment of COVID-19 https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-authorizes-first-oral-antiviral-treatment-covid-19
[3] Veterinary researchers and Anivive license antiviral drug for fatal cat disease 2018-9-20 https://www.k-state.edu/media/newsreleases/2018-09/fipantiviral92018.html
[4] Kim, Yunjeong; Shivanna, Vinay; Narayanan, Sanjeev; Prior, Allan M.; Weerasekara, Sahani; Hua, Duy H.; Kankanamalage, Anushka C. Galasiti; Groutas, William C.; Chang, Kyeong-Ok; Perlman, S. (2015). Broad-Spectrum Inhibitors against 3C-Like Proteases of Feline Coronaviruses and Feline Caliciviruses. Journal of Virology, 89(9), 4942–4950. doi:10.1128/jvi.03688-14
[5] A rational approach to identifying effective combined anticoronaviral therapies against feline coronavirus. S.E. Cook, H. Vogel, D. Castillo, M. Olsen, N. Pedersen, B. G. Murphy. bioRxiv 2020.07.09.195016; doi: https://doi.org/10.1101/2020.07.09.195016
[6] B.G. Murphy, M. Perron, E. Murakami, K. Bauer, Y. Park, C. Eckstrand, M. Liepnieks, N.C. Pedersen,The nucleoside analog GS-441524 strongly inhibits feline infectious peritonitis (FIP) virus in tissue culture and experimental cat infection studies,Veterinary Microbiology, Volume 219,2018,Pages 226-233, https://doi.org/10.1016/j.vetmic.2018.04.026.
[7] Pedersen NC, Perron M, Bannasch M, et al. Efficacy and safety of the nucleoside analog GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis. Journal of Feline Medicine and Surgery. 2019;21(4):271-281. doi:10.1177/1098612X19825701
[8]美国专利局文件:https://pdfaiw.uspto.gov/.aiw?PageNum=0&docid=20180296584&IDKey=B6678C4565B8&HomeUrl=http%3A%2F%2Fappft.uspto.gov%2Fnetacgi%2Fnph-Parser%3FSect1%3DPTO2%2526Sect2%3DHITOFF%2526p%3D1%2526u%3D%25252Fnetahtml%25252FPTO%25252Fsearch-bool.html%2526r%3D1%2526f%3DG%2526l%3D50%2526co1%3DAND%2526d%3DPG01%2526s1%3D%252522US%252B20180296584%252BA1%252522%2526OS%3D%252522US%252B20180296584%252BA1%252522%2526RS%3D%252522US%252B20180296584%252BA1%252522
[9]美国专利局文件:https://patft.uspto.gov/netacgi/nph-Parser?Sect1=PTO2&Sect2=HITOFF&p=1&u=%2Fnetahtml%2FPTO%2Fsearch-bool.html&r=20&f=G&l=50&co1=AND&d=PTXT&s1=GS-441524&OS=GS-441524&RS=GS-441524
[10]美国专利局文件:https://patft.uspto.gov/netacgi/nph-Parser?Sect1=PTO2&Sect2=HITOFF&p=1&u=%2Fnetahtml%2FPTO%2Fsearch-bool.html&r=19&f=G&l=50&co1=AND&d=PTXT&s1=GS-441524&OS=GS-441524&RS=GS-441524
[11] Sarah Zhang:A Much-Hyped COVID-19 Drug Is Almost Identical to a Black-Market Cat Cure,2020-5-8 https://www.theatlantic.com/science/archive/2020/05/remdesivir-cats/611341/
[12] Bethany Halford:How Pfizer scientists transformed an old drug lead into a COVID-19 antiviral. 2022-1-14 https://cen.acs.org/pharmaceuticals/drug-discovery/How-Pfizer-scientists-transformed-an-old-drug-lead-into-a-COVID-19-antiviral/100/i3
[13] An oral SARS-CoV-2 Mpro inhibitor clinical candidate for the treatment of COVID-19 https://www.science.org/doi/10.1126/science.abl4784
[14] Pfizer to Provide U.S. Government with 10 Million Treatment Courses of Investigational Oral Antiviral Candidate to Help Combat COVID-19 https://www.pfizer.com/news/press-release/press-release-detail/pfizer-provide-us-government-10-million-treatment-courses
[15] Pfizer to Provide U.S. Government with an Additional 10 Million Treatment Courses of its Oral Therapy to Help Combat COVID-19 https://www.pfizer.com/news/press-release/press-release-detail/pfizer-provide-us-government-additional-10-million
[16] Pfizer and BioNTech Announce an Agreement with U.S. Government for up to 600 Million Doses of mRNA-based Vaccine Candidate Against SARS-CoV-2 https://www.pfizer.com/news/press-release/press-release-detail/pfizer-and-biontech-announce-agreement-us-government-600
[17] JPM 2022: Pfizer CEO eyes 50% boost to Paxlovid production—and capacity expansions, too https://www.fiercepharma.com/pharma/jpm-2022-pfizer-bumps-paxlovid-production-estimate-to-120-million-for-year-while-also
[18] NIH:Ritonavir-Boosted Nirmatrelvir (Paxlovid) 2022-2-24
[19] FDA给雅培公司的批文:https://www.accessdata.fda.gov/drugsatfda_docs/nda/97/020659Orig1s000rev.pdf
[20] Arabi, Y.M., Asiri, A.Y., Assiri, A.M. et al. Treatment of Middle East respiratory syndrome with a combination of lopinavir/ritonavir and interferon-β1b (MIRACLE trial): statistical analysis plan for a recursive two-stage group sequential randomized controlled trial. Trials 21, 8 (2020). https://doi.org/10.1186/s13063-019-3846-x
[21] RECOVERY Collaborative Group. Lopinavir–ritonavir in patients admitted to hospital with COVID-19 (RECOVERY): a randomised, controlled, open-label, platform trial. The Lancet, doi:10.1016/S0140-6736(20)32013-4
[22] 国家知识产权局知识产权发展研究中心:洛匹那韦/利托那韦原研药企艾伯维公司抗病毒药物专利布局分析 2020.2.26 http://www.cnipa-ipdrc.org.cn/article.aspx?id=565
[23] 歌礼公告:歌礼宣布利托那韦口服片年产能进一步扩大至5.3亿片 https://www1.hkexnews.hk/listedco/listconews/sehk/2022/0313/2022031300012_c.pdf
[24] Tom Murphy:EXPLAINER: Why Pfizer needs time to make COVID-19 treatment 2022-3-2 https://apnews.com/article/coronavirus-pandemic-science-business-health-medication-2f84fdd8eab845606d05f7f9d1fe3e0b
[25] Derek Lowe:Making Paxlovid https://www.science.org/content/blog-post/making-paxlovid
[26]中盐化工2020年年报 http://static.sse.com.cn/disclosure/listedinfo/announcement/c/new/2021-04-22/600328_20210422_7.pdf
[27] 国泰君安证券2022春季策略研讨会:聚焦刚需下的比较优势
[28] 民生证券:MPP 新冠仿制药授权开启,上游有望加速放量
[29] 共同社:盐野义新冠口服药或致畸 不建议孕妇服用 2022-4-13 https://china.kyodonews.net/news/2022/04/3e1f27d5fb9a--.html
[30] Pfizer Announces Additional Phase 2/3 Study Results Confirming Robust Efficacy of Novel COVID-19 Oral Antiviral Treatment Candidate in Reducing Risk of Hospitalization or Death https://www.pfizer.com/news/press-release/press-release-detail/pfizer-announces-additional-phase-23-study-results
[31] Update: Ukrainian company Darnitsa signs sublicence agreement with MPP bringing to 36 the number of generic manufacturers to produce generic versions of Pfizer’s oral COVID-19 treatment https://medicinespatentpool.org/news-publications-post/update-ukrainian-company-darnitsa-signs-sublicence-agreement-with-mpp-bringing-to-36-the-number-of-generic-manufacturers-to-produce-generic-versions-of-pfizers-oral-covid-19-treatment
[32] Launch and Scalefaster :COVID-19 THERAPEUTICS https://launchandscalefaster.org/covid-19/therapeutics
[33] HealthData:COVID-19 Public Therapeutic Locator https://healthdata.gov/Health/COVID-19-Public-Therapeutic-Locator/rxn6-qnx8/data
[34] Kim Arin:Amid Paxlovid scarcity, Korea looks for alternatives 2022-3-25 http://www.koreaherald.com/view.php?ud=20220325000553
[35] African clinical trial denied access to key COVID drug Paxlovid. Nature 604, 412-413 (2022) https://doi.org/10.1038/d41586-022-00919-5
[36] Fraiser Kansteiner. High-flying Pfizer may disappoint on Comirnaty and Paxlovid sales in Q1, analyst warns https://www.fiercepharma.com/pharma/pfizers-first-quarter-haul-could-come-light-analysts-flag-overambitious-paxlovid-and
[37] Deena Beasley: Price of COVID treatments from Pfizer, Merck, GSK align with patient benefits -report https://www.reuters.com/business/healthcare-pharmaceuticals/price-covid-treatments-pfizer-merck-gsk-align-with-patient-benefits-report-2022-02-03/
[38] enny Lei Ravelo: 35 companies in 12 nations to manufacture Pfizer's oral COVID-19 drug https://www.devex.com/news/35-companies-in-12-nations-to-manufacture-pfizer-s-oral-covid-19-drug-102843
[39] 辉瑞官方:医疗保健提供者情况说明书:PAXLOVID™ 的紧急使用授权 https://labeling.pfizer.com/ShowLabeling.aspx?id=16474
[40] FDA:EMERGENCY USE AUTHORIZATION (EUA) OF PAXLOVID FOR CORONAVIRUS DISEASE 2019 (COVID-19) https://www.fda.gov/media/155051/download
[41] Pein Huang:Lifesaving COVID drugs are sitting unused on pharmacy shelves, HHS data shows https://www.npr.org/sections/health-shots/2022/03/18/1087380770/lifesaving-covid-drugs-are-sitting-unused-on-pharmacy-shelves-hhs-data-shows
[42] MSF responds to Medicines Patent Pool deal with 35 manufacturers to produce COVID-19 treatment nirmatrelvir/ritonavir https://msf-access-campaign.prezly.com/msf-responds-to-medicines-patent-pool-deal-with-35-manufacturers-to-produce-covid-19-treatment-nirmatrelvirritonavir
[43] WHO recommends highly successful COVID-19 therapy and calls for wide geographical distribution and transparency from originator https://www.who.int/news/item/22-04-2022-who-recommends-highly-successful-covid-19-therapy-and-calls-for-wide-geographical-distribution-and-transparency-from-originator
本文来自微信公众号:果壳硬科技(ID:guokr233),文章首发时间:2022年4月24日,作者:李拓、杨景诒

