两年多时间内,国产PD-1的价格下降了70%左右。PD-1作为一款数十年来难得一遇的超级靶点,吸引了无数创业者、科学家、资本。面对市场上同质化竞争的价格战, PD-1赛道上预期中的千亿市场或不复存在。本文来自微信公众号:八点健闻(ID:HealthInsight),作者:吴靖,责编:徐卓君,原文标题:《PD-1年费用进入1万元区间,国产创新药内卷和消失的千亿市场》,题图来自:视觉中国
在2020年年末一场足以改变国内PD-1格局的医保谈判中,一家重仓信达的基金公司的工作人员来到现场,试图打探恒瑞的PD-1抑制剂卡瑞利珠单抗是否谈成的消息。
信达作为当年唯一一家进入医保覆盖范围的PD-1药物,一时风头无两,2020年的销售额高达22亿,比起上一年的10亿的销售额,涨幅超过了100%。
2020年10月,素有“恒瑞出征,寸草不生”之称的恒瑞 ,在医保谈判开启前两个月,直接将自家的PD-1产品艾瑞卡的价格下调至3.96万一年,虽然公司解释为短期 的促销行为,但业界仍将其解读为一轮价格战的开端。
自2018年6月以来,陆续有8种不同的PD-1抑制剂在中国上市。
这8种PD-1产品在中国市场上经历了几轮价格战后,直接将PD-1的价格从年费用30万元以上(进口的K药和O药)打到10万以内——2019年医保谈判第一次将信达的PD-1产品信迪利单抗的年费用压制在10万以内。
但这远远不是尽头,在2020年末新一轮的医保谈判中,3家国产PD-1抑制剂,以平均降幅78%为代价,成功进入医保目录。
根据3月1日公布的新版药品目录,恒瑞的PD-1抑制剂卡瑞利珠单抗的年治疗费用从11.88万(慈善赠药后)降至4.98万元。
除恒瑞以外,另外两家谈判成功的国产PD-1抑制剂——君实的特瑞普利单抗和百济神州的替雷利珠单抗年治疗费用分别是5万和7万元左右。
比起一年前,国产PD-1抑制剂的价格几乎又下降了一半。
这也意味着,在两年多的时间内,国产PD-1的价格下降了70%左右(第一款国产PD-1抑制剂君实的特瑞普利单抗上市时年费用18.72万)出现了一般专利药7-10年后才会出现的专利悬崖。
PD-1作为一款数十年来难得一遇的超级靶点,吸引了无数创业者、科学家、资本, 打造出一个具有千亿潜力的市场,以一己之力塑造了中国本土创新药企当下的格局,是中国创新药企崛起的缩影。
如今,面对市场上同质化的竞争对手带来的价格战, PD-1赛道上预期中的千亿市场恐不复存在,它所面临的囚徒困境,又何尝不是中国本土的创新药产业在未来需要面对的困境?
百亿美元分子
某种程度上,做药就像挖矿,都是通过线索觉得某个地方可能有金矿,钱砸下去,赌一大笔高回报。
自制药业成为华尔街的宠儿之后,整个行业都以寻找和开发年销售额超过10亿美元的药物分子为己任。
2012年,跨国药企百时美施贵宝公布了O药(PD-1抑制剂)在令人束手无策的肺癌治疗的一期临床试验结果时,整个制药业为之欢呼。
人们确信,PD-1不仅仅是一款十亿美元分子,极有可能是一款百亿美元分子。
它不只带来了革命级别的治疗思维变化。PD-1抑制剂本身并不能直接杀伤癌细胞,而是通过激活病人自身的免疫系统来抗癌。这是最近十年肿瘤治疗领域最大的突破之一。
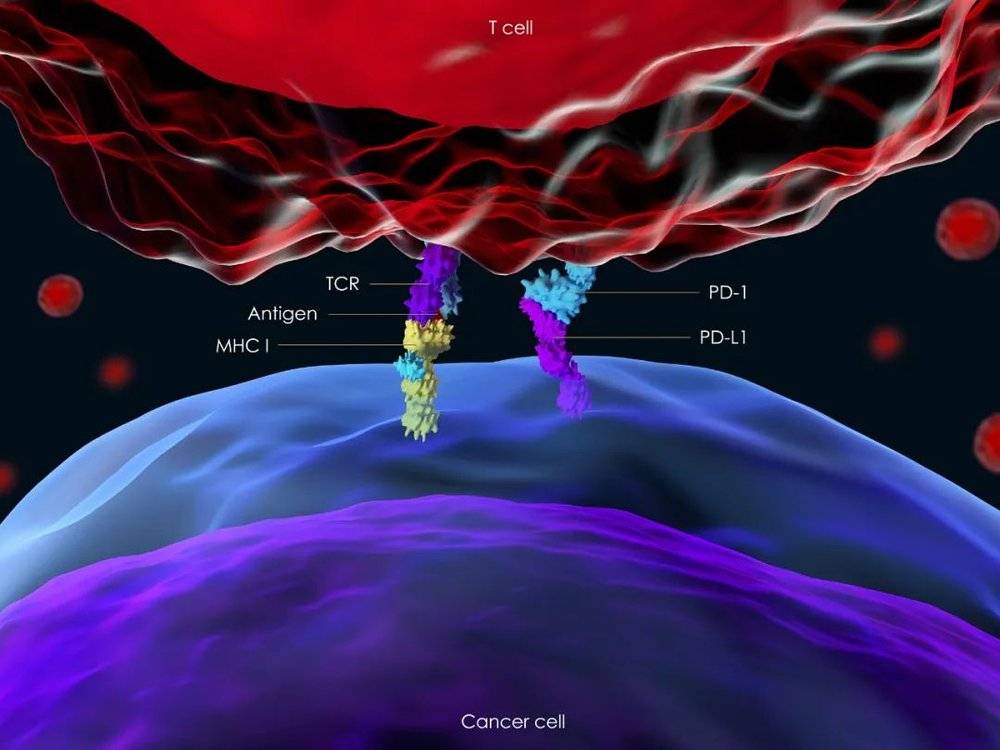
更重要的是,PD-1作为一种广谱的抗癌药物,横跨数十个癌症——尤其是肺癌、肝癌等大癌种,随着全球老龄化的进程,市场潜力无可限量。
彼时,《华尔街日报》大胆做出了预测:PD-1/PD-L1在全球的潜在市场规模有350亿美元/年,这个数字后来为不少PD-1相关的分析所津津乐道。
于是,一个席卷全球整个制药工业的PD-1狂潮随之兴起,不到10年,PD-1项目遍地开花,共有154个PD-1在做临床实验,其中已上市的有8个 。
更令人难以想象的是,中国竟然成为了PD-1投资和研发的热土:全球超过一半的PD-1由中国企业研发或合作开发,全世界已经上市的8款PD-1抑制剂,国产PD-1占了一半。
国内的资本市场热到什么程度了呢?有行业分析师回忆,不懂医药的一些投资人扎堆进入创新药行业,投资一家创新药企,评价标准只有一个,有没有PD-1。
PD-1似乎以一己之力,让国产药企和跨国药企有机会同台竞争,在极短的时间内,重塑了中国医药格局:一些以研发PD-1等免疫制剂起家的创新药企,正在从中国这个仿制药大国中,冉冉升起。
被重塑的中国医药产业格局
时间拨回2010年前后,此时中国生物药市场还是仿制药、辅助用药和中成药的天下,落后欧美十几年。
一批有跨国药企开发新药经验的科学家陆续回国创业,想做创新药。
但创新药是个极其烧钱的项目:在美国有一个双十定律——十年十亿美元才有可能诞生一款新药。
很多国产仿制药企曾有转型创新药的想法,但都被高额研发资金阻挡在了门外。只有极少数国产老牌药企试水,比如做仿制药发家的恒瑞医药。恒瑞在2010年开始就加大了对于生物药领域的研发布局,招了一批有丰富生物药创制经验的科学家。
经历过2008年金融危机的资本市场缓慢复苏,他们正在瞄向医药界下一个蓝海,免疫治疗。国际上对免疫治疗原理的研究结果和临床实验结果提振了他们的信心,包括令人振奋的PD-1,春江水暖,资本市场先知。
2011年,头顶多项光环、业界知名的肿瘤治疗药物专家俞德超自立门户创办国产创新药企信达生物仅2个月,便有资本闻讯而来。当年10月份,信达生物拿到了1000万美元的A轮融资;2012年6月,再次完成2500万美元的B轮融资。
但值得注意的是,投资机构特别是国内基金都对俞德超的做法最早持观望态度,信达生物的早期投资方,基本都是美元基金。此时国内的资本市场还在按兵不动。
国外热闹国内观望的情形在一年后很快被打破。
因为在2014年这一年,PD-1在国外有了实质性的突破:跨国药企巨头百时美施贵宝的PD-1(O药)在日本和美国获批上市了,用于治疗晚期的、不可切除的黑色素瘤,这是质的飞跃,从公布临床试验结果到上市,不过短短2年时间。
并且,FDA的审批速度之快,给所有研发PD-1的药企吃了定心丸:O药在黑色素瘤的审批比预期缩短了3个月。更夸张的是,2015年3月,FDA在O药新适应症非小细胞肺癌的审批上,也只花了不到一周的时间,就批准上市了。
当月,该跨国药企的市值突破1000亿美金。
千亿市场规模和一家跨国药企市值的极速提升刺激了国内资本市场的神经。国内资本市场变得热火朝天了起来。
新成立的创新药企,加诸创始人的光环,很快获得资本的青睐,手上突然有了大笔资金,但时间不等人,包括信达在内的一些刚成立的创新药企,早期开启了买买买的步伐,从国外购买以PD-1为代表的前期研发成熟的抗体技术,进行临床试验和商业化,极大缩短这些品种的生产周期。
这几乎成了国内最早一批创新药企的缩影。它们的路径几乎都指向那一条路:上市。
比如信达生物,2018年10月31日,带着一份巨额亏损单,信达奔赴港股上市:2016年、2017年分别亏损5.44亿元、7.16亿元;2018年上半年,亏损5760万元。但这依旧不影响市场给它的高估值,上市当天IPO市值156.36亿港元,较上市前E轮融资时80亿港元的估值翻倍,中间相隔不过半年。
虽然信达产品链上有 17个单克隆抗体新药品种在研发,但PD-1毫无疑问是信达高市值的核心。其当时的招股书里提到,中国PD-1及PD-L1的市场规模在2019年预计为12亿元,而2030年将达到984亿元。
创新药企估值在半年翻倍并非信达独有,2018年7月,也拥有PD-1研发项目的复宏汉霖完成1.57亿美元融资,投后估值200亿元,而半年前融资1.9亿美元的投后估值仅为100亿元。
但这些都不是最夸张的。
有一家创新药企靠一款上市不久的PD-1撑起了千亿市值,那就是君实生物。2020年7月15日,君实生物登陆科创板,市值高达1315.63亿。
虽然有人会反驳,在其产品线中还有更多在研品种,并非只有PD-1,但不得不承认,其在早期融资时,如果没有PD-1这个品种以及它带来的巨大的想象空间,投资者不会如此“阔绰”。
作为第一个获批进入PD-1临床试验的企业,就在当年8月,创始人熊俊很快将君实在新三板挂牌上市,半年内从资本市场募集了近6个多亿的资金,之后又不断发布定增融资方案,筹钱。这几乎是当时那一批创新药企最早上市的公司,又最早获得千亿市值的公司。
在热火朝天的几年间,不菲的市场定价,中国数以百万计的癌症患者,成为业界勾勒PD-1药物市场前景的横纵坐标。
资本、药企、证券分析师给予了PD-1最高期待,不断给这个市场输入信心:PD-1将成为中国肿瘤领域的最高标杆,诞生多个国内重磅新药(10亿元人民币以上)和超级重磅新药(50亿元人民币以上)。
根据业界的估算,到2030年,中国的PD-1市场一年的销售额就高达千亿人民币。在君实和信达的招股书中,都向投资者传递了这一信息,考虑到PD-1的高昂的国际市场定价和中国每年新增的400多万癌症病人,这个市场预期并不算太过分。
从某种程度上,PD-1以一己之力塑造了中国本土创新药企当下的格局。因为,在PD-1还未在中国上市的2014年,根据花旗研究的报告数据,在中国卖得最好的药物还是生理盐水(氯化钠)。
国产PD-1的囚徒困境
但很快,还没等来想象中的国内千亿市场,PD-1在中国的内卷提前开始了。
早在2018年,国产PD-1上市前夕,时任百济神州中国区总经理吴晓滨说,“在PD-1上打价格战没有出息。”
一语成谶。
最先降价的是跨国药企。2018年是中国PD-1元年。跨国药企生产的K药、O药在中国获批,国产PD-1也相继问世,受到国产药的价格压力,O药在国内20多万一年定价、K药30多万一年(慈善赠药后)的定价,比起在美国十几万美元一年的定价,显得“平易近人”了许多。
当2018年国家医保局成立后,一个医保超级大买方掀起了前所未有的医保控费的大浪潮。
医保控费对于创新药的策略之一就是医保谈判,这带来了更广阔的使用人群,以及愈发激烈的价格战。
一个典型例子是,最早在国内上市PD-1的君实生物一边向外界吹风呼吁希望尽快进医保,以量换价,另一方面自动将定价调低,以示诚意,上市价格仅18.4万一年,如果算上慈善赠药后,年治疗费用约10万元,是进口K药的三分之一。
这一下子让各方惊掉下巴,低价竞争为进医保带来的价格战一触即发。
2019年11月医保谈判,医保局首次将PD-1纳入医保谈判,进口O药和K药被预测大概率不会大幅降价进医保,当时已上市具备谈判资格的两款PD-1(君实PD-1和信达PD-1)是否会进入医保成了最大关注点。
在谈判期间,有不少人判断两家国产PD-1都谈判成功,但最终结果是只有信达的PD-1进入医保。谈判前,信达PD-1的年治疗费用在16.7万元左右,谈判后医保支付价公布后,年治疗费用是9万多,年治疗费用下降了42%。
也很少有人能预测到,随着百济神州、恒瑞等更多国产PD-1玩家的加入,原本在国内预测十几万年治疗费用的国产PD-1,在第二次医保谈判,降到了如今的五万元左右。
进入到中国的四款进口PD-1,受到维系全球定价而早早败北,无缘医保。
不过,君实最初所期冀的进入医保意味着“以量换价”可能只是空想。
当2020年底医保谈判中,信达以外的三家国产药企PD-1挤破脑袋经过大幅降价才谈判成功进入医保后,很多人才意识到,它们又重新回到同一起跑线,价格战的高潮才刚刚开始,进入医保只是价格战的开端,一张重新站在同一起跑线的门票。
医保谈判不能完全带来确定的市场,这是最令人焦虑的。能销售的量,还要看一个药企商业化能力、销售能力等。
而且,目前五万一年的价格很有可能不是尽头,每两年一次的医保谈判是悬在各家药企头上的紧箍咒, 3万一年并不会太遥远。
根据西南证券杜向阳的分析报告,如果以年费用6万计算,中国PD-1总市场空间为305亿元;如果PD-1的价格进一步下降到3万一年,虽然市场的渗透率有望提升的,但市场规模将萎缩至236亿元。
除了价格战,他们正在烧钱铺开更多PD-1新适应症的临床实验,比拼临床试验速度等,在低价的道路上,试图覆盖更多癌症人群,获得更多的销量。
因为PD-1在瘤种上有非常大的发挥空间,目前有效的瘤种大概有11个,实际上还有更多细分的瘤种,一旦在这些方向上面选了一个别人没做的适应症,还做出了非常好的疗效,就还有一丝机会。但换句话说,四家国产药企新适应症临床试验速度相差不大,依靠新适应症加强竞争力,可能只是暂时的安慰,这个窗口期这个逐渐缩小。
举个例子,君实PD-1的新适应症鼻咽癌刚获得审批,恒瑞就紧跟其后,被传很快就要获批,这期间相差不过几个月。
正如恒瑞董事长周云曙在一场闭门论坛上所说,“现在整个PD-1都是囚徒困境,这不是恒瑞的问题,而是PD-1太多了。”
中国国产PD-1,正在面临一场高度同质化竞争,但是仅仅在几年前,被赞美重塑中国医药格局的PD-1药企,谁会想到如今的局面呢?
无论如何,一个具有想象力的千亿市场,可能将不复存在,而后来者PD-1,将很难从这个正在缩水的市场中分一杯羹。资本是残酷的,投资人很快意识到这个问题,除了加码目前已经上市的四家药企,不断为他们铺开的临床实验投入大笔资金外,他们已经不用愿意再赌注后面的几十个还未上市的PD-1。
无形之手
多数观点认为,国内药企和资本的蜂拥而至,同质化的药物,是当下国产PD-1困局的根源。
但实际上,作为超级支付方的医保,才是背后的无形之手。
在过去二十年间,在以仿制药、中成药、过期专利药为主的中国医保目录中,很少出现高价创新药的身影。
医保支付和药品定价只能分属不同职能部门,甚至出现了2016年国家卫健委对高价抗癌药进行谈判降价,但却无人执行最后不了了之的结果,抗癌药在市场售卖依旧维持原价,因为这些抗癌药不在医保目录中,既没有一个巨大的支付方对降价的抗癌药买单,又没有足够多的中国本土创新药企,高价抗癌药依旧维持跨国企业自主定价的局面。
高定价之所以难以撼动,是因为创新药拥有专利保护,一套完善的专利网可以为创新药企业有效阻隔后来竞争对手,维持某个药物分子甚至某个治疗领域的垄断竞争格局,以此获得较高的定价权与渗透率。而垄断意味着高价和少数人群,由药企主导话语权的市场。
2018年3月国家医保局成立,这是中国医保制度成立以来,第一次出现的一个超级支付方,它的背后是全国十三亿参保人。
它正在用庞大的人口和消费量支起一个杠杆,撬动起原本难以撼动的垄断性高价创新药市场。
比如医保谈判,重构了国内的创新药的供需关系,创新药的有效供给大幅增加,买方继续集权增加博弈筹码,供给端继续增加有效供给,这个政策预期长期存在。有人评价,未来,市场博弈自然会达到更优的价格配置。
很少有创新药企不为此心动,这既能迅速扩大销售量,也让药能直接进入医院药房,少了不少中间环节。但代价就是,大幅降价。
在中国有史以来最强大的支付方国家医保局的调控下,一个不同于以往甚至是其他国家的创新药市场在中国出现了:超级支付方主导的以量换价的市场。
高价创新药的垄断规律被打破,创新药市场的消费群体从原本少数中产阶级群体延伸,正在触达四五线城市的普通工薪家庭,普通老百姓也能吃好药了,中国的创新药消费格局正在发生巨变。
自2021年3月1日开始,国产PD-1的价格进入5-7万一年的区间,若以70%-80%的医保报销比例计算,个人自付部分一年最低可降至1万。
这种在美国初上市的价格高达100万人民币的“神药” ,在中国已经可以说变成一款平价药了。
比起20年前格列卫刚进入中国时,一个月超过2万元的天价药费时,这个全新的市场格局对于中国的病人而言,无疑是福音。
出海能解决问题吗?
国产PD-1药企从内卷化的国内走出来,争夺广阔的海外市场,似乎成了新的选择。
即便走上出海这条路,对于本土药企来说也实为不易,还有更多问题等着它们去解决。
2019年4月,在美国癌症研究协会年会(AACR)上,美国FDA肿瘤学卓越中心主任Richard Pazdur被一位观众提问,FDA在批准一个新药时是否会考虑价格因素,他的回答是:FDA不考虑价格,但是FDA会欢迎成本较低的PD-1/PD-L1抑制剂进在美国上市。
他在会上提到,中国公司在PD-1药物价格上的竞争对大家来讲可能是一件好事,因为还没有看到这些大型制药公司在PD-1药物价格上有松动的迹象。
这种鼓励姿态的背后,还有更大的推手:2017年6月,中国加入ICH(人用药品注册技术国际协调会议)。这意味着之后中国临床数据可以和欧美互认,一些本土药企可以拿着在中国的PD-1临床试验数据去申请FDA审批上市,只要临床数据的质量足够好。
在这个充满鼓励色彩的2019年,一批本土药企开始将目光瞄向那个曾经遥不可及的海外市场。
当然远不止鼓励,还有无奈的现实因素:迅速萎缩的400亿国内市场,撑不起资本给这个品种带来的1000多亿人民币估值和巨大的想象空间。
国内市场萎缩的另一面是,中国PD-1赛道的拥挤程度,已经赶英超美。到了2019年,中国在研PD-1项目有50多个,美国40多个,欧洲10多个,日本是个位数。
上述种种因素的叠加之下,中国的PD-1企业开始从国内转移到了海外。
于是,2019-2021年间,跨国联姻成为PD-1药企的主流选择。一些成立时间不长的本土药企更多借助跨国药企的成熟的临床研发实力和销售渠道,打开局面,而非自己搭建,它们已经意识到,无论是国内还是海外市场,时间是生命,已经耗不起,搭建平台销售团队和渠道需要时间,这期间,市场可能早就被瓜分完毕。
信达生物和跨国巨头礼来联姻是一个典型。信达生物2011年才成立,即便是国内销售渠道,也无法在短短几年内全面铺开,干脆和深耕中国多年的跨国药企礼来合作,礼来负责国内销售。
2020年8月,这种合作模式从国内拓展到海外。信达生物又将北美、欧洲及其他地区的PD-1独家研发和销售许可给了礼来,与此同时,信达生物可以获得2亿美元的首付款和高达8.25亿美元的开发和销售里程碑付款。
这个海外市场不止是欧美等国家,也有本土药企将对准了“潜在的蓝海市场”—东南亚市场。
2019年9月,一家本土药企复宏汉霖授权一家印度尼西亚制药公司进行PD-1首个单药疗法及两项联合疗法在东南亚地区10个国家的独家开发和商业化权利。而复宏汉霖获得了1000万美元的首付款、最高达6.5亿美元的销售里程金、最高达2200万美元的监管里程金以及1000万美元的联合疗法临床试验资金。
早期出海失败的恒瑞医药,也不甘示弱,在中国获批上市后,找到了一家韩国医药公司,2020年4月,双方达成了一项金额为8775万美元的合作协议,该韩国公司将恒瑞医药PD-1在韩国的独家临床开发、注册和市场销售的权利。
在跨国药企联姻趋势日渐明晰之下,已经出现了另一个语境:一些跨国巨头在早期误判错失PD-1,主动找到本土药企合作,拓展海外市场。
比如,在几大跨国巨头中,只有诺华的PD-1进展不佳,急需在外界寻找成熟的PD-1药物补充管线。此前没多久,诺华就宣布其在研PD-1抑制剂,在联合BRAF抑制剂Tafinlar(达拉非尼)和MEK抑制剂Mekinist(曲美替尼)一线治疗无法切除或转移性的突变阳性黑色素瘤的3期临床研究中未达主要终点,宣告失败。
没过多久,今年1月跨国药企诺华主动牵手本土药企百济神州。双方就百济神州PD-1在多个国家的开发、生产与商业化合作达成协议,百济神州获得了6.5亿美元,如果顺利,合作总交易金额将高达22亿美元。
不过,对跨国药企来说,中国药企正在争夺的海外市场,也就是它们的本土市场,竞争同样惨烈。FDA已经批准了来自7家公司的6种PD-1/PD-L1抑制剂,涉及近50种适应症。
PD-1的困境,也是中国Me too药物的困境
在国产PD-1陷入价格战的2020年,默沙东的PD-1抑制剂K药成长为销售近150亿美元的超级重磅产品。
它不但贡献了默沙东2020年全年制药营收的三分之一。还一跃成为跨国药企TOP10销售单品中的第二,和第一名修美乐的差距不过50亿美元。
再看K药2014年上市后的销售数据:2015年5.66亿美元,2016年14.08亿美元,2017年30.09亿美元,2018年71.71亿美元,2019年110.84亿美元,2020年143.8亿美元。
以这样的趋势来看,明后年,PD-1会在全球迎来单品种千亿元市场的巅峰时刻。第一名全球药王修美乐,用了14年时间,才登顶全球千亿元市场,而K药,大概率只需要7年时间。
明年,对于国产PD-1企业而言,同样是关键的一年。
四家国产药企一起进入医保的第一年,虽然价格和利润的预期大幅降低,有医保这个超级支付方的加入,将是放量的一年。这一年的厮杀,必将决定中国PD-1赛道未来的格局。
恒瑞没有披露2020年PD-1的销售额,但是第三方披露,恒瑞光是今年上半年就卖了20亿。这还是在没有进入医保的情况下,半年销量接近进入医保的信达全年销量。
这也是为什么好些同行将销售能力极强的恒瑞医药视为“搅局者”。
中国的PD-1赛道,本质上仍然是一个销售驱动,而非创新驱动型赛道, 而这些恰好是这些成立不到10年的创新药企的弱项——一个被业界广为流传的数字是,恒瑞在PD-1上的销售人数十倍于这些新兴的创新药。
不得不承认,即便PD-1被称为是肿瘤免疫领域的神药,中国本土药企做出来的PD-1还是只能是me too的跟踪性创新药。进入生物大分子药时代以来,比起格列卫这样的小分子药物,更容易绕开专利保护。各家药企的PD-1只是分子结构和序列有轻微差异,这些细微的差异,并不足以给某个药企的PD-1,在疗效方面带来显著优势。
目前本土药企在做的50多个PD-1临床试验,大多数都是K药和O药已经做过或者正在做的,此前K药和O药加起来已经做了好几百个与不同癌症相关的临床实验,有的成功了,有的失败了。
而很多本土药企采用了最简单的一种方法,跟着K药和O药做,K药新开了哪个癌种的试验,就直接拷贝。“比如K药后面失败了,这时候你抄了K药的,没有动脑子,它失败的时候你就会很尴尬”,有本土PD-1药企内部人士评价。
这种事不是没有发生过。2019年上半年,K药在美国的两个主要的联合用药临床III期试验都宣告失败,消息一出来,国内不少布局PD-1的药企傻眼了,因为同样的联合用药临床试验国内有20多家正在做。
而为了争夺市场,就只要在同质化竞争下寻求适应症的差异。
依靠单一PD-1品种融资、上市的本土药企根本无法停下脚步,只有通过不断铺开更多的适应症以及适应症更快的获批去争夺半年甚至只有1个月的窗口期,稍不留神,就会错过所谓的黄金销售期。
随着及国内同质化产品的竞争,导致中国特色的跟踪性新药在未来的市场机会越来越小,这也大概率是其它跟踪性“创新药”会发生的故事。
中国新药投资人在经历了20多年的新药投资以来,很多投资人通过资本市场实现了财务回报,但是未来在超级支付方医保的调控之下,me-too药物必然不可能像美国的创新药市场一样能获得高额利润,“重磅产品”在中国的实际市场规模较预期大幅缩水,PD-1不会是个例。
作为“重磅产品”PD-1的预期市场规模都在缩水,其他靶点的跟踪性新药在中国前景几何?那么这些跟踪性新药公司未来是否还会有投资人期望的盈利机会?
本文来自微信公众号:八点健闻(ID:HealthInsight),作者:吴靖,责编:徐卓君

