3. 由于临床试验的评判标准不同,无法准确比较出疫苗的“高下”。在信息有限的情况下,对于各款疫苗的安全性,只能谈“感觉”。梳理各种疫苗的副作用,目的在于让民众有正确的心理准备。各种疫苗的不良反应有所不同,但严重的不良反应都比较少。
4.中国的灭活疫苗存在独有优势,让其走向世界是提高中国形象、帮助全球抗疫的好机会。但疫苗说明书也应该达到国际标准,实事求是地根据临床试验所观察到的数据来描述。

国药灭活疫苗的副作用有73种?网上为何流传两个不同版本说明书?450万接种者副作用与说明书副作用相比,真相可能令人大吃一惊!
副作用几乎是所有疫苗的“命门”,尤其是严重的副作用,它的任何风吹草动,都会成为重大公共事件。2020年12月31日, 国药集团中国生物北生所的新冠灭活疫苗获得国家药监局附条件上市批准。关于这款疫苗,日前网络上流出了一份 “招标专用”说明书,核准日期为2020年12月30日。

在说明书中,列举了该疫苗可能出现的不良反应,数了一数,有73种之多,其中甚至包括流行性感冒、粪便变色等等。注意到其中很多症状十分罕见,发生率低于0.01%,也就是每万人中都不会出现一例。在网络上,还有一份“北生所”无核准日期的说明书,其中所提到的不良反应,十分常见的是注射部位疼痛;常见的是发热、乏力、头痛、腹泻;注射部位发红、肿胀、瘙痒、硬结;偶见的是注射部位皮症,恶心呕吐,非接种部位瘙痒,肌肉痛,关节痛,嗜睡,头晕等。

该说明书表明:未出现与疫苗接种有关的严重不良反应。这两个说明书,是否一个是李逵,一个是李鬼?到底国药灭活疫苗会有什么样的不良反应?在“招标专用”的说明书中,提到了3期临床试验,但是目前此款疫苗并没有公布3期临床研究的细节,更没有正式发表试验结果。因此,本文只能参照已发表的1/2期临床试验的数据,对注射疫苗后的不良反应进行推测。国药北生所灭活疫苗的1/2期临床试验结果,于本月发表于《柳叶刀|传染病》杂志[1]。在1期临床试验中,测试了三种不同的疫苗剂量:2微克、4微克、8微克。从目前的信息分析,三期临床试验及紧急接种使用的剂量,对应的是4微克疫苗剂量。在2期临床试验中,接种4微克剂量的受试者,需要接种两次,根据接种的间隔时间分成了三组,分别为间隔14天、21天、28天,每组112人。根据所发表的结果,在接种疫苗7天内,总体上有12%~21%的受试者出现不良反应,主要是注射部位疼痛(7% ~14%)和发烧(1% ~4%),所有观察到的不良反应都是1级、2级,没有严重不良反应。表1:国药北生灭活疫苗在2期临床试验中的不良反应统计
任何级别
局部
注射部位疼痛
7% ~ 14%
注射部位发红
0% ~ 1%
注射部位发肿
0% ~ 4%
注射部位发痒
0% ~ 1%
皮疹
0%
系统性(全身)
发烧
1% ~4%
疲劳
1% ~ 2%
头痛
0% ~ 2%
非注射部位瘙痒
0% ~ 2%
恶心
0% ~ 2%
咳嗽
0% ~ 1%
腹泻
0% ~ 2%
肌肉痛
0% ~ 1%
严重过敏性休克
0%
嗜睡
0% ~ 1%
眩晕
0%
所以,从1/2期临床试验的结果看,“无核准日期”的说明书,更接近于临床数据。会不会是3期临床试验发现了更多的不良反应,导致说明书将不良反应增加到73种呢?这基本不可能!那份“招标专用”的说明书,因为自媒体人士陶黎纳先生的曝光,引起了各方人士的关注。环球时报主编胡锡进发表文章对此做出解读:
“老胡了解了情况,‘73种不良反应’确实写在国药疫苗的说明书里,但那是对所有潜在、可能副作用的罗列,是国家药监局对疫苗说明书的规定内容。它们不是国药疫苗在三期临床试验中已经出现过的不良反应,而是对各种相近疫苗历史上有过副作用的总结性提示。药监局要求必须这样写,让接种者了解包括最坏情况的全部信息。尽管有的副作用可能永远不会发生,但只要没有证据能够确定它们发生的可能性是零,就得写上。”
如果老胡了解的这个情况属实,那更加说明这个招标说明书是非常不合理的!既然是药品、疫苗的说明书,那必须“量体裁衣”,以试验数据为准绳,而不是把其他药品、疫苗出现过的情况也简单地罗列进来。
药品说明书是否应该更明确地反应不良反应的真实数据,而不是各种尚未发生的可能性呢?如果说明书都不需要根据临床试验所观察到的结果来写,那又有什么必要做临床试验?吃瓜群众如何相信疫苗的保护效果?又怎么能对疫苗的安全性放心呢?在入冬之后,国内多地出现了疫情,目前河北省石家庄市藁城区为疫情高风险地区,在北京、河北、辽宁、黑龙江,有59个中风险地区。为了防备疫情因为春运进一步扩大,国内已经开始大规模接种疫苗。如果这个时候要按照某种“规定”把别的疫苗的不良反应也写到说明书里,不但不是实事求是,而且会让民众对疫苗的根本不存在的副作用产生恐惧,影响疫苗的接种。

图/2020年11月3日,迪拜王储谢赫·穆罕默德·本·拉希德·阿勒马克图姆(左)准备注射国药疫苗2020年12月31日,卫健委发布会公布的数据表明,中国已经接种了450万剂,接种疫苗者达到总人口比例的0.32%,主要接种的是国药集团的疫苗。卫健委副主任、国务院联防联控机制科研攻关组疫苗研发专班负责人曾益新称,疫苗的不良反应情况及总的发生率,跟常规接种的几种灭活疫苗很接近,主要的表现是一些局部的疼痛、局部的硬结这样一些情况。这其中,轻度发热的病例大概不到0.1%,过敏反应等比较严重的不良反应发生率大约为百万分之二。


辉瑞疫苗的副作用是否比说明书标注更严重?论文提及的淋巴结肿大为何没有标注到说明书中?国药说明书事件在国内外媒体上以不同的方式被解读。药品说明书上的副作用应当如何撰写,如何表述,对于疫苗发达国家来说,显然都有一家的约定俗成的标准。他们是如何撰写至关重要的副作用,以及疫苗的安全性如何表达,或者说,这两种疫苗的副作用是否比国药严重还是轻?美国最先获得紧急批准的新冠疫苗,是辉瑞的mRNA疫苗。这款疫苗由德国BioNTech研发,中国的复星医药是其在大中华区的合作伙伴。目前这款疫苗已经在美国、欧洲等很多国家和地区得到了(紧急)上市批准。从美国FDA的网站上,可以查到辉瑞疫苗的“说明书”。

在不良反应中,说明书提到了如下的不良反应:注射部位疼痛,疲劳,头痛,肌肉疼痛,发冷,关节痛,发烧,注射部位肿胀,注射部位发红,恶心,不适和淋巴结肿大。说明书还提到,在大规模接种该疫苗的过程中,发现了严重过敏反应。

上面提到的这些不良反应,具体数据来自3期临床试验。辉瑞的临床试验数据,于12月10日FDA紧急批准该疫苗之前发表于《新英格兰医学杂志》[2]。根据所发表的数据,有26.7%的疫苗组受试者在接受第一剂注射后报道了不良反应,其中与疫苗注射有关的不良反应比例为20.7%。在这些不良反应中,绝大多数是轻微、不严重的,接种者出现严重不良反应的比例是0.6%,共126起,但其中只有4起是与接种疫苗有关,具体为注射疫苗引发的肩伤, 右腋窝淋巴结肿大,阵发性室性心律失常和右腿感觉异常。作为参照,注射生理盐水的对照组,也有12.2%的受试者在接受第一剂注射后报道了不良反应,其中与注射有关的不良反应比例为5.1%。在这些不良反应中, 严重不良反应的比例是0.5%,共111起。既然对照组也出现了不良反应,这说明部分不良反应是与打针有关,并不是新冠疫苗所特有。并且,也不是所有在疫苗注射后出现的不良反应,都等于是疫苗的副作用。
任何级别
严重
局部
注射部位疼痛
66%~ 83%
注射部位发红
5%~7%
注射部位发肿
6%~7%
系统性(全身)
发烧
1% ~16%
疲劳
34%~ 59%
3.8%
头痛
25% ~52%
2.0%
发冷
6%~35%
呕吐
0~2%
腹泻
8% ~11%
肌肉痛
14%~ 37%
关节痛
9%~ 22%
表:辉瑞疫苗临床试验中出现的不良反应[2]。大家可能注意到,在上述不良反应比例的列表中,仅仅出现注射部位疼痛的比例,就高于前面所提到的“有26.7%的疫苗组受试者在接受第一剂注射后报道了不良反应”。为什么会出现这个差异呢?26.7%这个比例,分母是所有疫苗组的参试者,而后面列表中的分母,则只是收集了“反应原性”数据的参试者,只有总人数的五分之一。在出现的不良反应中,第二针后出现的要比第一针稍微更多一点,但年长者(65岁以上)要比年轻者要少一些。局部出现的症状,一般在1-2天之内消失。

图/FDA上标注的辉瑞疫苗的副作用说明书。对于不良反应的定义,“轻度”指不干扰日常活动,“中度”有干扰,“严重”则是妨碍了日常活动;4级以上的不良反应,则需要急诊或住院。对于注射部位的红肿,严重者直径> 10.0厘米;4级为出现皮肤坏死或脱落性皮炎。对于呕吐,轻度指24小时内呕吐1至2次,中度为 2次以上,严重者是需要静脉补水。对于腹泻,轻度、中度、严重者分别是24小时内发生2至3次, 4至5次,及 6次以上。发烧为38摄氏度以上,严重者为39~40度,4级为40度以上。从不良反应来看,绝大部分不良反应都是轻度、中度,严重的不良反应较少,有3.8%的接种者出现严重疲劳,2%的人出现严重头痛。在说明书中,提到“不适”和淋巴结肿大,没有提到腹泻。淋巴结肿大不在列表里,但在论文中,提到疫苗组有0.3%的人出现了淋巴结肿大。“不适”是个一般性的表述,可以代表腹泻,也可以代表其他极小概率的不良反应。此说明书也提到了禁忌症:对mRNA疫苗成分有严重过敏反应。目前美国疾控中心认为,如果对聚乙二醇(PEG)或聚山梨酯过敏,要避免注射mRNA疫苗。聚乙二醇是疫苗中的一个成分,聚山梨酯不存在于疫苗中,但是与聚乙二醇有相似。

图/人们在佛罗里达州萨拉索塔的诊所排队等候接种疫苗,目前美国有将近700万人接种了疫苗。

Moderna公司mRNA疫苗的副作用与辉瑞疫苗相似,多了局部腋窝肿胀Moderna疫苗是美国批准的第二款疫苗。笔者从美国FDA的网站上,也可以查到Moderna疫苗的“说明书”。显然疫苗的说明书在美国官方网站可以随时获取,并不是什么“机密”。

在说明书里,疫苗的不良反应包括:注射部位疼痛,疲劳,头痛,肌痛,关节痛,发冷,恶心/呕吐,腋窝肿胀/触痛感,发烧,注射部位肿胀, 注射部位出现红斑。Moderna疫苗的临床试验数据,于12月30日发表于《新英格兰医学杂志》[3]。从所报道的不良反应种类和比例来看,基本与辉瑞疫苗类似,但是少了腹泻,多了局部腋窝肿胀/触痛感。Moderna疫苗说明书提到的不良反应种类,与论文中所观察到的一致。在辉瑞和Moderna疫苗的说明书中,都提到:当大规模推广使用疫苗时,其他的不良反应会出现,包括严重不良反应。
任何级别
严重
局部
注射部位疼痛
83.7%~ 88.2%
2.7%
注射部位发红
2.8%~ 8.6%
0.3%
注射部位发肿
6.1%~ 12.2%
0.5%
腋窝肿胀/触痛感
10.2%~ 14.2%
0.3%
系统性(全身)
发烧
0.8% ~15.5%
0.1%
疲劳
37.2%~ 65.3%
1.8%
头痛
32.7% ~58.6%
1.0%
发冷
8.3%~44.2%
0.2%
呕吐
8.3%~ 19%
肌肉痛
22.7%~ 58%
0.6%
关节痛
16.6%~ 42.8%
表:Moderna疫苗临床试验中出现的不良反应[3]。

了解这三种国内外新冠疫苗的不良反应,不是为了比对各款疫苗的高下?要对不同的疫苗进行比较,很重要的一个条件,是要有公开透明的信息!这就好比要对比两个国家的疫情,如果一个国家病毒检测做到了应检尽检,而另一个国家却该检不检,那就无法做出比较了。不仅如此,由于不同临床试验的评判标准不一样,也不可能仅仅依据来自不同试验的数据,就准确地比较出两种疫苗的高下。比如说,在国药北生所的2期临床试验中,3级发烧的标准是体温超过38.5摄氏度,而辉瑞的临床试验中,是38.9摄氏度以上。同样的发烧温度,在一个临床试验中只是2级,但在其他的试验中就报道为3级不良反应。所以,在目前信息有限的情况下,对于各款疫苗的安全性,不能谈比较,只能谈“感觉”!感觉上是灭活疫苗的不良反应相对要少。在同时进行几款新冠疫苗3期临床试验的巴西,布坦坦研究所曾对媒体表示,“科兴的灭活疫苗安全性更好”。当然,科兴的3期试验的具体数据,目前也没有报道细节。
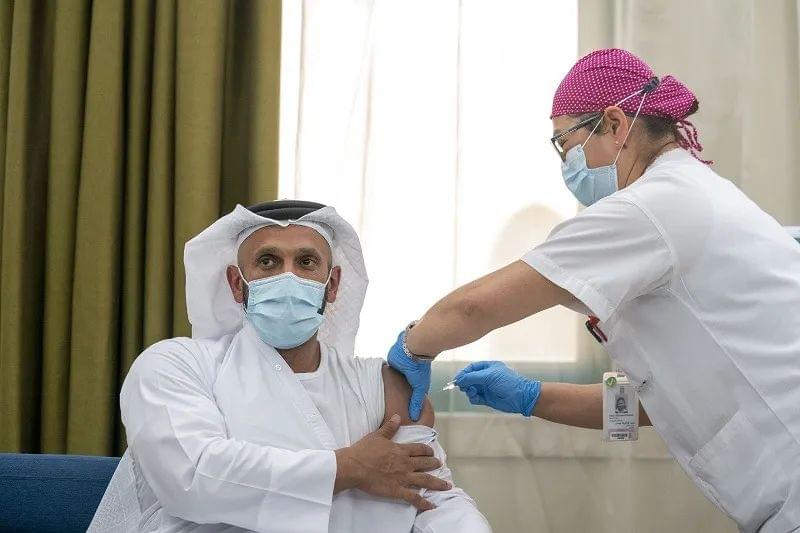
图/阿布扎比卫生部长Sheikh Abdullah bin Mohammed Al Hamed正在接种国药疫苗如果目前无法准确地横向比较几款疫苗,那我们梳理不同疫苗的副作用,又有什么意义呢?其实只是希望大家对可能出现的不良反应有一个正确的心理准备。有人关心疫苗,目的只是为了想知道自己能打的疫苗,是不是比别人的更好。在如今的疫情面前,我觉得这个关心的焦点有点儿歪!目前中国出现的本土疫情,多少都跟输入的病毒有关,这其实也是再次提醒所有人:在病毒面前,没有国界,即便中国有超强的能力一次又一次地交出漂亮的抗疫作业,但是只要世界上的疫情不断,中国就会不断地面临输入疫情的压力,同样会有巨大的抗疫成本。相反,如果全世界都能用上安全、有效的疫苗,疫情因此而大大缓解,中国的压力也就减少很多。因为目前疫苗紧缺,不同的疫苗之间,其实不是竞争关系,而是互补关系。在疫苗的有效性、安全性获得3期临床试验的验证之后,需要尽可能地快速推广使用,才能尽快控制疫情。只有阻断疫情,才可以避免病毒变异出毒性更大的毒株,给人类带来更大的灾难。

图/2020年4月11日,员工在国药控股北京疫苗生产厂检查和清洁设备


无法对疫苗进行挑选是如今的现实,但需要公开透明的数据让民众尽快接受疫苗目前世界各地总共批准(包括紧急批准)了7款疫苗,包括两款RNA疫苗,两款腺病毒载体疫苗,3款灭活疫苗。很多人感觉疫苗太多,仿佛进了餐馆,看到菜单上各种美味佳肴,面临着选择性障碍。但是,这个感觉是错误的。事实上,目前的新冠疫苗并不是太多,而是太少。比如目前美国,只有mRNA疫苗,没有灭活疫苗,即便接种mRNA疫苗,也需要根据感染风险排队等待接种,而一旦排到,自己并无选择。同样,在中国国内的人,目前也只能选择灭活疫苗。虽然复星医药跟德国BioNTech有合作协议,在今年将有1亿剂mRNA疫苗提供大陆使用,但是目前尚未在国内获得上市批准。即便是目前有两种mRNA疫苗和科兴灭活疫苗的新加坡,民众也无法对疫苗做出选择,按规定是随机分配疫苗,在注射后才知道使用的是哪一种。由于mRNA疫苗需要低温保存,这也对疫苗的可及性带来了限制。对于一个缺少零下70度或零下20度冰箱的地区,将无法选择mRNA疫苗,只有选择灭活疫苗或者腺病毒载体疫苗。

所以,疫情治愈了所有的选择性障碍症。如果目前需要打疫苗,不但无法根据疫苗的保护率做出选择,也不能对安全性做出选择。没有选择,是否就不需要对疫苗的效果和不良反应做出合理的说明呢?并非如此。不管是哪种疫苗,都会有不良反应,虽然目前几款疫苗的不良反应会有所不同,但是严重的不良反应都比较少,没有成为各国药监部门准许疫苗上市的障碍。中国的灭活疫苗,有自己的一些优势,如果这个时候能走向世界,不但可以提高中国产品的科技形象,也可以真正地帮助全球抗疫。面对这没有国界的病毒,帮助别人,其实也是帮助自己。但是,如果要走向国际,疫苗说明书就应该达到国际标准,实事求是地根据临床试验所观察到的数据来描述,完全没有必要穷举各种毫不想干的症状。直播的时候不开美颜,那叫实在;但如果为了追求真实,干脆几天不洗脸,直接蓬头垢面上镜,那就是奇葩了。
参考文献:
1. Xia, S., et al., Safety and immunogenicity of an inactivated SARS-CoV-2 vaccine, BBIBP-CorV: a randomised, double-blind, placebo-controlled, phase 1/2 trial. The Lancet Infectious Diseases, 2020.
2. Polack, F.P., et al., Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. New England Journal of Medicine, 2020.
3. Baden, L.R., et al., Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. New England Journal of Medicine, 2020.
4. https://www.fda.gov/media/144413/download

