本文来自微信公众号:iSynBio造物 (ID:gh_1c7f920d8f21),作者:赵杭,题图来自:《普罗米修斯》
纵观人类与病毒的斗争史,从16世纪的天花大流行,到当下的新冠疫情,每一次病毒的肆虐都对人们的健康和生活产生了深刻的影响。“病毒”二字似乎已经成为了人们眼中“恐惧”和“死亡”的代名词。
但随着生物学的发展,科学家们发现,病毒并被没有我们想的那么邪恶。事实上,自然界也存在很多对人类生命健康有益的病毒,比如噬菌体。
噬菌体是一类能够专一性地感染细菌而的病毒,对正常而不会影响人体细胞不会产生影响的病毒,凭借着这一特性。因此,它们噬菌体可能会成为是人类对抗超级耐药菌的终极武器。
另一方面,随着基因工程技术的发展,科学家们可以精准地改变病毒的基因,从而改变病毒结构或清除病毒毒性,甚至赋予它们治疗疾病的能力,让它们“弃恶从良”,为我人类所用。
一个经典的案例就是改造艾滋病的病原体——人类免疫缺陷病毒(human immunodeficiency virus,HIV)。它和新冠一样,也是单链RNA病毒。但HIV属于逆转录病毒科(Retroviridae)的慢病毒属(lentivirus)。与其它病毒相比,HIV最为特殊的地方是存在逆转录酶。
什么是逆转录酶呢?这要从中心法则谈起。大家都知道,DNA是携带遗传信息的载体,根据中心法则,DNA先转录为信使RNA(messenger RNA, mRNA),再翻译为蛋白质,进而发挥生物学功能。总之因此中心法则代表了遗传信息流动的方向,即“DNA→RNA→蛋白质”。
然而,凡事都有例外,HIV病毒的逆转录酶可以实现“RNA→DNA”,也就是把病毒的RNA基因组,逆转录为DNA,再且永久地整合到宿主细胞的染色体上。结果就是,“天真无害”的人体细胞被改造成了病毒工厂,源源不断地在人体中生产病毒,导致疾病无法被完全治愈。这也就是为什么艾滋病如此可怕。
此外,HIV另外一个特征是病毒表面的糖蛋白,它像是病毒的导弹一样,能够精准地攻击人体的T淋巴细胞,最终导致人体免疫力下降。这也是为什么艾滋病被称为获得性免疫缺陷综合征(acquired immunodeficiency syndrome, AIDS)。
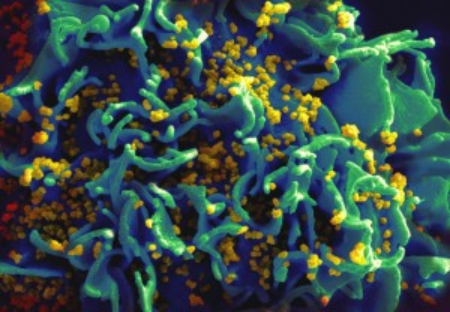
来源:https://www.nature.com/articles/nm0715-657
在研究艾滋病的过程中,HIV的逆转录活性引起了科学家们极大的兴趣。众所周知,几乎所有疾病的发生都和人类基因密切相关。比如血红蛋白基因突变会导致镰刀型贫血和地中海贫血是由于血红蛋白基因突变,而抑癌基因p53的突变则与超过50%恶性肿瘤的发生相关等等。另外,有超过50%的恶性肿瘤都发生了抑癌基因P53的突变,这导致细胞在DNA损伤之后不能正常凋亡。
针对这些疾病,目前的治疗方式,如手术、药物治疗等,尽管能够有效缓解疾病的症状,但却不能修复致病基因。因此,这些疗法在一定程度,就像噶韭菜一样,属于“治标不治本”。但如果我们可以在基因水平上“动刀”,将突变或缺失的基因重新修补回去,那就有望彻底治愈疾病了。
上述提到的HIV的逆转录酶具有将基因序列插入到宿主染色体中的能力,那是否可以通过逆转录酶来实现“基因治疗”呢?
为了实现这一目标,首先,科学家需要深入地研究了HIV的基因组,搞清楚哪些基因是对人类有益的,哪些是有害的。如下图示,HIV的基因组能够表达不同功能的蛋白质,共同组装形成完整的病毒颗粒。
![图源:HIV病毒的基因组结构<sup>[1]</sup><br>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_17_2245518652809249.png)
为了让HIV病毒“弃恶扬善”,我们要保留一部分具有重要功能、并且没有危害的基因,比如逆转录酶pol(实现“RNA→DNA”)、衣壳蛋白gag(病毒的核心蛋白,与RNA基因组结合)。
此外,我们要去除那些功能不重要,甚至对人体有害的基因,比如包膜蛋白env(帮助病毒攻击T细胞)、大部分辅助基因,如tat、nef、vif、vpr、vpu等(缺失后并不影响病毒复制)。
具体而言,研究人员需要采用基因工程的方法对HIV基因组进行改造。最常用的基因工程载体就是质粒。这是一种双链、环状、闭合的DNA分子,能够在细菌中扩增,具有稳定性强、操作方便的优点,因此广泛用于基因工程。
![图源:细菌结构<sup>[1]</sup>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_20_2245521279333885.png)
此外,为了让质粒表达病毒的蛋白质,我们还需要在质粒上游加入启动子(promoter),促进病毒基因在宿主细胞中进行高效地转录;并且以及在下游加入poly(A)信号能够来稳定mRNA分子,促进蛋白的翻译。
改造之后,病毒基因组被拆解为了三个质粒,分别含有病毒的核心、包膜、外源基因。它们各司其职,能够在宿主细胞中表达病毒的蛋白质,随后这些蛋白会再次组装,形成安全有效的重组HIV病毒颗粒,又称为慢病毒载体。
下面,我们分别介绍三种质粒的结构:
包装质粒:含有病毒包装需要的结构基因。为了减少质粒的长度,增加表达效率,科学家只保留了组成病毒核心结构的gag/pol,以及促进病毒组装的rev基因。包装质粒的数量可以为一个或二个。
![图源:包装质粒<sup>[1]</sup>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_20_2245521464742150.png)
包膜质粒:替换包膜糖蛋白,让HIV不再感染T细胞。为了降低HIV原本包膜蛋白的免疫毒性,研究者将其替换为了水疱性口炎病毒的包膜蛋白VSV-G,它能结合细胞膜上广泛表达的磷脂酰丝氨酸,因此重组HIV能够感染更多类型的宿主细胞,甚至包括那些不分裂的细胞,比如神经细胞。
![图源:包膜质粒<sup>[1]</sup>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_21_2245522154705310.png)
载体质粒:含有我们感兴趣的外源基因,以及HIV基因组两端的长末端重复序列(long terminal repeats, LTRs)。这是因为LTR上含有特殊的包装信号,使其能能够被其它病毒蛋白识别,最终被包裹在重组HIV的病毒颗粒中。而其它质粒,尽管能表达病毒蛋白,但它们转录的RNA上不含有LTR,因此就不会被包装进病毒颗粒中。
![图源:载体质粒<sup>[1]</sup>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_21_2245522637742747.png)
可以说,载体质粒是最关键的一个质粒。因为它让重组HIV的基因组中只含有外源基因的RNA,而不含有其它任何一种病毒蛋白。这就让重组HIV在感染细胞后,不能再产生新的子病毒。这种策略保障了慢病毒载体的安全性。
总结一下,研究者将HIV的基因组拆散,用三个质粒表达病毒蛋白。保留了病毒必需的基因,去除了HIV的毒性,并且赋予了它们表达其它基因的能力。最终获得了安全高效的重组HIV,又称为或者说慢病毒载体(Lentiviral Vector)。
那么,在获得质粒之后,我们怎么获得慢病毒颗粒呢?
答案是,我们需要将上述三种质粒导入到293T细胞中进行表达。293T细胞是一种含有SV40病毒T抗原的人肾上皮细胞系,能够使含有SV40病毒的复制起始位点的质粒进行复制,从而显著提高质粒的表达水平,因此被广泛用于蛋白表达、病毒包装。
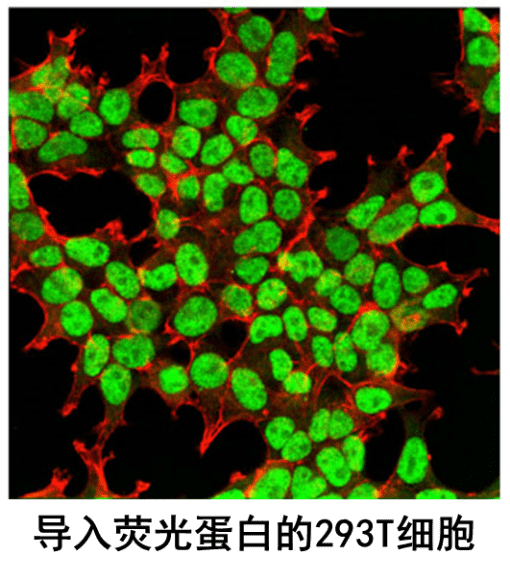
在导入质粒之后,包装质粒和包膜质粒将分别构成病毒的核心、外膜,而载体质粒表达含有包装信号的外源RNA,最初形成携带外源基因的慢病毒载体。
![图源:质粒导入病毒的过程<sup>[1]</sup>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_23_2245524287813159.png)
在用病毒感染靶细胞(target cell)后,病毒的逆转录酶会把RNA转变为DNA,使其永久地插入到宿主染色体中。靶细胞取决于研究者要对哪种细胞改造,常见的细胞有造血干细胞、T淋巴细胞。
在这个过程中,慢病毒载体在基因组上的插入位点是随机分布的,这可能会影响一些正常基因的功能。尽管目前没有临床证据支持这一点,但科学家们还是认为要关注慢病毒载体安全性是很有必要的的问题。
在获得慢病毒载体之后,人类终于打开了一扇“逆转录”的大门,这意味着科学家能直接改变细胞的基因组,改变有缺陷的基因,从而一劳永逸地治愈遗传性疾病。以地中海贫血为例,慢病毒可以将正常的β-珠蛋白基因序列送入造血干细胞中,从而彻底矫正贫血症状,该疗法已于2019年获欧盟批准上市。
![图源:基因治疗原理<sup>[1]</sup>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_25_2245526677674111.png)
除了导入正常的基因,科学家也可以导入全新的基因,比如嵌合抗原受体(Chimeric Antigen Receptor, CAR)。CAR能够靶向识别肿瘤细胞表面的受体蛋白,并且高效地激活T细胞。这就使得CAR-T细胞比T细胞具有更强的肿瘤识别和杀伤能力。
自2017年以来,美国FDA先后批准了5种CAR-T细胞疗法,用于治疗白血病、淋巴瘤和骨髓瘤。其中对于难治复发B细胞急性淋巴细胞白血病,CAR-T的治愈率惊人的达到了80%以上,这无疑是一次革命性的进步。
![图源:CAR-T疗法原理<sup>[2]</sup>](https://i.aiapi.me/h/2022/12/19/Dec_19_2022_01_38_27_2245528550353288.jpeg)
美国耶鲁大学学者卡尔·齐默在《病毒星球》一书中提到,我们生活的历史,其实就是一部病毒史。病毒不仅从未离我们远去,也永远不会离我们远去。
事实上,有学者推测地球上的病毒种类可能已经达到了8700万种,其中可能能感染人类的病毒就有73万种。然而,目前确认的已知病毒只有约5000种,其中能够感染人类的病毒仅有200多种。因此,可以将病毒说成是说生命科学研究中“暗物质”。
面对这些未知的病毒,我们不应陷入恐慌,更不能缴械投降。而是应该坚持科学理性的精神,深入的研究病毒的本质,开发治疗有效的治疗手段。
HIV病毒无疑是最危险的病毒之一,但经过数十年的发展,科学家们不仅开发出了有效的抗HIV药物,更是开发出了突破性的慢病毒载体,让“一劳永逸”的基因治疗成为了现实。我相信,随着新冠病毒的深入研究,未来也会有意想不到的突破等待着我们。
参考文献
1. Wang, X., Ma, C., Rodríguez Labrada, R., Qin, Z., Xu, T., He, Z., & Wei, Y. (2021). Recent advances in lentiviral vectors for gene therapy. Science China. Life sciences, 64(11), 1842–1857. https://doi.org/10.1007/s11427-021-1952-5
2. Naldini, L., Trono, D., & Verma, I. M. (2016). Lentiviral vectors, two decades later. Science (New York, N.Y.), 353(6304), 1101–1102. https://doi.org/10.1126/science.aah6192
3. https://viralzone.expasy.org/4976
4. https://proteopedia.org/wiki/index.php/Gp120
本文来自微信公众号:iSynBio造物 (ID:gh_1c7f920d8f21),作者:赵杭

