Nature Communications 最近报道了一项引人注目的研究,来自英国爱丁堡大学和伦敦帝国理工学院的研究团队,展现了基因编辑在保护鸡免受禽流感威胁方面的巨大潜力。
禽流感病毒在禽类中可长期自然传播、循环感染,同时该病毒还具有不断发生变异或重组的特性,这使得它有可能在人与哺乳动物中流行。目前,我们主要采取以下三种行动来遏制禽流感的传播:
1. 在农场和家禽价值链中实施严格的生物安全措施,并保持良好的卫生习惯,从源头上预防禽流感。
2. 加强对动物和人类的禽流感监测,及时发现并应对可能出现的疫情。
3. 快速报告、妥善应对禽流感,及时消灭受感染的鸟类,以防止疫情扩散。
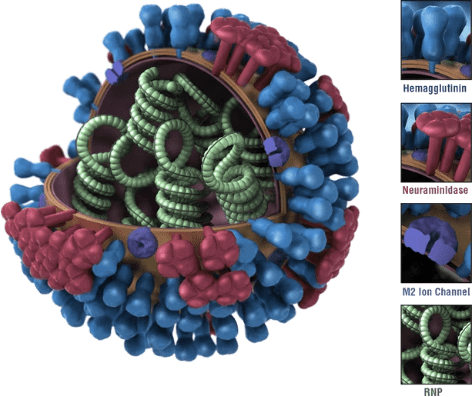
禽流感病毒属于甲型流感病毒(A型流感病毒),甲型流感病毒是变异最为频繁的病毒之一。甲型流感病毒是唯一已知会引起全球流感大流行的流感病毒,大部分已知的甲型流感病毒亚型都可以感染鸟类。
(图源:https://www.cdc.gov/flu/about/viruses/types.htm)
禽流感在全球范围内广泛传播,对野生鸟类造成了严重威胁,给家禽养殖者带来了巨大的经济损失,同时也给人类健康带来了风险。
然而,基因编辑技术的突破为阻止因禽流感爆发而遭受的巨大经济损失提供了新的可能性。这将是控制可能导致人类严重疾病和死亡的疾病的重要一步,为人类健康和经济发展带来了新的希望。
一、为什么管理禽流感很重要?
禽流感的全球爆发已造成了数十亿美元的经济损失。据美国农业部报告,仅2022年就有高达5000万只禽类因禽流感而死亡。近期,南非家禽协会也表示,自2023年上半年发现禽流感疫情后,已有超过700万只鸡被销毁。
然而,除了对全球经济的影响外,禽流感的爆发也对人类健康构成威胁。在COVID-19大流行之前,禽流感被认为有可能引发毁灭性的人类大流行,这促使世界动物卫生组织、世界卫生组织和联合国粮食及农业组织牵头开展国际监测。
这种担忧并非空穴来风,因为20世纪发生的三场流感大流行——1918年西班牙H1N1流感(约5000万人死亡),1957年亚洲H2N2流感(200万人死亡),1968年香港H3N2流感(100万人死亡)——都源于鸟类。这也意味着,源于鸟类的禽流感有可能最终引起人类群体的发病和流行。
二、疫苗能做的远远不够
有病毒?那打疫苗呗!确实,疫苗接种是预防鸡禽流感爆发的主要方法。
然而,由于禽流感病毒的快速进化,疫苗的有效性受到了限制。流感病毒的表面抗原极易变异,每隔十几年就会发生抗原性大变异,这意味着现有的流感疫苗每隔十几年就会失效。
同时,随着时间的推移,疫苗的有效性持续降低。此外,禽流感病毒存在多种毒株,但疫苗仅对特定毒株有效,无法一劳永逸地预防感染。因此,疫苗的使用与生产需要与引起疫情的流行菌株相匹配。
除了这些因素外,使用疫苗还可能面临大量的成本问题和分配方面的实际障碍。
三、基因编辑增强动物抗病能力
基因编辑是一种尖端的生物技术,它允许科学家对动物的特定基因进行精确的修改,从而引入诸如抵抗特定疾病、提高生产力和改善动物性状等有益特征。
与疫苗接种不同,基因编辑针对的是动物体内的一种或多种蛋白质,这些蛋白质对所有流感病毒株都至关重要,因此通过编辑这些蛋白质,可以有效阻止病毒的传播。
对鸡进行基因编辑,或许可以一劳永逸地解决禽流感病毒的感染与传播问题。同时这种基因编辑方法并不涉及将新的遗传物质引入鸡的DNA中,而只是对其进行一个小小的剪切。相对于转基因动物,这可能有助于通过基因伦理的调查。
通过基因编辑对动物的遗传信息进行修改已经在其他物种中得到实现。
例如,科学家利用基因编辑技术改变了奶牛的基因,成功地培育出了无角的奶牛。在传统的饲养过程中,为了降低奶牛相互攻击或伤害农民的风险,通常都会将它们的角去掉。然而,无角奶牛的诞生彻底改变了这一做法,逐渐淘汰了给幼牛去角的痛苦过程。
为了在研究中产生经过基因编辑的“抗流感鸡”,研究人员使用了强大的分子剪刀CRISPR/Cas9来对鸡进行基因组编辑。这次,这把分子剪刀的目标瞄准的是ANP32A蛋白的相关基因。
Why?为什么是这个蛋白?
这是因为禽流感病毒在宿主体内的细胞内复制依赖于宿主(禽类)蛋白ANP32A。科学家们通过利用CRISPR/Cas9分子剪刀精准地改变ANP32A蛋白内的两个氨基酸,成功地破坏了病毒的细胞内复制过程。
这样,经过基因编辑的这只鸡就具备了对禽流感病毒的抵抗力,病毒也无法进一步传播。
现在,研究人员已经得到了“基因编辑鸡”,接下来,研究人员将首先观察这只经过基因编辑的鸡与普通鸡是否存在差异。万一折寿你说咋整?
经过科学家的研究表明,这些经过基因编辑的鸡与同时孵化的正常鸡相比,在健康方面没有发现太大的差异。
接下来,科学家们肯定想要验证这只经过基因编辑的鸡是否真的能够抵抗禽流感。为了测试这只“战斗鸡”的抵抗力,科学家们决定将基因编辑鸡暴露于低剂量的禽流感病毒中。
实验结果令人欣喜:这些经过基因编辑的鸡中,十分之九表现出完全抵抗禽流感病毒的能力,并且没有将病毒传播给其他鸡。
研究人员采取了更为雄心勃勃的步骤,将经过基因编辑的鸡接种了高剂量的病毒。然而,结果出乎意料,这次实验中,10只接种的基因编辑鸡中有5只被感染。
这表明单一基因编辑可能不足以完全阻止病毒的传播,需要进行多种基因编辑来减少病毒逃逸的可能性。
除了上述发现,科学家们还注意到禽流感病毒能够适应使用经过编辑的ANP32A蛋白以及两种相关蛋白——ANP32B和ANP32E。
然而,通过细胞实验,科学家们证明了如果同时对这三种蛋白质进行基因编辑的话,可以完全抑制禽流感病毒的复制和传播。

野生母鸡(左)和编辑了ANP32A基因后生长的母鸡(右)。
四、下一步是什么?
未来,“战斗鸡”的路在何方?
确定创造下一代基因编辑鸡所需的基因编辑的特定组合,从而提供针对禽流感的完整和永久的保护。
基因编辑应被视为预防和控制致命动物疾病的重要工具。
需要支持性的政府法规旨在增强动物健康和福利的基因编辑的发展。
抗病动物保护全球粮食安全和公共健康的潜力是追求生物技术创新之路的一个令人信服的理由。
原文链接:https://phys.org/news/2023-11-bird-flu-eradicated-genes-chickens.html
更多论文相关信息:https://www.nature.com/articles/s41467-023-41476-3
本文来自微信公众号:iSynBio造物 (ID:gh_1c7f920d8f21),作者:未央,编辑:麦璇风

