本文来自微信公众号:iSynBio造物(ID:gh_1c7f920d8f21),主讲人:李雪飞,作者:捉蝴蝶的猫,编辑:果粒珍珍,原文标题:《李雪飞:果壳中的肿瘤》,题图来自:《我不是药神》
癌症最早记载于古埃及时期(乳腺癌),当时的人们对这种可怕的疾病束手无策,只能通过粗糙的治疗手段来延缓其发展进程。如今,1700多年过去了,人类对癌症的认识已经有了天翻地覆的变化,癌症的复杂性和多样性一次又一次地挑战着我们的认知。
近些年来,各种免疫疗法的发明标志着人类获得了对抗癌症的有力武器。在各种免疫治疗策略之中,最受瞩目的当属CAR-T疗法,这种疗法通过改造人体自身的免疫细胞,使其获得特异性杀伤癌细胞的能力,从而起到治疗作用。
然而,在实体瘤复杂的微环境面前,CAR-T疗法似乎也显得束手无策。随着研究的不断深入,我们开始意识到,肿瘤不只是由肿瘤细胞组成,肿瘤也从来都不是一种单一的疾病。下面,就让我们跟李雪飞老师一起,了解复杂的肿瘤系统以及免疫疗法的研究进展。
一、什么是肿瘤?
1. 肿瘤的主角之一:癌细胞是怎么来的
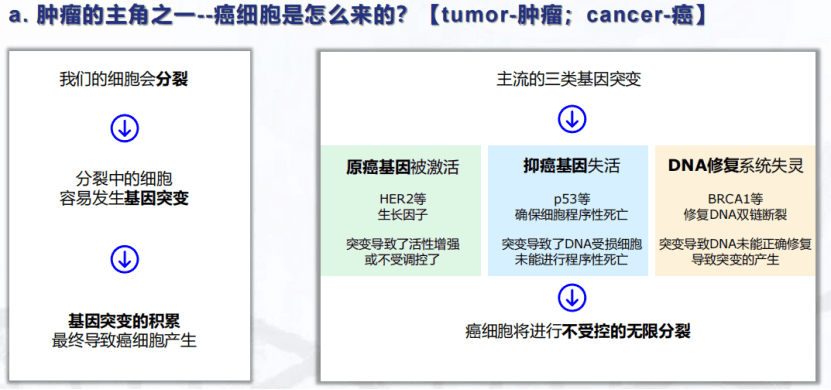
目前的一种观点认为,癌细胞的产生源于细胞分裂,分裂中的细胞非常容易发生基因突变,这种基因突变的积累最终导致了癌细胞的产生。在发生突变的基因之中,有三类基因尤其受到关注。
首先是原癌基因,很多名字中带生长因子的基因都属于这类基因,这些基因在正常细胞中的表达量是比较低的,是可控的,但如果这些基因出于某些原因被激活了,他们的活性就会增强,就不受调控了,最终会驱动癌细胞的产生。
第二类基因是抑癌基因,这类基因的失活也会导致癌细胞产生,在抑癌基因中最著名的要数p53基因,其能确保细胞发生程序性死亡,这样当细胞因某些情况发生损伤时,就能及时被机体清除干净。
因此,这类基因的失活也会导致癌细胞产生。关于p53基因还有很有意思的一个点是,大象的细胞中有很多个拷贝的p53基因,这样,即使一个拷贝发生突变,还有其它个拷贝能发挥正常功能,因此人们猜测,p53基因的多拷贝可能是大象很少会得癌症的原因之一。
第三类基因是DNA修复相关的一些基因,其中比较有代表性的要数BRCA1基因,这个基因负责DNA的保真性修复(阻止更多突变的发生),所以如果检测到这个基因发生了突变,那么产生癌细胞的几率就会大大升高。美国著名演员安吉丽娜朱莉曾进行过相应的检测,结果表明其BRCA1基因存在突变,根据统计分析结果,她患上乳腺癌的几率可能高达80%。
2. 肿瘤/癌症发展的阶段
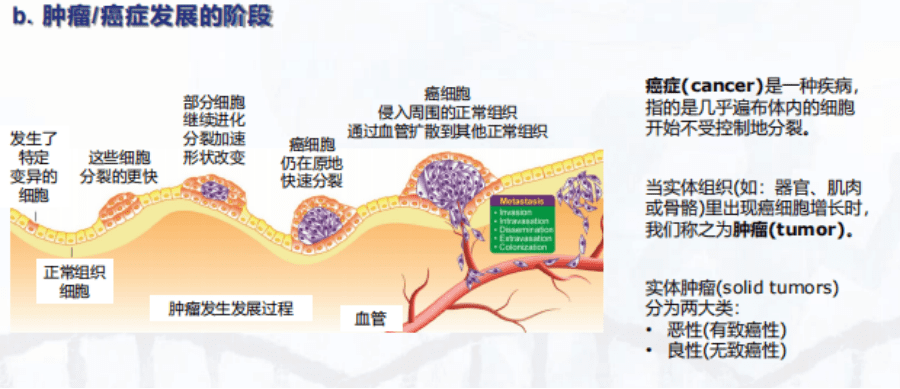
我们讲的第二个问题是癌症发生发展的阶段有哪些。我们人体食道、口腔上皮以及肠道都有很多上皮细胞,这些上皮细胞的癌症大约占到所有癌症类型的80%。我们今天就以这个例子为大家介绍一下上皮细胞的突变以及癌变的整个过程。
第一个过程是正常组织细胞发生特定的基因变异(包括上面提到的三类基因),这些突变会积累,积累到一定阶段以后,出于某些原因,这些细胞可能会分裂的更快(比如上面提到的一些生长因子基因突变后细胞分裂的过程会加快),那么它们在分裂时就很容易积累更多突变,这些细胞继续演化,分裂加速,并且形状也会发生一些改变。
这些细胞在原地一直维持快速分裂、突变、演化,形成息肉或肿瘤样的结构,一旦突破到某个临界点,这些细胞就不只是待在原地了,当癌细胞突破基底膜结构后,它们就可能通过血管扩散到身体上其它正常组织处。
那么这些细胞能不能在其它组织或器官中定植下来呢,当然是不一定的,这是一个撞运气的过程,但是一旦癌细胞在其它部位定植下来,就会发生一些不可逆转的症状。
对于癌症(cancer)和肿瘤(tumor)这两个词,很多人可能会有些迷惑,其实说到癌症的话,它指的应该是一种或一类疾病,指的是体内的细胞开始不受控制地分裂。那么当实体组织里面出现癌细胞增长时,我们就将它称为肿瘤。而实体肿瘤又分为两大类:良性和恶性的。
二、关于肿瘤/癌症的若干冷知识
1.癌症(Cancer)这个词来源于拉丁文的词汇“螃蟹”(Crab),因为当时观察的时候发现肿瘤会长出很多分支,长的有点像螃蟹。
2.最早关于癌症的描述可以追溯到公元前1600年左右的埃及,下面这张图中画得是切割出来的一个肿瘤。
3. 癌症如果去细分的话可以分出多达200余种,所以说癌症不是一种疾病,而是一类疾病的统称。
4.非洲裸鼹鼠体内(包括血液里)有一种特定的玻尿酸,这种玻尿酸可能让癌细胞无法粘附在组织上面,从而无法形成肿瘤。
5.目前的研究表明大约只有5~10%的癌症是可遗传突变造成的,但是更多的其实是跟环境相关的。
6.按照目前的统计数据,如果人的寿命足够长,每3位女性中就有1人会罹患癌症,而每2位男性中,则会有1人罹患癌症。
7.现有的超过一半的癌症是可以预防的,有效预防有望每年减少300万左右的患者。比如说吸烟,根据其它国家的一些统计,戒烟确实是可以降低一些癌症的发生的。
三、从科研的角度看肿瘤
这一部分主要是围绕两篇文章进行介绍,首先第一篇文章是Douglas Hanahan和Robert A. Weinberg写的题为癌症的特征1.0(Hallmarks of Cancer 1.0),这篇文章是2000年发表的。这篇文章的引用率现在已经超过了5万次了,也说明这篇文章的影响力是非常大的。
接下来我们也会就这其中的几个点进行介绍,在此之前,需要强调的一个点是,肿瘤不只是有肿瘤细胞在里面,它其实是一个很复杂的系统,里面有很多不同细胞、不同的组织结构以及各种细胞因子。
大概在3年前,我从国外的一位临床医生那里听到,他们切出来的胰腺癌的肿瘤组织可以硬的像石头一样,很难想象,我们身体里面除了骨骼外还能长出这么坚硬的组织,实际上原因就是里面有很多的成纤维细胞,这些成纤维细胞产生了很多的胶原蛋白,这些胶原蛋白层层叠加,最终让肿瘤组织长的像石头一样坚硬。
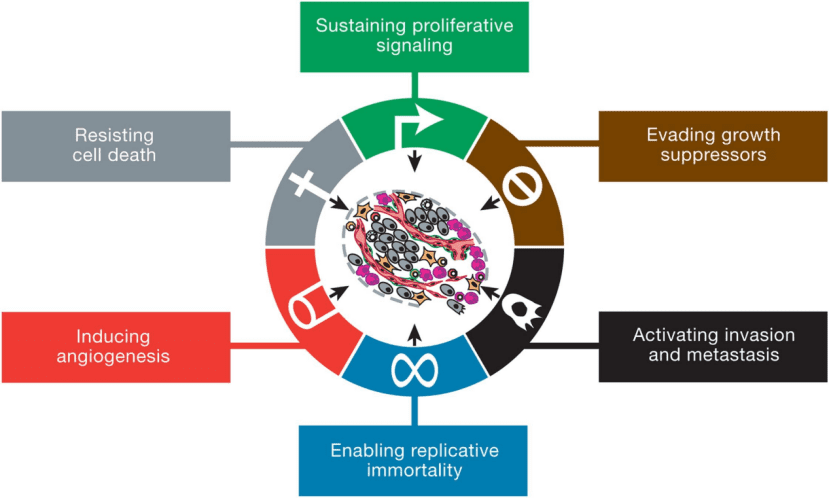
1. 癌症的特征
从生物的角度来讲,其实癌症的每种特征都是复杂的分子相互作用网络的产物,每种蛋白之间的相互作用最终会形成一个网络,如果网络中的某些关键的网络节点出现了错误就会导致网络功能的灾变。
为什么几个节点的变化就会导致整体网络的灾变呢,我们举个例子,意大利的电网已经建设了几十年,期间也没有出现过什么差错,但是某天一个小小的变电站出现了故障,结果在接下来几天里就导致了整个意大利的电网的瘫痪。
这个例子就是告诉大家,当一个网络很复杂,并且我们对网络结构的了解还不深入的时候,可能一个小小的节点发生错误,整个网络就可能会发生混乱。所以当我们了解了一些原因之后,我们就要想办法去避免这些问题。
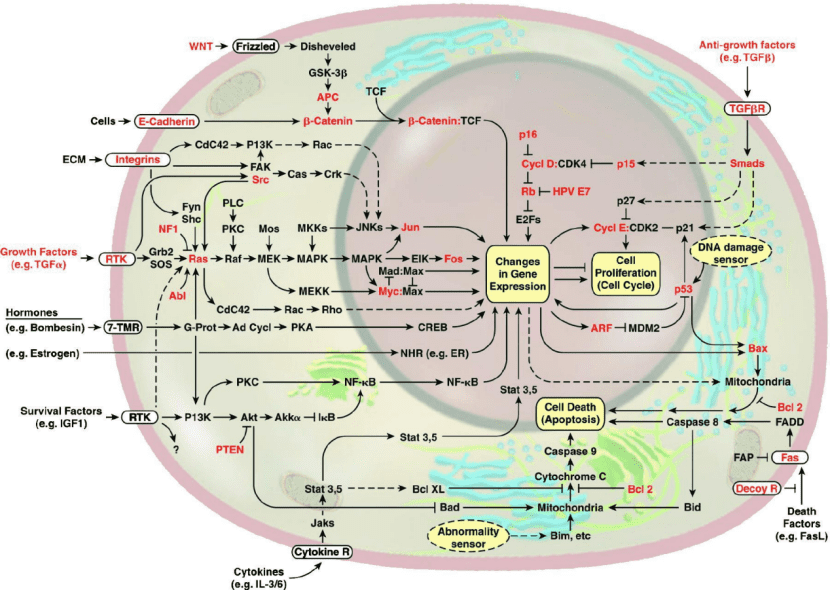
我们接着介绍癌症的这些特征。首先这几点其实是比较接近的,都跟细胞的死亡或增殖相关,我们就放一起介绍。
需要注意的是,这个领域还是持续不断向前发展的,并不是说我们已经了解了关于癌症的所有东西,所以说,各种癌细胞抵抗死亡的策略现在还是不断被发现的,而针对一些特定的生长相关的通路进行抑制的话,就可以开发一些靶向的药物。
比如说我们前面提到的HER2和EGFR,其中HER2主要是乳腺癌细胞里面高表达的,而EGFR的话有很多种,这两种都是生长因子,它们在细胞里面的表达量太高了,那么我们就可以使用一些药物把细胞里面这些蛋白的浓度降下来,或者降低它们的活性,这样就可以抑制癌细胞的生长,在这些方面,已经有一些药物被成功开发出来了。
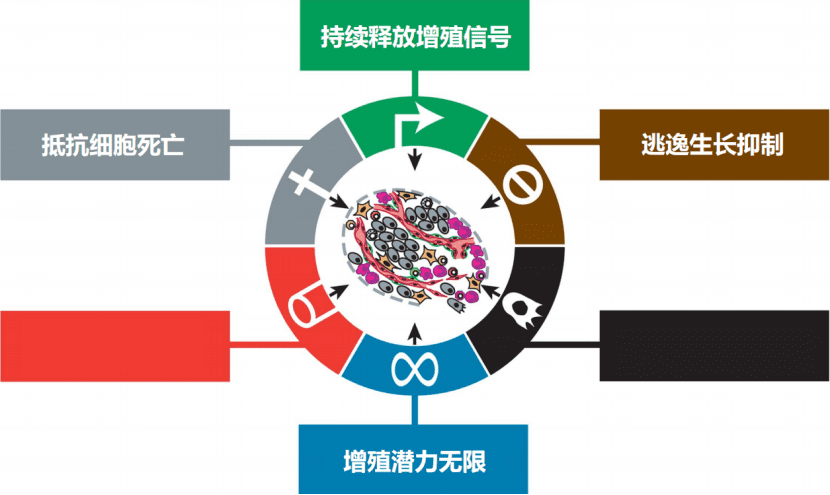
第二个方面是肿瘤可以促进血管增生。有这样一种说法:癌症其实是一种永远无法被治愈的伤口,在伤口愈合的过程中就有很多血管增生的现象,通过这些增生血管,肿瘤细胞能够不断的获得营养物质。
目前研究人员也在尝试开发一些靶向药物,来抑制血管生成,从而饿死癌细胞。这个想法听上去虽然很有趣,但是目前的研发进展还不是太乐观。
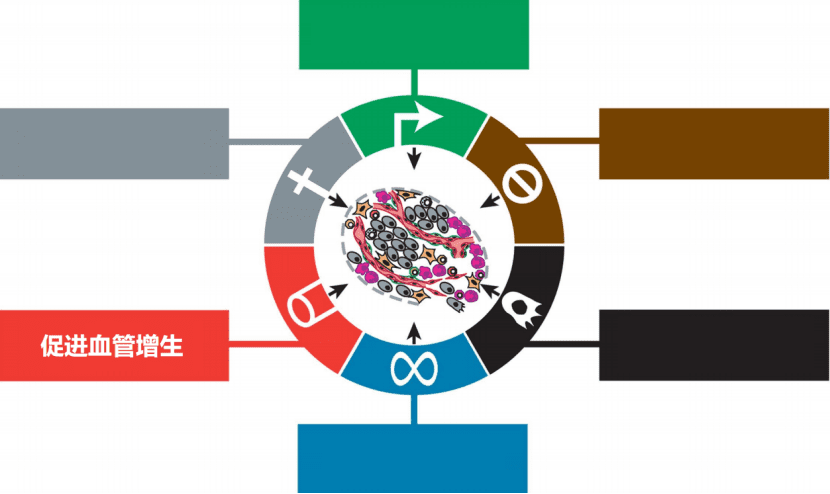
另外,肿瘤转移也是一个很重要的问题。据统计,肿瘤转移导致了67-90%的癌症患者的死亡。所以说弄清楚,肿瘤为什么转移,什么时候转移,对于癌症治疗是非常有用的。在这个方向,很多新的概念也是在不断的涌现出来。
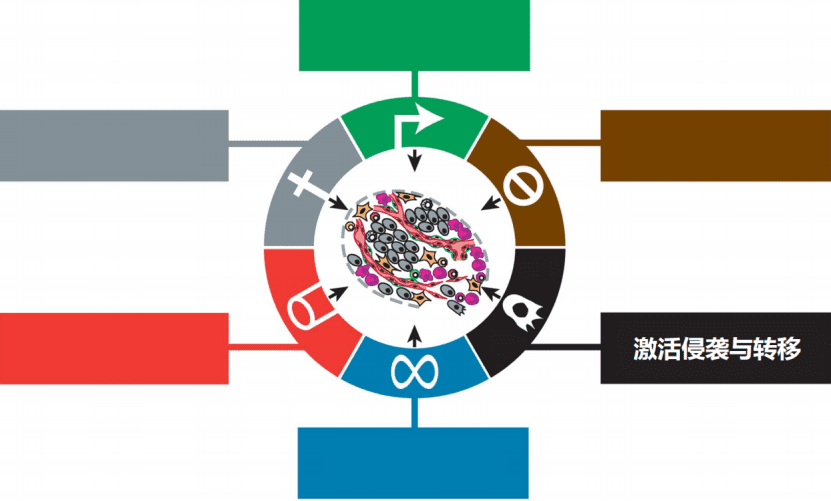
在癌症的特征1.0发表后11年,这两名科学家又发表了癌症的特征2.0(Hallmarks of Cancer 2.0),在原先的版本上,又添加了一些对肿瘤特征新的理解。
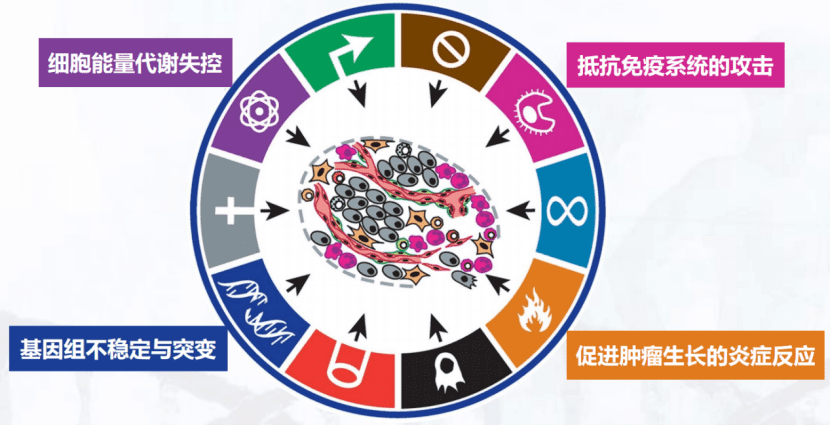
首先是细胞能量代谢的失控,肿瘤细胞很有意思的一个点是它生长的时候消耗的氧气量可以是很低的,这个现象叫做Warburg Effect。另外,肿瘤细胞也可以产生很多的乳酸,这些乳酸能够抑制免疫细胞的活性。最后,很多研究也发现,癌细胞可以“吃”很多种东西(可利用的能量来源多样),而不像我们大脑的脑细胞,它只能“吃”葡萄糖。
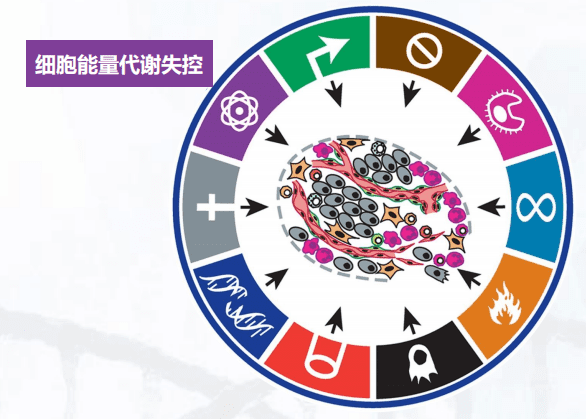
我们知道人体细胞有23对染色体,但是癌细胞经常会出现染色体的缺失,以及某些特定染色体的倍增,而染色体的倍增相应的也会导致它上面的基因的表达水平升高。
另外,在存在选择压力的情况下,癌细胞的突变率可以变得特别高,大概在10-3到10-6,大家可能觉得这个数字已经很小了,但正常细胞的突变率只有10-12。
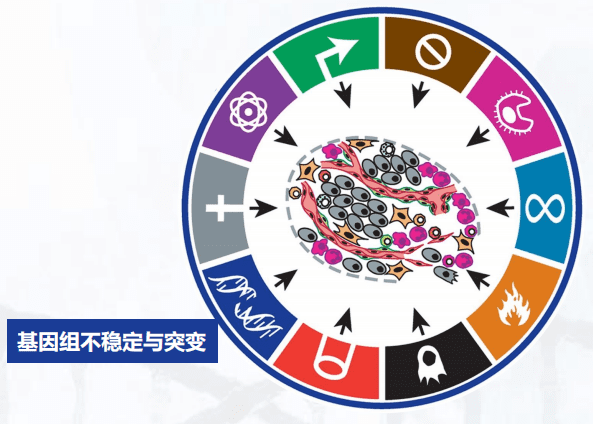
关于免疫的内容暂时跳过,后面会进行仔细讲解。
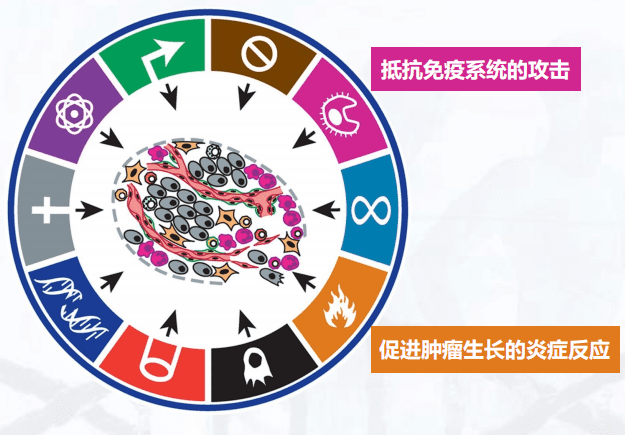
2. 肿瘤微环境
这部分前面我们已经提到,肿瘤里面不只有肿瘤细胞,还有很多其它类型的细胞。最近十年左右提出了肿瘤微环境这样一个概念,说的就是这样一种现象。
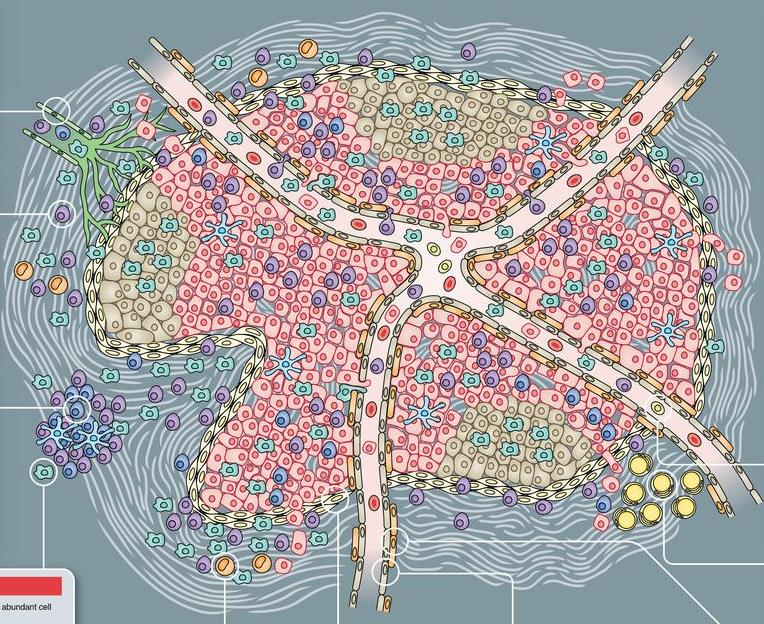
四、肿瘤的治疗策略
这一部分我们对肿瘤治疗的一些策略进行简单介绍。
1. 基本分类
手术疗法:切除可发现的肿瘤,但是发生大面积转移后无法进行手术。
化学疗法:主要是通过抑制DNA的复制或是阻止染色体分离。这种方法毒性大,且癌细胞通过进化会产生抗药性。
放射疗法:使用辐射线,包括X射线或者质子束破坏细胞的遗传物质,毒性大,癌细胞会通过扩散逃逸治疗位点。
靶向疗法:利用分子靶向药物特异性阻断靶点的生物学功能(比如抑制一些生长因子),这种疗法的副作用会小一点,但是很明显的一个问题就是一个药用几年之后,如果没有将癌细胞都杀死,癌细胞就会通过进化产生抗药性。
免疫疗法:近些年,尤其是2010年之后,很多新兴的免疫疗法的机制被发现,具体治疗的方法也在不断被更新,但是这种疗法的一个特点就是它的响应率其实不高,而且很多原理也还不完全清楚。
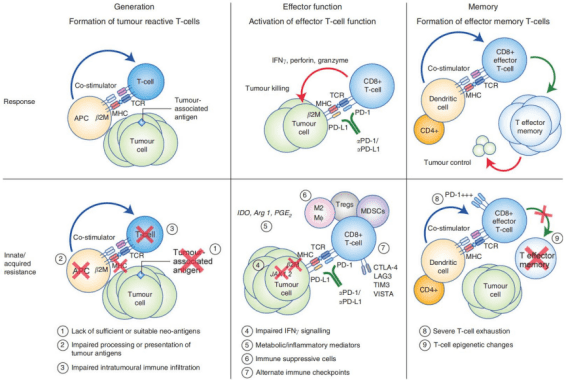
2. 免疫检查点抑制剂疗法——原理
最近几年特别火的一种疗法是免疫检查点抑制剂疗法,简单来说,这种疗法的原理就是把免疫细胞的刹车片去掉。由于各种各样的原因,免疫细胞在肿瘤微环境里面其实是“踩了很重的刹车”的。最有名的两个药物针对的其实就是CTLA-4以及PD1/PD-L1这两个靶点。
实际上,肿瘤细胞通过结合免疫细胞上的这两个靶点,使其功能失活(也就是“踩了刹车”),那我们做的自然就是开发一些抗体,把这些“刹车片”给拿掉,这样,免疫细胞就能发挥它的正常功能。
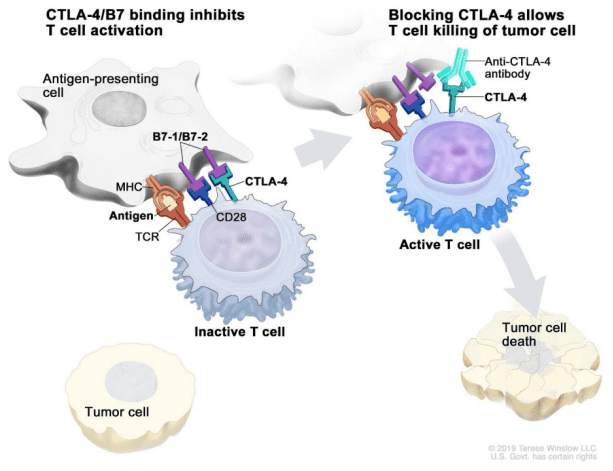
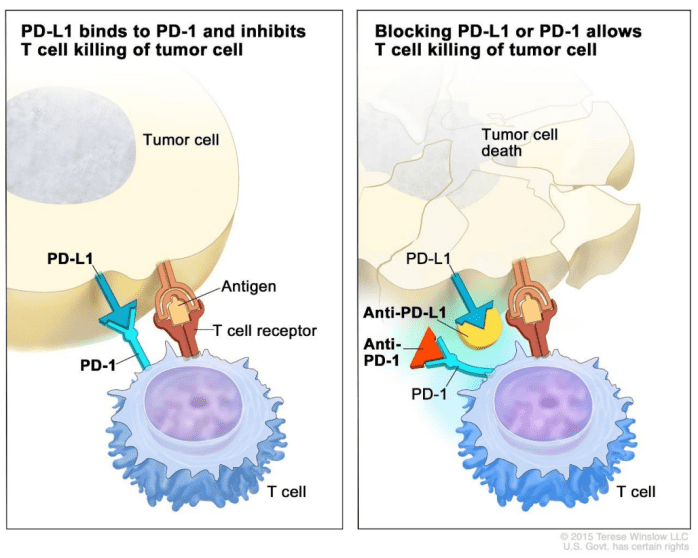
3. 免疫检查点抑制剂疗法——优势
免疫检查点抑制剂疗法有很强的优势,对于晚期的皮肤癌以及晚期的非小细胞肺癌,如果采用常规疗法,患者的存活期大概只有几年。但是经过免疫治疗之后,大约有20%左右的患者可以实现十年以上的生存,且没有表现出任何癌症的迹象。
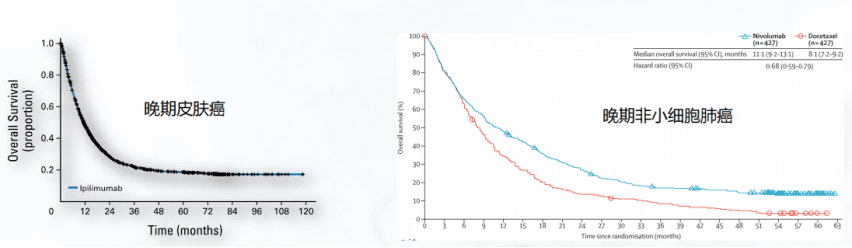
4. 免疫检查点抑制剂疗法——挑战
首先就是响应率低的问题,上面提到的20%已经是最理想的情况,对于绝大多数的癌症类型,响应率只有1%,甚至低于1%。响应率低的原因目前还没有太清楚的解释。
另外,这种疗法也存在一些副作用,比如可能会导致一些自身免疫疾病的产生。最后,其实使用这种疗法,癌细胞也会演化出耐药性。
五、肿瘤治疗与合成生物学
1. CAR-T疗法
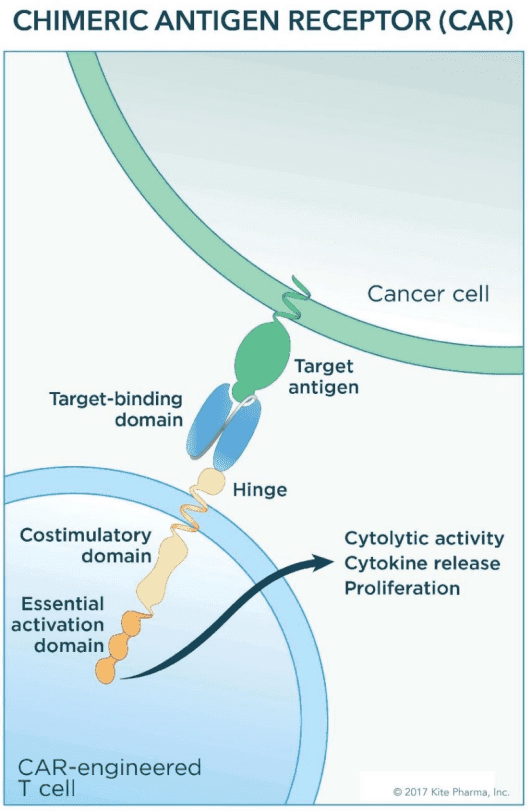
CAR-T疗法的中文名叫做嵌合抗原受体T细胞疗法。癌细胞与免疫细胞(比如T细胞)之间常会出现一些蛋白的配对,比如肿瘤细胞的细胞膜上经常存在一些特异的分子(在这里我们形象的把它们比成钥匙),这个时候,如果我们在T细胞上安上一把“锁”,这样“锁”和“钥匙”分子结合,就会产生一些信号,从而告诉T细胞去执行它的功能(杀伤癌细胞)。
关于这种疗法最有名的一个例子就是美国的一名血液癌患者在经过CAR-T治疗后一直活到了现在,且未表现出癌症症状。为了设计好这把“锁”(从而实现特异性的识别与攻击),就需要对合成策略与工艺进行不断更新。目前国内的很多公司和科研单位也在进行相关的工作。
但是这种方法存在的一个问题就是容易引起细胞因子风暴(有点类似败血症,免疫系统疯狂攻击导致正常器官衰竭)。另一方面,CAR-T疗法对于实体肿瘤的治疗效果也欠佳且原因不明。另外,癌细胞也能通过突变把这些“钥匙分子”隐藏起来。
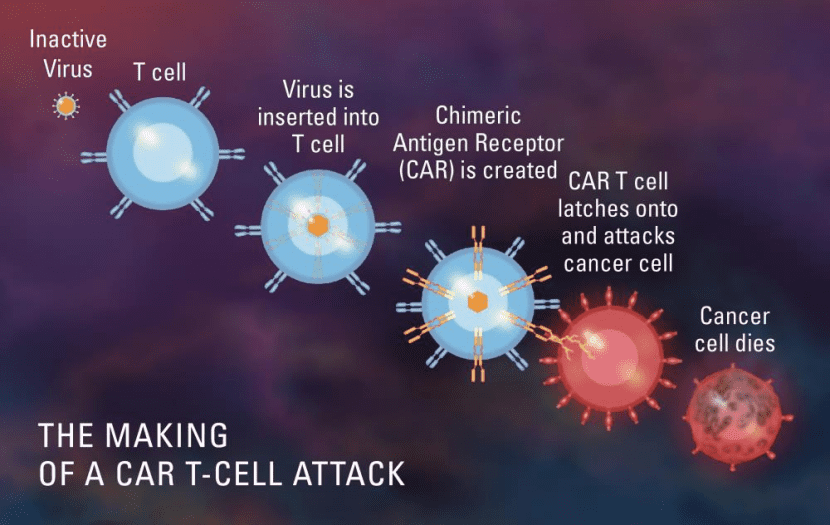
那么,合成生物学对CAR-T疗法的实现起到了哪些作用呢。我们在构建CAR-T细胞时需要使用某些病毒去把这些“锁”的基因插入到免疫细胞身上,这样,免疫细胞通过表达这些基因就能产生出“锁”蛋白。
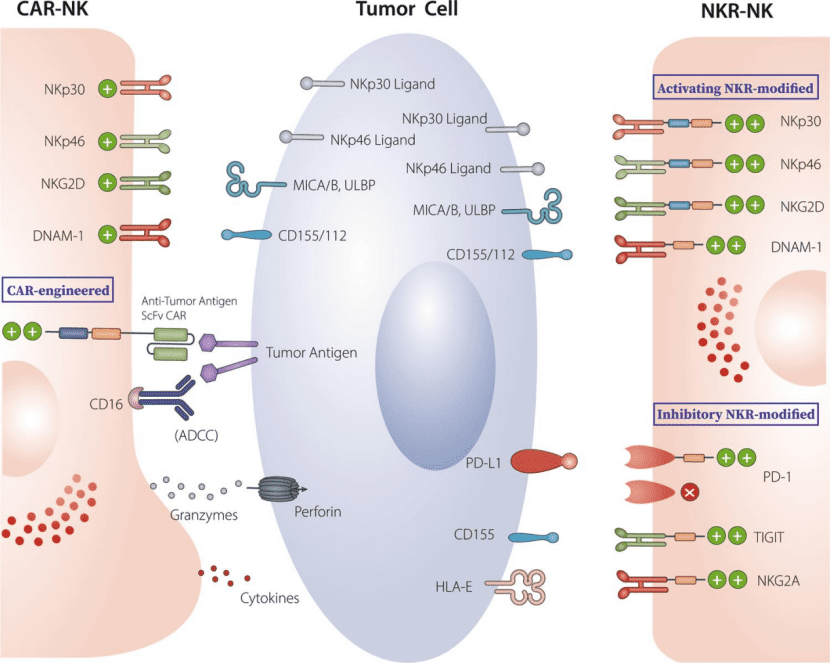
2. 合成自然杀伤细胞疗法
除了上面提到的T细胞,还有另一类免疫细胞叫做自然杀伤细胞(NK细胞),这类细胞与固有免疫相关,合成自然杀伤细胞疗法也存在着一些优缺点,这里就不展开进行介绍了。
3. 肿瘤疫苗(基本原理)
与流感等其它疾病的疫苗不同,肿瘤疫苗不仅可以起到预防作用,还能起到治疗作用。关于肿瘤疫苗最关键的一类细胞是树突细胞,树突细胞能发挥很多方面的作用,其中最关键的就是它能吞噬很多肿瘤的抗原,然后将它们加工后放到细胞表面。然后树突细胞与T细胞“握手”就能够招募或者激活T细胞。
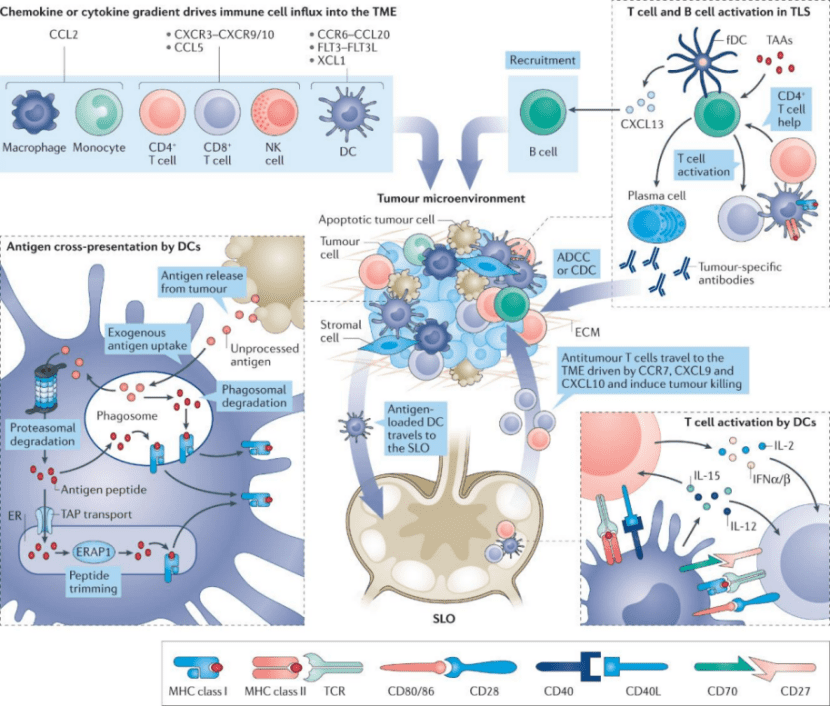
4. 肿瘤疫苗(合成方法)
关于树突细胞的编辑方法非常的多种多样,最近比较火的mRNA疫苗就是通过将mRNA导入到树突状细胞里面,让它能够表达相应的蛋白。
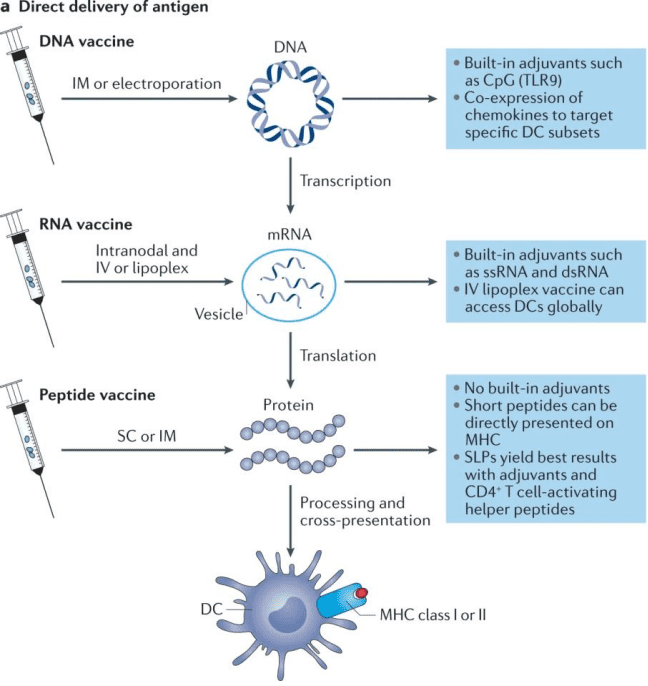
另外比较有趣的一点是,我们现在可以利用患者自身的细胞进行分化,从而培养树突细胞,这样就能减少很多的免疫排斥反应。
主讲人简介:李雪飞,博士,副研究员。研究领域主要包括,生物数据的定量与自动化分析,以及从定量生物数据出发,进行数理模型的构建与分析。研究课题主要围绕肿瘤微环境中的生物学和物理学。主要代表性工作之一是通过定量分析肿瘤切片图像数据,刻画淋巴毒性T细胞在肿瘤中的空间分布,并根据定量数据,构建了合理的数学物理模型以解释分布机理,从而为提升免疫治疗效果提供了理论指导。另外,通过构建合理的物理模型,揭示了肿瘤内成纤维细胞环绕肿瘤规则排列的机制,为扫除限制药物、免疫细胞浸润的物理屏障提供了理论指导。个人网址:http://isynbio.siat.ac.cn/Li(x)lab/
视频链接:http://www.isynbio-talk.cn/#/video/video-info/329
本文来自微信公众号:iSynBio造物(ID:gh_1c7f920d8f21),主讲人:李雪飞,作者:捉蝴蝶的猫,编辑:果粒珍珍

