阿尔茨海默病(AD)是在老年人中常见的一种神经退行性疾病,伴随认知障碍、记忆失衡和行为异常等症状。随着世界人口的老龄化,这种疾病给患者、他们的家庭和社会都带来沉重的负担。
据世界卫生组织估计,全球至少有5000万人患有阿尔茨海默病。流行病学调查还表明,阿尔茨海默病患者中,女性数量为男性患者的2倍。而且女性患AD的终生风险高于男性,疾病进展率大约高出3倍。
为什么女性比男性更容易罹患阿尔茨海默病?对于这一令人困惑的现象,很多科学家曾给出了各种可能的理由。比如有人认为睡眠不足、长期压力等,可能是女性AD高发的原因;也有人提出,携带特定风险基因的女性患上AD的风险更高;还有人认为,跟女性绝经之后激素降低有关。
今日,一篇发表在顶尖学术期刊《自然》上的研究论文给出了一种新的解释。由中国科学院深圳先进技术研究院脑认知与脑疾病研究所研究员、中国科学院深圳理工大学(筹)叶克强教授领衔的研究团队与美国纽约西奈山医学院Mone Zaidi教授合作,首次揭示卵泡刺激素(Follicle-Stimulating-Hormone,FSH)的增高是女性比男性更容易罹患阿尔茨海默病的重要原因。

女性在绝经前后,体内有多种激素的浓度发生了急剧变化。卵泡刺激素就是其中一种核心激素。这是由腺垂体分泌的一种促性腺激素,在女性和男性体内都有,分别促进卵巢和睾丸产生配子。女性在围绝经期,卵泡刺激素的体内含量急剧升高至10倍以上;相比之下,同年龄段老年男性体内,卵泡刺激素的水平仅增高2~3倍。
研究团队发现,急剧增高的卵泡刺激素可以直接作用于大脑的海马神经元与皮质神经元,选择性激活一条信号通路:C/EBPβ/AEP。而该团队先前的工作指出,这条分子信号通路正是导致阿尔茨海默病等神经退行性疾病的核心推动因素。
这条分子通路通过转录因子C/EBPβ激活δ-分泌酶AEP,促进淀粉样前体蛋白(APP)切割,进而引发Aβ增加,Tau蛋白聚集,而这些变化正是阿尔茨海默病的典型病理现象。
为了验证卵泡刺激素通过影响C/EBPβ/AEP通路进而影响阿尔茨海默病的产生,研究团队通过小鼠模型从四个不同角度和方式展开了实验。
研究人员给阿尔茨海默病小鼠模型注射外源卵泡刺激素,发现无论雄性还是雌性小鼠,都会因此加速形成相关的病理改变。相反,在切除卵巢以模拟绝经的雌性AD小鼠中,用抗体阻断卵泡刺激素的作用,可以降低病理改变,而且小鼠的认知水平也得到一定程度的恢复。
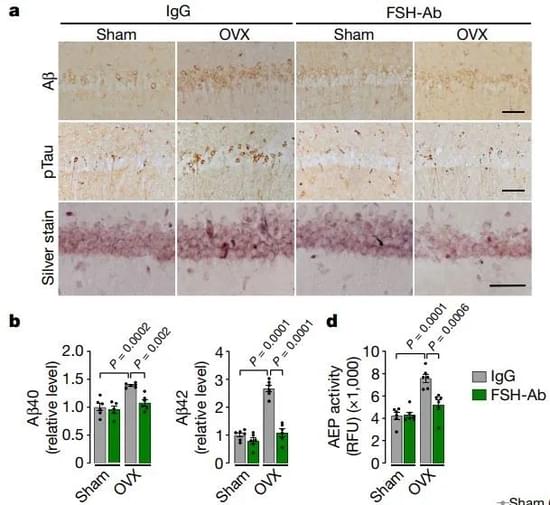
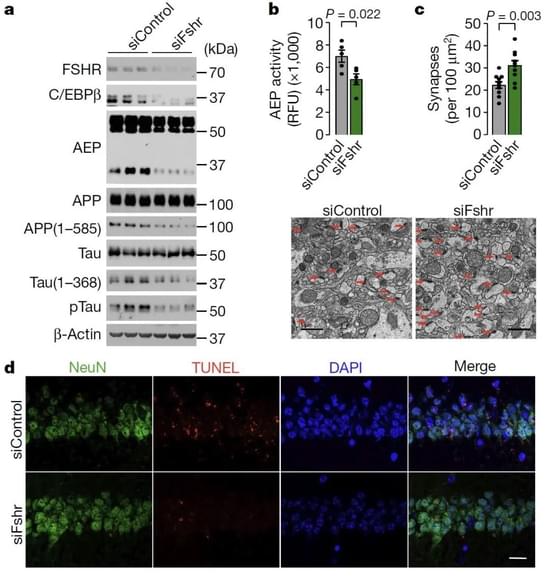
类似的,将阿尔茨海默病模型小鼠神经元中的卵泡刺激素受体敲除,或是敲除C/EBPβ,使C/EBPβ/AEP通路无法被激活,都可以让摘除卵巢后的小鼠病理症状减轻,并加强了记忆的恢复。
综合这些结果,围绕卵泡刺激素这一关键因素,研究团队从多个环节证实,卵泡刺激素通过C/EBPβ/AEP通路导致了阿尔兹海默症相关病理的改变,进一步揭示了女性阿尔兹海默症发病率高于男性的具体机制。
文章共同第一作者熊婧博士,现任武汉大学人民医院神经内科副主任医师,从事AD和帕金森病(PD)发病机制的研究和诊治。她表示:“女性月经期间,雌性激素升高,并通过大脑调控抑制卵泡刺激素的增高,以此循环。随着年龄的增长,卵巢功能衰退,女性绝经后,雌性激素减少,卵泡刺激素便不再受到抑制,进而导致女性更易患阿尔兹海默症。”
研究团队表示,在发现了卵泡刺激素这一重要的致病性因素后,下一步还将针对特定风险基因如ApoE4与卵泡刺激素的关系进行机制层面的深入研究, 以解释为什么ApoE4 女性携带者更容易患病。
华中科技大学同济医学院病理生理学系教授王建枝评论说:“这一重要发现不但为解答女性为何更易罹患阿尔茨海默病提供了新病因和新机制,也为临床早期筛查和干预阿尔兹海默症提供了新分子靶点。”
论文通讯作者叶克强教授介绍,针对卵泡刺激素的特异性抗体正在临床前研究,以期不久实现对阿尔茨海默病的全新治疗策略。
面对更高的患病风险,女性又该如何降低阿尔兹海默症的发生?对此,叶教授表示,均衡饮食,保持乐观心态,避免压力过大,合理锻炼,保障充足睡眠时间和质量,可有助于降低体内炎症,延缓绝经期的到来,在一定程度上可延后疾病的发生。

