根据来自威尔康奈尔医学院和冷泉港实验室的研究人员展开的一项临床前研究显示,一种已经在临床上获FDA批准、已经使用了70多年的药物可能会保护严重的COVID-19和其他对肺部造成免疫介导的损伤的疾病的肺部损伤和血栓风险。
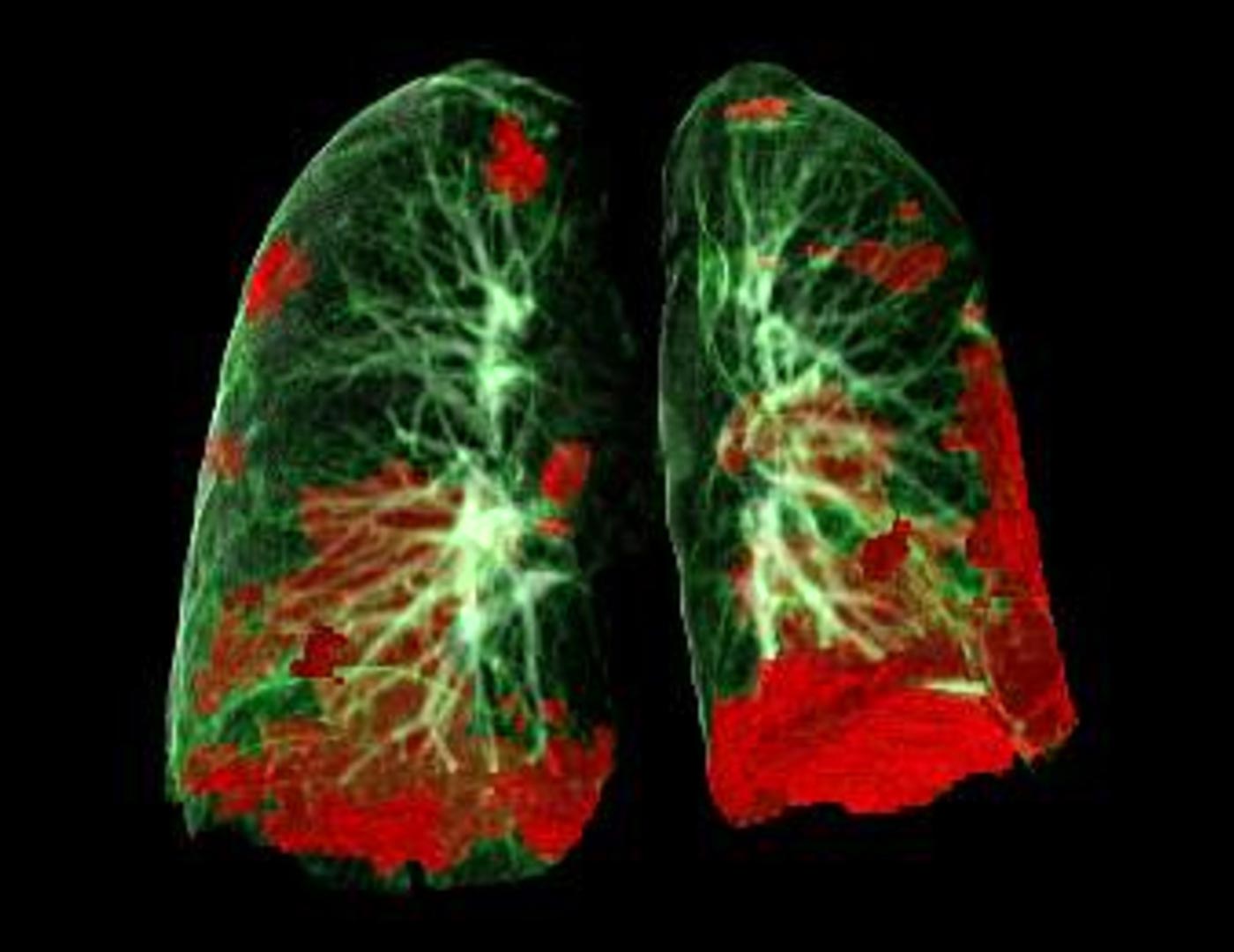
研究人员的报告于2022年2月8日发表在《JCI Insight》上,他们发现药物双硫醒(disulfiram)在两种不同类型的损伤模型中保护啮齿动物免受免疫介导的肺部损伤:感染导致COVID-19的SARS-CoV-2新冠病毒以及在罕见情况下输血后发生的称为TRALI的肺衰竭综合症。
这项研究的论文高级合著者Robert Schwartz博士说道:“随着我们对这些肺部损伤的基础生物学有了更多的了解,我们也许能够专门针对损害肺部组织的过程。”
现在已知这两种类型的肺部损伤部分是由免疫细胞形成的网状结构驱动的,这种结构被称为中性粒细胞胞外陷阱(NETs)。这些结构可以捕获并杀死感染性有机体,但也可能对肺组织和血管造成伤害、导致肺部积水(水肿)并促进血栓的形成。双硫醒可阻断NETs形成的其中一个步骤。
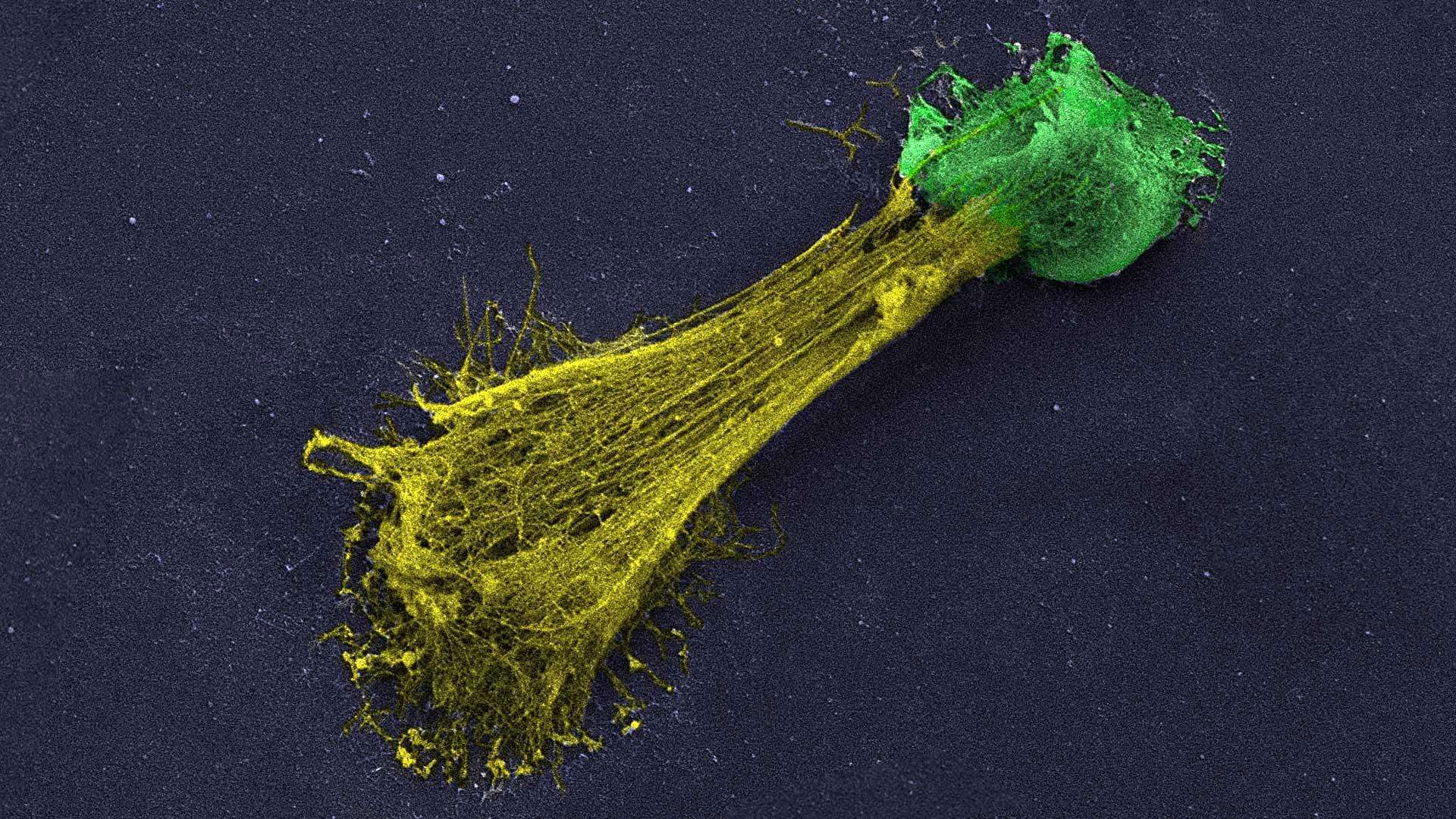
这项研究是Schwartz博士的研究小组跟冷泉港实验室的教授和癌症中心联合负责人Mikala Egeblad博士领导的小组之间的合作。
偶然性几乎从双硫醒作为药物的历史开始就伴随着它。这种化合物最初被用于生产橡胶,后来被研究为一种抗寄生虫治疗。在偶然的观察中发现,服用这种药物的人只要一喝酒就会出现轻微的不适,这使得FDA在1951年批准将其作为酒精使用障碍患者的一种威慑性消费。
科学家们在2020年发现,双硫醒还能抑制部分炎症过程,该过程可能会导致被称为中性粒细胞的白血球形成NET。这一发现促使人们将双硫醒作为一种NET阻断剂进行测试。Egeblad博士说道:“虽然NETs会损害组织,但由于双硫醒干扰了产生NETs所需的分子galdermin D,因此在双硫醒治疗后不会形成NETs。”
双硫醒在实验中确实大大减少了人类和小鼠中性粒细胞形成的NETs。之后,研究人员在TRALI和COVID-19的模型中对其进行了测试,这两种疾病的特点是中性粒细胞广泛入侵肺部、形成NET并常常会造成致命的肺部损伤。
在TRALI的小鼠模型中,在诱导综合征的前一天和前三小时进行的双硫醒治疗使95%的动物得以存活,而没有用这种药物治疗的动物只有40%。研究结果表明,双硫醒显然是通过减少NET的形成、阻止了未接受治疗的小鼠发生的肺组织和血管的渐进性损伤并以此使肺功能稳定下来,另外在最初的损伤后相对迅速地恢复。相比之下,一种名为DNase 1的吸入性药物被研究为潜在的TRALI治疗方法,即使在TRALI诱导前几分钟给药也没有改善小鼠存活率的显著效果。
在《Journal of Experimental Medicine》上发表的早期合作工作中,尸检结果表明,NETs存在于严重的COVID-19患者中并提出了一种新的可能性。
Schwartz博士说道:“目前对于COVID相关的肺部损伤还没有任何好的治疗方案,因此在这方面,特别是在严重的COVID-19患者中,双硫醒似乎值得进一步研究。”
接下来,研究人员在金仓鼠的COVID-19模型中测试了双硫醒。这种形式的COVID-19没有最严重的人类病例那么严重,但在感染SARS-CoV-2的前一天或后一天进行的双硫醒治疗明显导致了有利的结果:较少的NET形成、较少的肺部疤痕组织形成(纤维化)以及基因活动的变化表明有害的炎症反应明显减少而抗病毒免疫力没有受到影响。
相比之下,标准的严重COVID-19治疗方法地塞米松(一种免疫抑制类固醇药物)在保护肺部组织免受疾病相关变化的影响方面作用较小,另外还会导致肺部的SARS-CoV-2水平升高。
Schwartz博士表示:“双硫醒对NET形成的强烈抑制作用及其在不同啮齿动物模型中对疾病结果的改善突出了它的使用潜力以及未来在各种疾病中开发更好的NET形成抑制剂的潜力。”另外他还指出,其他研究人员已经开始对COVID-19患者进行小规模的双硫醒临床试验,不过这些试验的结果还没有公布。

