根据一项新研究,一种新的治疗方法通过迫使癌细胞进入无法增殖的“休眠”状态,防止小鼠转移性肿瘤的生长。这项发表在《实验医学杂志》(JEM)上的研究可能会带来新的治疗方法,防止各种癌症类型的复发或扩散,包括乳腺癌和头颈鳞状细胞癌(HNSCC)。
许多癌症患者复发,往往是在最初治疗的几年或几十年后,并形成新的肿瘤,在同一部位重新生长或转移(扩散)到身体的其他部位。这些继发性肿瘤往往对治疗有抵抗力,是由个别肿瘤细胞产生的,这些肿瘤细胞在重新激活开始增殖之前可能会保持长时间的“休眠”状态。因此,如果研究人员能够找到一种使剩余的癌细胞处于“休眠”状态的方法,就可以防止病人复发。
在之前的一项研究中,西奈山伊坎医学院的Maria SOLEDad Sosa和阿尔伯特-爱因斯坦医学院的Julio A. Aguirre-Ghiso发现,癌细胞保持“休眠”的能力是由一种叫做NR2F1的蛋白质控制的。 这种受体蛋白可以进入细胞核并打开或关闭许多基因,激活一个防止癌细胞增殖的程序。原发性肿瘤中的NR2F1水平通常较低,但在休眠的扩散性癌细胞中却升高了。然后当癌细胞再次开始增殖并形成复发或转移性肿瘤时,NR2F1蛋白的水平再次下降。
Aguirre-Ghiso解释说:“因此,我们认为用一种小分子激活NR2F1可能是一种有吸引力的临床策略,可以诱导癌细胞休眠,防止复发和转移。”
在新的JEM研究中,Sosa和Aguirre-Ghiso的团队使用了一种基于计算机的筛选方法来确定一种名为C26的药物,它能激活NR2F1。 研究人员发现,用C26治疗患者衍生的HNSCC细胞能提高NR2F1的水平并阻止细胞增殖。
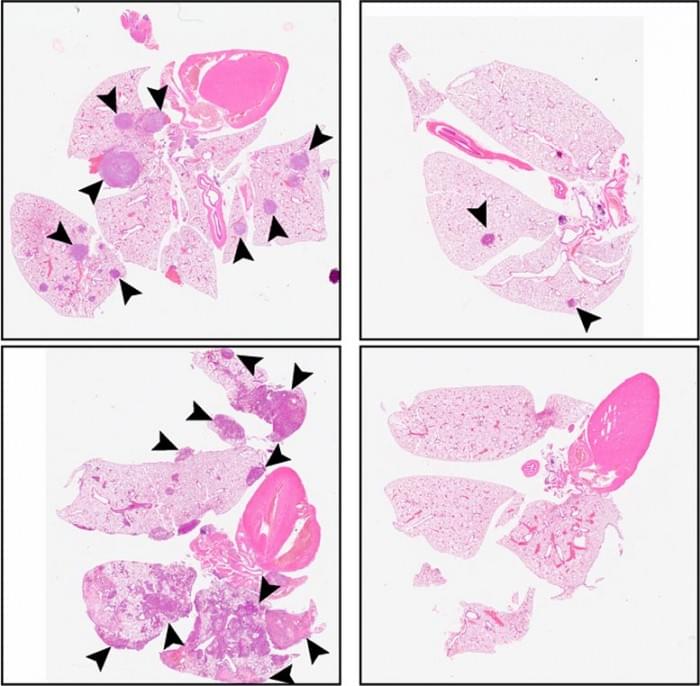
研究人员随后测试了C26是否会阻止小鼠的转移。注射了患者来源的HNSCC细胞的动物通常会形成大的原发肿瘤,在手术切除原发肿瘤后扩散到肺部。用C26治疗减少了原发肿瘤的大小,并且在手术后,进一步剂量的C26完全阻止了转移性肿瘤的生长。相反,啮齿动物的肺部只含有少数“休眠”的扩散性癌细胞,即使在停止治疗后也无法增殖。
Sosa和Aguirre-Ghiso的团队确定,通过激活NR2F1,C26迫使癌细胞进入一种长期的休眠状态,其特点是基因活动的独特模式。肿瘤显示出类似基因活动模式的癌症患者往往会更长时间不复发,这表明用C26型药物诱导这种休眠程序可能对人类有效。
Sosa说:“激活NR2F1的药物可能对乳腺癌特别有用。与ER阴性肿瘤相比,NR2F1在ER阳性肿瘤中高度富集,激活NR2F1可能能够抑制因抗雌激素疗法而保持在该状态的休眠癌细胞的苏醒。然而,由于C26治疗提升了NR2F1的水平,该方法也可能对其他受体蛋白水平本来就低的癌症有用。”
Aguirre-Ghiso说:“总的来说,我们的研究揭示了一种基于机制和合理设计的策略,利用NR2F1激活的休眠状态作为防止转移性复发的一种治疗选择。”

