近日,科学家们回顾了一种特殊的转座子(或跳跃基因),即Line-1逆转录子,在不断扩大的神经退行性疾病中的激活情况。逆转录基因来源于人类内源性逆转录病毒(HERVs),但通常在其基因的开头和末端失去了标志性的长末端重复序列。本周二,发表在medRxiv预印本服务器上的一篇论文可能会解释许多普遍观察到的SARS-CoV-2的致病特征。
作者提供了确凿的证据,证明SARS-CoV-2刺突蛋白激活了血细胞中HERV-W编码的包膜(ENV)蛋白,而这又直接导致了该疾病的许多病理特征。HERV-W因该组的许多逆转录病毒在引物结合位点使用色氨酸tRNA而被命名。显然,字母W的形状在某种程度上让命名委员会想起了色氨酸侧链中原子环结构的形状。
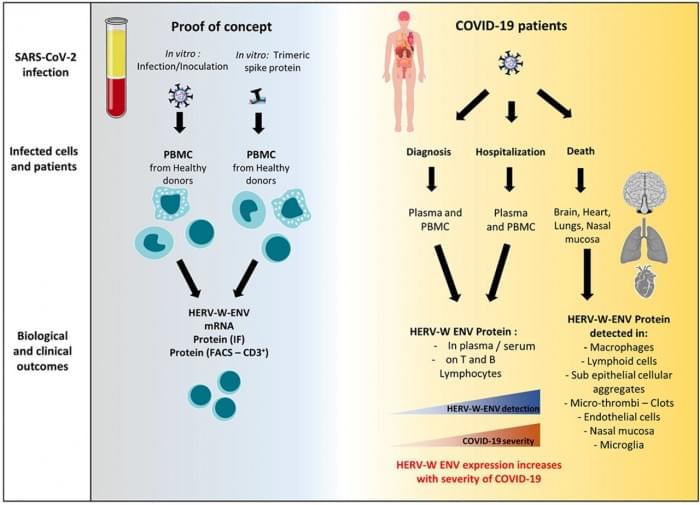
研究人员以前曾观察到HERV-W ENV蛋白在T淋巴细胞中的表达与SARS-CoV-2患者的严重呼吸窘迫有关联。然而,涉及的确切机制并不清楚。现在,HERV-W激活的真正“罪魁祸首”已经被发现。研究人员向SARS-CoV-2患者培养的外周血单核细胞(PBMCs)中添加了一种没有稳定突变的重组三聚体刺突蛋白。他们发现HERV-W和HERV-K的ENV蛋白的RNA立即出现明显的上调。奇怪的是,只有HERV-W的RNA会导致随后的ENV蛋白表达。
因此,mRNA疫苗有轻微的修改,同时使mRNA的免疫原性降低,而其编码的刺突蛋白的免疫原性增强。这方面的一个方法是通过在编码中加入两个战略性的脯氨酸来稳定特定的构象。然而,还需要进行更多的研究,以充分确定稳定的刺突蛋白的融合潜力。一些疫苗制造商已经从他们的mRNA构建体中消除了furin裂解位点,以减少2-PP稳定的构建体的潜在残留融合。其中一些观察结果最初是由一位在社交媒体上以"Underground courtlady"为名操作的匿名研究人员指出的。
这些研究的一个关键发现是,并不是所有的COVID-19患者都有明显的HERV-W ENV激活;只有20%或30%的患者有。这一发现可能反映了感染者的潜在遗传易感性,绝对需要加以定义和考虑,特别是如果HERV-W要被用作疾病严重程度的一般标志物,或作为人源化单克隆抗体疗法的治疗目标,正如现在所设想的那样。例如,在多发性硬化症中发现了可溶性HERV-W的六聚体形式的激活,并被指定为潜在的可药用选项。
但究竟是哪种HERV-W呢?我们的基因组中有1%以上是HERV-W的残留物,比我们所有的蛋白质编码区域加起来还要多。事实上,人类基因组中至少有13个带有全长ENV基因的HERV-W基因座。其中一个来自7q21.2号染色体区域,有一个完整的HERV-W ENV蛋白的不间断开放阅读框。这种蛋白质,即Syncytin-1,在正常的胎盘发育中非常有名,而且基本上是这样。使事情复杂化的是,多发性硬化症现在似乎有许多折衷的潜在起源。研究人员本周透露,受到爱泼斯坦-巴尔病毒的感染是多发性硬化症的一个重要的“上游”、“下游”,或可能完全独立的触发因素,这引起了相当大的好评。
研究人员最近还发现,一种被称为PEG10的逆转录病毒样蛋白直接与细胞外病毒样壳结合并分泌自己的mRNA。这种行为与现在被理解为在突触部位形成记忆的关键的ARC1逆转录病毒蛋白的行为极为相似。令人难以置信的是,研究人员已经开始对这些病毒样颗粒进行假定性,以创造一种内源性载体,作为基因疗法传递功能性mRNA载体。显然,在这些事务中需要谨慎行事。
在COVID-19患者的心脏组织样本中,HERV-W ENV主要在众多小血管的内皮细胞和心包脂肪组织中发现。在这种情况下,HERV-W ENV阳性细胞的内皮性质被CD31染色所证实。不祥的是,在患者的血块、鼻粘膜以及中枢神经系统中也发现了大量的HERV-W ENV,尤其是在小胶质细胞中,即使在这些组织中无法检测到SARS-CoV-2。作者指出,SARS-CoV-2诱导HERV-W ENV在人类淋巴细胞中表达,这些细胞既不表达典型的ACE2受体,也不表达TMPRSS2蛋白酶。这表明病毒进入这些细胞的其他途径。其他候选机制的一个最新线索可能来自替代受体,如ASGR1,它在肝细胞中高度表达。
现在最重要的是找出SARS-CoV-2是如何激活HERVs的。鉴于已知的转座子既能被激活,又能进一步整合到活跃的DNA修复位点,可能值得重新审视早期的研究,这些研究旨在表明反转录的SARS-CoV-2 RNA可以整合到培养的人类细胞的基因组中,随后在患者衍生的组织中表达。这些作者发现了病毒序列侧面的目标位点重复和整合位点的共识性LINE1内切酶识别序列--这些特征与LINE1逆转录子介导的、目标刺激的逆转录和逆转录机制一致。

