一个国际科学家小组已经确定了奥密克戎(Omicron)变体的刺突蛋白的精确结构变化。他们的观察结果解释了该病毒如何能够躲避针对以前变种的抗体而仍然保持高度的感染性。
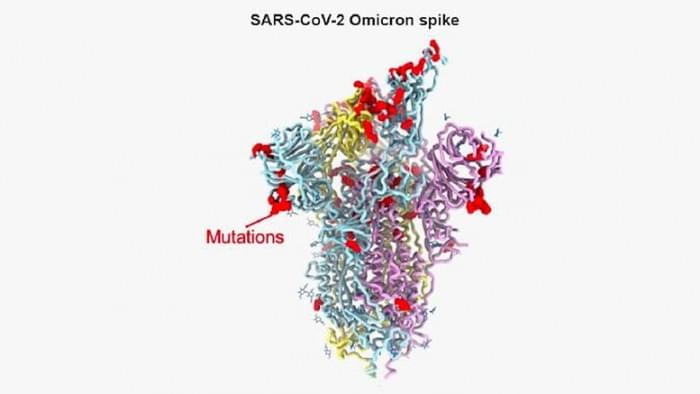
霍华德-休斯医学研究所调查员、西雅图华盛顿大学医学院生物化学副教授David Veesler说:“这些发现提供了一个蓝图,研究人员可以用它来设计新的对策,无论是疫苗还是治疗方法,以应对可能出现的Omicron和其他冠状病毒变种。”他与旧金山Vir生物技术公司的Gyorgy Snell领导了这项研究工作。
研究人员在《科学》杂志上报告了他们的发现。
Veesler实验室的博士后Matthew McCallum和Vir生物技术公司的科学家Nadine Czudnochowski是该论文的主要作者。
Omicron变体于2021年11月在南非首次被发现,它正在导致世界各地的感染激增。除了具有高度的传染性之外,该变体还能逃避针对早期变体的抗体,导致已接种疫苗的人和以前被感染的人发生突破性感染。
该病毒的传染性被认为至少部分是由于该病毒的刺突蛋白的氨基酸序列发生了大量的变异。该病毒利用刺突蛋白来锁定并进入它所感染的细胞。Omicron尖峰蛋白有37个突变,这使它与2020年的第一批SARS-CoV-2分离物不同。
Veesler及其同事以前的研究表明,由六种最常用的疫苗产生的抗体,以及目前用于治疗感染的单克隆抗体中除一种外的所有抗体,中和Omicron的能力下降。
但变体中的许多突变会影响刺突蛋白负责附着和进入细胞的区域的结构,这个区域被称为受体结合域,而且许多人预计受体结合域结构的结果变化可能会损害变体与细胞上的目标结合的能力。这个目标是称为血管紧张素转换酶-2的蛋白质,或ACE2。然而,在他们的研究中,Veesler和他的同事发现,这些变化实际上使受体结合域与ACE2结合的能力增加了2.4倍。
为了了解Omicron是如何在保留与宿主受体ACE2有效互动的同时积累了如此多的突变,Veesler和他的同事使用低温电子显微镜和X射线晶体学研究来揭开Omicron刺突蛋白的三维组织。这种方法使他们能够达到大约3埃的分辨率。在这种分辨率下,有可能分辨出组成刺突蛋白的单个氨基酸构件的形状。研究人员还确定了刺突蛋白的结构变化是如何影响对以前变体有效的抗体与Omicron结合的能力的。
利用这些技术,科学家们揭示了突变如何改变了该蛋白与抗体的相互作用方式,从而使几乎所有针对它的单克隆抗体的能力降低,同时,穗状受体结合域与ACE2结合的能力得到增强。总体效果是使受体结合域有可能躲避针对它的抗体,并更紧密地与ACE2结合。
Veesler说,这些发现表明SARS-CoV-2是一个多么可怕的对手。
“这种病毒具有难以置信的可塑性。”他指出:“它可以改变很多,并且仍然保持它所需要的所有功能,以进行感染和复制。而且几乎可以保证Omicron不是我们要看到的最后一个变体。”
Veesler说,未来的目标应该是关注并确定刺突蛋白上的其他区域,这些区域不能在不导致蛋白失去功能的情况下被改变。由于其重要性,这些区域往往保持保守,即使蛋白质的其他部分发生突变。

