生物聚合物可以自发地自我组装成复杂的结构--类似于容器或笼子,但小得多,被称为“纳米笼”。这些结构可以在里面容纳各种各样的分子以作为“客人”行事。一个流行的例子是“铁蛋白纳米笼”,它是由24个亚单位自组装成的蛋白质铁蛋白形成,可以包围作为重要催化剂的金属离子。
在这些金属离子的帮助下,催化反应将任何底物转化为产品。尽管广为人知,但铁蛋白笼在工业中的潜在应用还没有被充分开发。
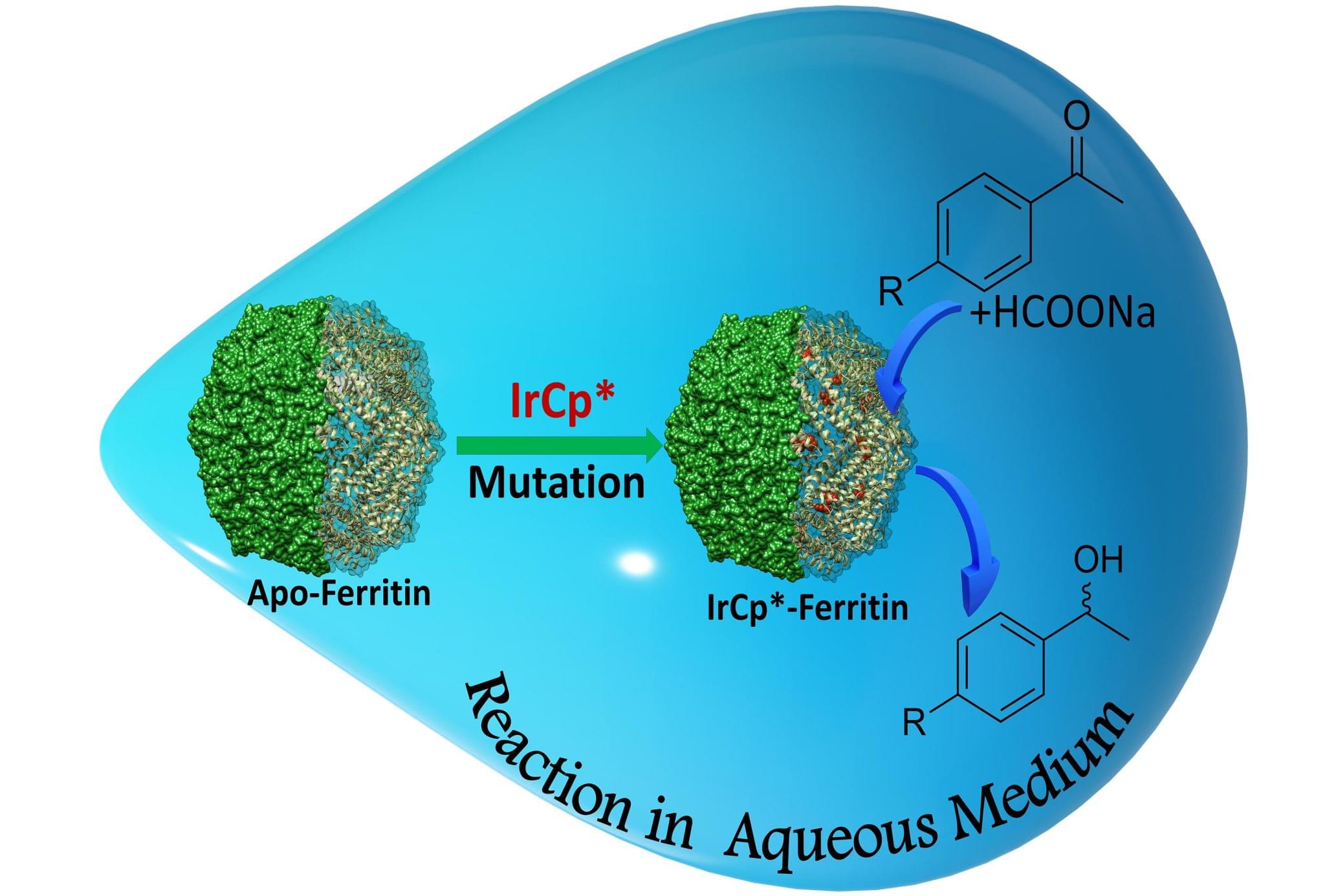
截止到目前,大多数提高铁蛋白中金属离子吸收量的努力都引发了笼子的低稳定性。为了使“客人”能够很好地坐在笼子里,有效的设计是关键。考虑到这一点,由日本东京工业大学的Takafumi Ueno教授领导的科学家团队在铁蛋白纳米笼的核心部分引入了特定位点的突变并增加了其对铱金属络合物(IrCp*)的吸收量。他们的研究结果发表在《Angewandte Chemie》上。铱是酒精生产途径中的一种重要催化剂,另外在制药、食品和化学工业中也得到商业应用。
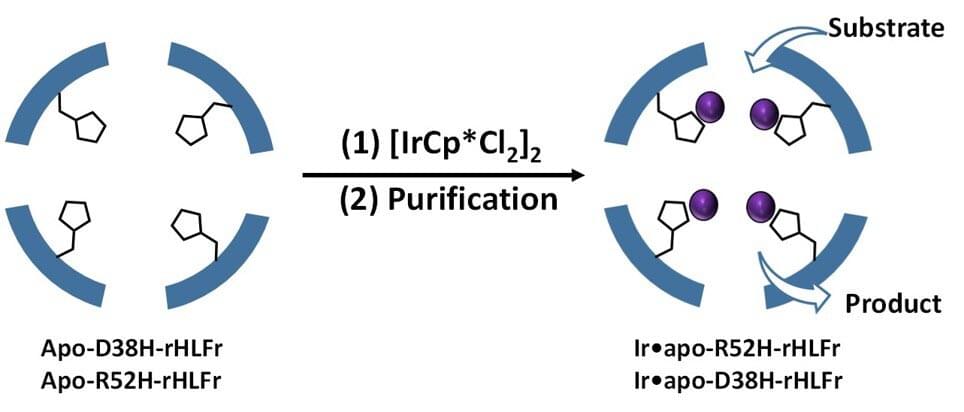
Ueno表示:“根据以前的文献,我们知道笼子里的配位氨基酸的存在会改善铱的活性,用适当的残基取代这些氨基酸可以缓解这个问题。由于铱复合物的行为是一种催化剂,配位残基会起到作用。”研究人员使用氨基酸组氨酸取代两种残基,即常规(野生型)铁蛋白笼子的精氨酸和天冬氨酸,并创造出突变体R52H和D38H。值得注意的是,组装结构或笼子的大小没有受到这些变化的影响。
接下来,他们将IrCp*加入突变体中,发现R52H能嵌入比野生型笼子多0.5倍的铱原子。但令他们震惊的是D38H突变体,它的表现与野生型完全一样。所以,为什么这两个突变体都没有被发现?那么,为什么两个突变体没有相同的效果呢?据Ueno说道:“这意味着不仅组氨酸残基的存在且其位置也是决定笼子中吸收效率的关键。”
使用新的催化笼子,研究人员能够完成高达88%的酒精生产率。显然,突变有利于反应成分的结构重新排列从而提高了转化率。
为了了解底物在笼内的表现,研究人员使用了模拟,其中底物分子可以在纳米笼内自由移动。他们观察到R52H突变体中底物和组氨酸之间的一些相互作用,这在野生型笼子中是不存在的,也就是说,底物在纳米笼内表现出优先结合。
“这些混合生物纳米笼也被发现是高度稳定的,这表明它们可以作为工业应用中可行的催化剂。目前基于结构设计的金属离子结合点研究可以被推进,从而创造出具有选择性吸收特定客体分子的新型铁蛋白突变体,用于化学和制药业的各种催化应用,”Ueno教授说道。

