伊利诺伊大学芝加哥分校(UIC)的研究人员发表的一项研究描述了一种分析细胞焦亡(Pyroptosis)的新方法。细胞焦亡又称细胞炎性坏死,通常是指由感染引起并导致体内过度炎症的细胞死亡过程。该研究还显示,虽然长期以来科学家认为该过程被启动后是不可逆的,但事实上其可以停止和控制。
《自然通讯》杂志报道了这一发现。这项研究意味着科学家们有了一种新的方法来研究与细胞死亡过程有关的疾病,比如一些癌症,以及可能因该过程引起的炎症失控而变得复杂的感染。这些感染包括败血症及急性呼吸窘迫综合症,后者是COVID-19疾病的主要并发症之一。
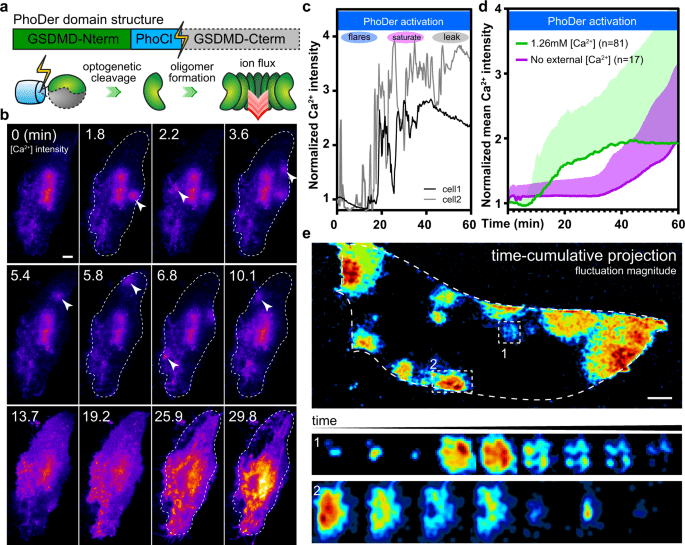
细胞焦亡是一系列的生化反应,它利用气体素(一种蛋白质)打开细胞膜上的大孔,破坏细胞的稳定性。为了更多地了解这一过程,UIC的研究人员通过基因工程设计了一种“光遗传”gasdermin,使其对光做出反应。
UIC药理学和再生医学系以及医学院生物医学工程系的副教授Gary Mo说:“细胞死亡过程在身体中发挥着重要作用,无论是健康状态还是不健康状态,但研究细胞焦亡--这是细胞死亡的一种主要类型--一直具有挑战性。”
Mo说,检查活体细胞中起作用的细胞焦亡机制的方法很难控制,因为它们是由不可预测的病原体启动的,而这些病原体在不同的细胞和人身上又有不同的影响。
Mo表示:“我们的光遗传学gasdermin使我们能够跳过不可预测的病原体行为和可变的细胞反应,因为它在分子水平上模拟了一旦启动焦亡作用在细胞内发生的情况。”研究人员应用这一工具,并使用荧光成像技术在细胞实验中精确激活gasdermin,并观察各种情况下的孔隙。他们发现,某些条件,例如特定浓度的钙离子,仅在几十秒内就触发了孔的关闭。
这种对外部环境的自动反应提供了证据,证明细胞焦亡动态地自我调节。
“这向我们表明,这种形式的细胞死亡不是一张单程票。”Mo说:“这个过程实际上是用一个取消按钮和一个关闭开关来编程的。了解如何控制这一过程为药物发现开辟了新的途径,现在我们可以找到对双方都有效的药物--它使我们能够考虑在疾病中调整、促进或限制这种类型的细胞死亡,而我们以前只能去除这一重要过程。”

