在寻求有效新药的过程中,通常科学家希望找到能附着于致病蛋白质并改变其功能的类药分子。其中至关重要的是,他们要知道一个分子的三维形状,以了解它将如何附着在蛋白质的特定表面。近日麻省理工学院(MIT)的研究人员开发了一种深度学习模型,可以在给定分子结构的二维图形后迅速预测其可能的三维形状。这项技术可以加速药物发现。
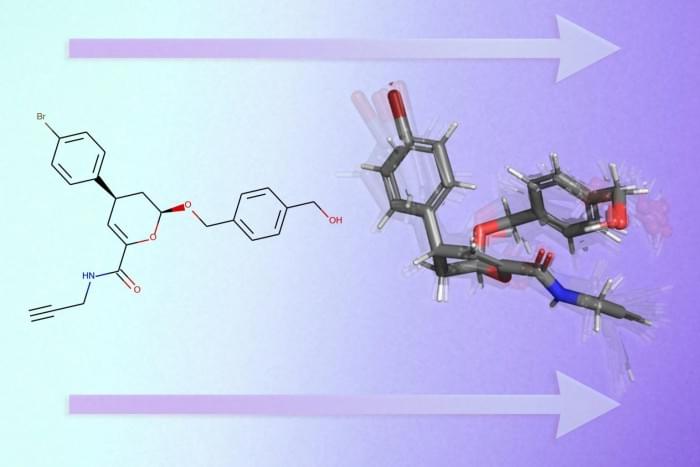
在实际探索过程中,一个分子可以以数千种不同的方式折叠,因此通过实验解决这一难题是一个耗时且昂贵的过程,就像在分子干草堆中寻找一根针。麻省理工学院的研究人员正在使用机器学习来简化这项复杂的任务。他们创建了一个深度学习模型,仅根据分子结构的二维图形就能预测分子的三维形状。分子通常被表示为小图形。
他们的系统 GeoMol 只需几秒钟就能处理分子,并且比其他机器学习模型,包括一些商业方法表现得更好。计算机科学与人工智能实验室(CSAIL)的博士后、该论文的共同第一作者 Octavian-Eugen Ganea 说,GeoMol可以帮助制药公司加快药物发现过程,缩小他们需要在实验室实验中测试的分子数量。
化学工程系的研究生、该论文的共同第一作者 Lagnajit Pattanaik 说:“当你在考虑这些结构如何在三维空间移动时,实际上只有分子的某些部分是灵活的,这些可旋转的键。我们工作的关键创新之一是,我们考虑像化学工程师那样对构象灵活性进行建模。这实际上是在试图预测结构中可旋转键的潜在分布”。
GeoMol 利用了深度学习中的一个最新工具,即消息传递神经网络,它是专门为在图上操作而设计的。研究人员调整了消息传递神经网络,以预测分子几何的特定元素。给定一个分子图,GeoMol最初预测原子之间的化学键的长度和这些单个键的角度。原子的排列和连接方式决定了哪些键可以旋转。
然后,GeoMol 单独预测每个原子的局部邻域的结构,并通过计算扭转角来组装相邻的可旋转键对,然后将它们对齐。扭转角决定了三个连接段的运动,在这种情况下,三个连接四个原子的化学键。

