美国国家过敏和传染病研究所(NIAID)的科学家表示,一种基于mRNA的实验性HIV疫苗在小鼠和非人类灵长类动物中显示出希望。发表在《自然·医学》上的该项研究表明,这种新型疫苗是安全的,并能引发针对HIV样病毒的抗体和细胞免疫反应。
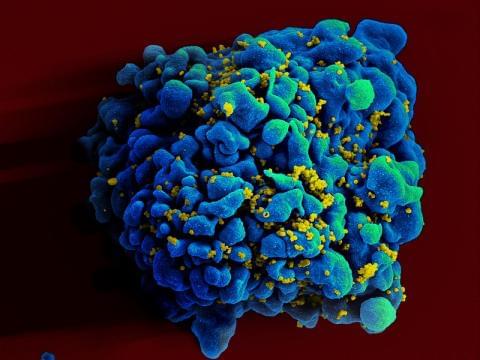
与未接种疫苗的动物相比,接受初免疫苗后多次加强接种的恒河猴,感染猴/人免疫缺陷嵌合病毒(SHIV)的风险降低了79%。论文合著者、NIAID所长安东尼·福奇表示,这一研究结果代表了一种有前途的方法。
实验疫苗的工作原理类似于mRNA新冠疫苗,但并不携带冠状病毒刺突蛋白的mRNA指令,而是提供编码指令来制造两种关键HIV蛋白——Env和Gag。接种动物的肌肉细胞将这两种蛋白质组装在一起,产生病毒样颗粒(VLP),其表面散布着大量Env副本。这些VLP由于缺乏HIV的完整遗传密码,能像HIV一样刺激免疫反应,却不会导致感染或疾病。
研究人员报告说,在实验中,两次注射形成VLP的mRNA疫苗在所有动物中诱导了中和抗体。根据mRNA指令在小鼠中产生的Env蛋白与整个病毒中的Env非常相似,这比之前的实验性HIV疫苗有所改进。
研究团队随后在猕猴中测试了Env-Gag VLP mRNA疫苗。疫苗接种方案的细节在接种动物的亚组之间有所不同,但都涉及用经过修改以优化抗体产生的疫苗来启动免疫系统,并在一年内进行了多次加强接种。加强疫苗包含来自两个HIV进化枝的Gag mRNA和Env mRNA,而不是初免疫苗中使用的那个。研究人员使用多种病毒变体来优先激活针对Env中更保守的“共享”区域(广泛中和抗体的靶标)的抗体,而不是针对每个病毒株中差异更大的可变区域。尽管递送的mRNA剂量很高,但疫苗耐受性良好,在猕猴中仅产生轻微的暂时性副作用。
从第60周开始,免疫和未免疫猕猴对照组每周通过直肠黏膜暴露于SHIV。由于非人类灵长类动物不易感染HIV-1,因此科学家在实验环境中使用嵌合SHIV,因为该病毒会在猕猴中复制。经过13次每周接种,7只免疫猕猴中有2只未感染。其他免疫猕猴的感染总体延迟,平均发生在8周后。相比之下,未免疫猕猴平均在3周后被感染。

