研究人员已经发现了mRNA到达细胞中修改或传递遗传信息的地点和方式,这被认为是开发新疗法的一个关键过程。脱氧核糖核酸(DNA)含有生命发展和维持所需的遗传信息。这种信息通过信使核糖核酸(mRNA)传递,以制造蛋白质。基于mRNA的治疗方法有可能解决各种疾病的未满足需求,包括癌症和心血管疾病。mRNA可以被传递到细胞,以触发目标蛋白质的生产、降解或修改,这是其他方法不可能做到的。
这种方式的一个关键挑战是能够将mRNA送入细胞内,使其能够被翻译成蛋白质。mRNA可以被装入脂质纳米颗粒(LNPs)--以保护mRNA并将其送入细胞。然而,这个过程并不简单,因为mRNA在到达其在细胞内部的作用场所--细胞质之前必须通过膜。
MPI-CBG主任Marino Zerial团队的研究人员是用高分辨率显微镜观察分子在细胞中的进入路线的专家,如mRNA。他们与来自阿斯利康的科学家合作,后者向研究人员提供了他们为治疗方法开发的脂质纳米粒子原型,以跟踪细胞内的mRNA。该研究发表在《细胞生物学杂志》上。
“为了传递,mRNA必须进行一次漫长的旅程。封闭在脂质LNP气泡中,它需要首先进入细胞,”Marino Zerial解释说。“LNPs到达细胞表面,在那里它们与受体结合。然后它们被带入被称为内体的专门的膜封闭隔间。在这一点上,mRNA在细胞内,但被两道屏障包围,即脂肪泡和内体壁,或者更正确地说,膜。mRNA所面临的挑战是如何逃出这两道屏障,到达细胞质,在那里作为模板制造蛋白质。我们知道,只有极小部分的RNA分子能够逃到细胞质中。”
内化的“货物”分子,如LNPs,首先被运送到“早期”内体。这些是物流中心,将“货物”分子分配到细胞内的各个目的地。它们要么将分子回收到细胞表面,要么在晚期内体和溶酶体中降解它们。到目前为止,人们认为mRNA是利用晚期内体的非常酸性的内容从晚期内体中逃脱的。
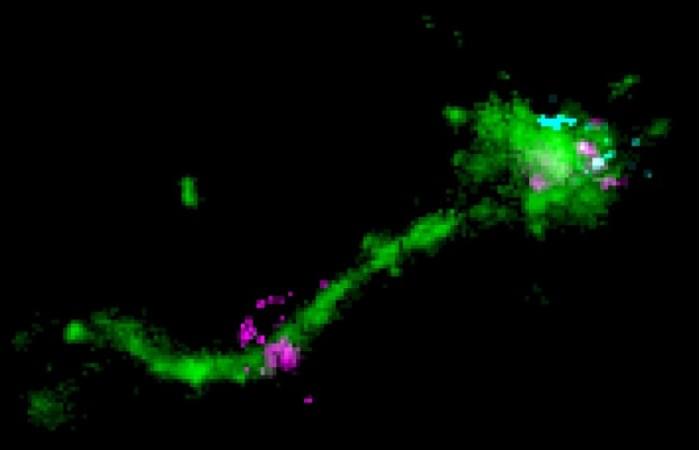
该研究的第一作者Prasath Paramasivam解释说:“通过单分子显微镜技术,我们第一次可以看到细胞内的LNP中的mRNA。我们还捕捉到了mRNA的实际逃逸过程,它发生在回收内体的小管中,而回收内体只是呈弱酸性。”Zerial说:“我们的结果暗示,将LNP-mRNA送入晚期内体对传递有反作用,只会增加细胞的毒性。这些发现有助于更详细地了解mRNA逃离内体的机制。”
Marino Zerial总结说:“由于内体逃逸效率较低,用于mRNA的LNP递送系统有必要使用高剂量。知道了mRNA的去向以及它如何逃离内体,我们就能开发出更好的载体,以更低的剂量进行更有效的传递。我们可以改进mRNA传递系统,使其可以用于治疗性应用,例如癌症治疗。”

