本文来自微信公众号:RNAScript(ID:RNAScript),作者:RNAScript,原文标题:《Nature | 下一代冠状病毒疫苗》,题图来自:视觉中国
COVID-19在世界范围内的大流行,极大地影响了世界范围内多数人的健康。为了抵抗COVID-19,目前世界范围内已有数十亿人接种了新冠疫苗,并在新冠疫情中避免了2000万余人的死亡。但由于新冠病毒不断变异,既往疫苗提供的保护力不再能对人体提供有效的保护。因此,世界各地的研发人员都投入到“下一代COVID-19疫苗”的研发中,不仅是丰富疫苗针对毒株,还要更新疫苗研发的技术和平台。目前,已有数十种“下一代COVID-19疫苗”在研。
目前在研的新冠疫苗非常多样化,但都有一个共同的目标——能够应对病毒变种且提供持久保护作用。有些疫苗提供对未出现变种的保护力,有些病毒则可以提供更强的免疫力或采用更低的剂量引起更强的免疫力,又或者还可以更好地预防病毒的感染和传播。
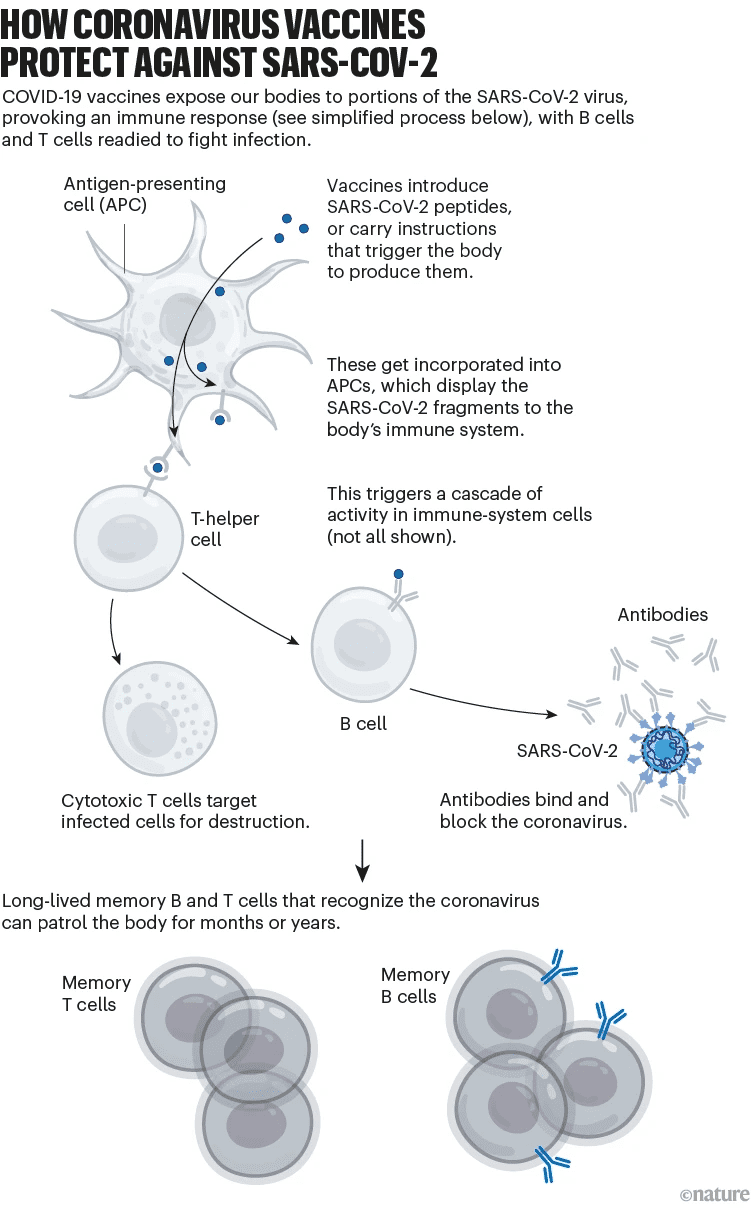
尽管疫苗可以为机体提供对抗严重疾病的持久的保护,但疫苗对病毒提供的保护力在几个月内逐渐减少,而病毒的变异也会增加其免疫逃逸能力,导致疫苗的保护效果降低。(见图4)。
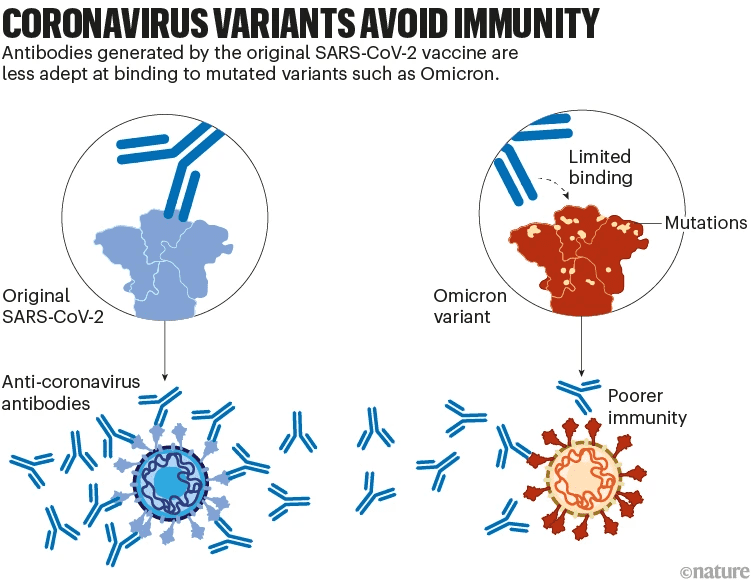
目前,疫苗研发人员已经开发出了第二代疫苗,以增强对奥密克戎变异株的免疫力,之后可能也会根据病毒的变异对疫苗进行更新。但随着免疫衰减和病毒进一步进化,尚不清楚疫苗是否能够提供足够持久的保护力。
因此,研究团队仍需采用更有效对的方法来开发新疫苗。
升级版疫苗
为了应对新冠变异毒株,疫苗开发商辉瑞/BioNTech和Moderna去年推出了新一版大热疫苗,由于同时编码了原始株和Omicron的刺突蛋白(SARS-CoV-2与细胞结合的位置),因此被称为二价mRNA 疫苗。
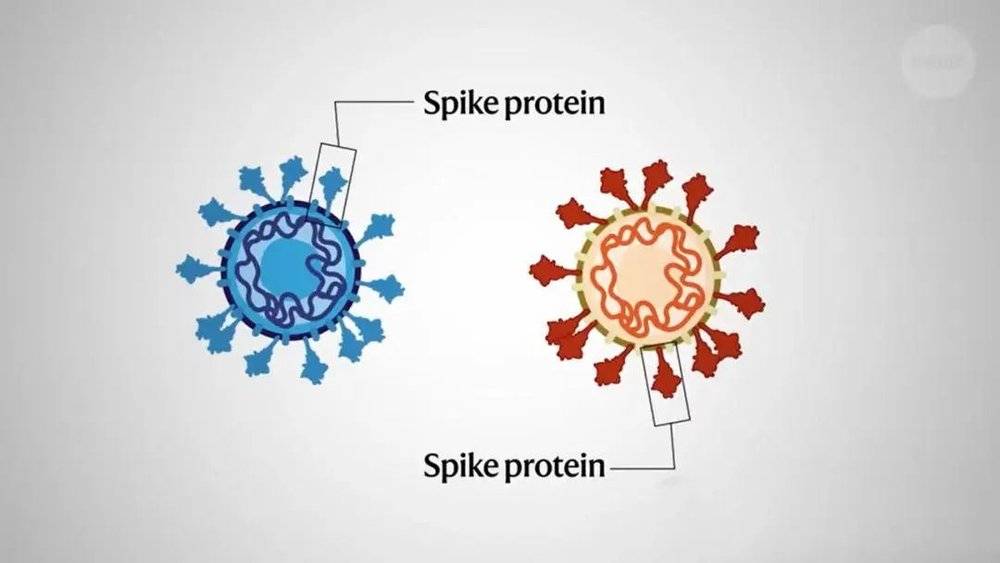
该疫苗通过多种方式发挥作用。与其他COVID-19加强疫苗一样,该疫苗也通过刺激之前疫苗产生的记忆B细胞,获取免疫反应,其中部分细胞可以产生识别奥密克戎的抗体。记忆B细胞的免疫应答效果也会随着时间的推移而增强,当识别到新的奥密克戎刺突蛋白时,这些细胞也会进行突变和进化,从而产生一批新的B细胞,该细胞产生的抗体会与奥密克戎的刺突蛋白产生更紧密的结合,从而起到免疫作用。
此外,二价疫苗中的奥密克戎抗原成分也可以刺激B细胞产生特异性抗体。
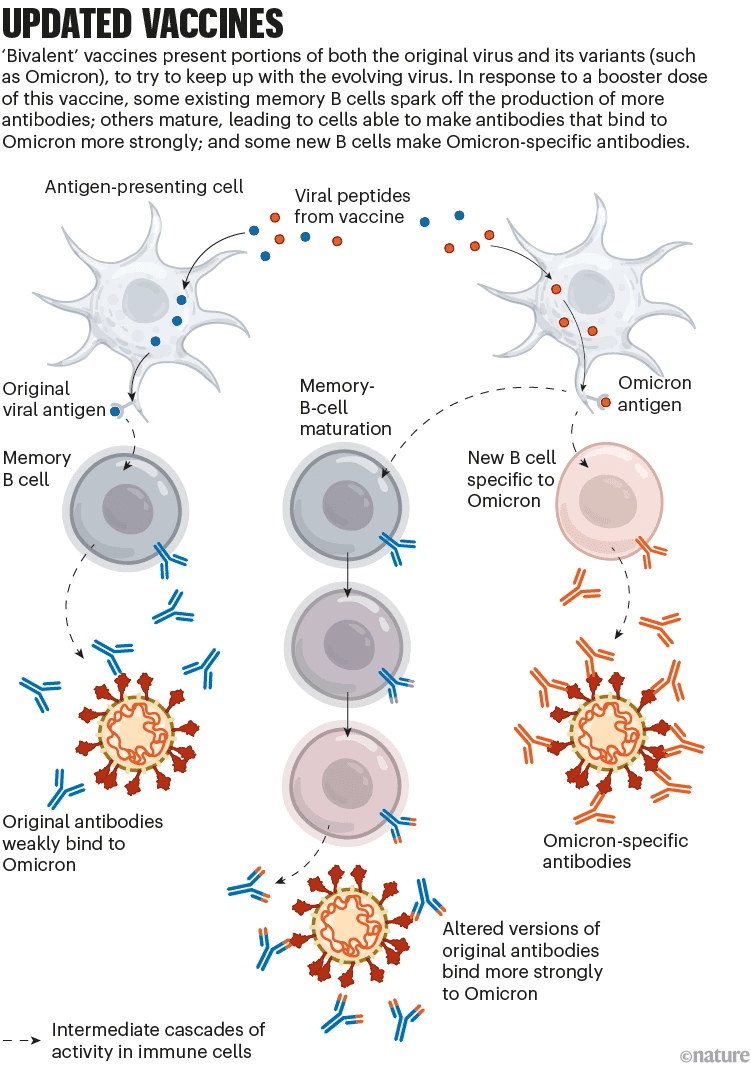
以上作用方式,也让二价疫苗加强针更有潜力对奥密克戎产生了更强的保护作用,但实际效果仍需检验。
辉瑞/BioNTech等疫苗开发商也在尝试开发联合疫苗,以同时提供新冠和其他病毒感染性疾病的侵害,但多数仍处于早期开发阶段。
可提供广泛保护的疫苗
如果说针对新的病毒变种去开发疫苗,那么疫苗的更新就注定会落后于病毒的变异。所以科研团队希望能够开发出针对未出现变种,甚至是相关类型的冠状病毒的“广泛保护性”疫苗。
其中一个开发方向是,选取新冠病毒中不易变异的保守区域,作为疫苗开发的抗原。其中一个目标区域是受体结合域(RBD),该区域与人体细胞上的ACE2受体蛋白结合,并可以被人体抗感染抗体靶向。
西雅图华盛顿大学和帕萨迪纳加州理工学院的至少两个团队正在研发“马赛克”(mosaic)疫苗,该疫苗纳米颗粒上有新冠病毒和来自同一家族的冠状病毒(称为sarbecoviruses)的RBD,例如SARS病毒和从蝙蝠中分离出来的其他病毒。
当B细胞识别出镶嵌在纳米颗粒上的多个RBD时,就会与多种病毒的保守区域紧密结合,反过来会刺激B细胞增殖产生更多抗体,并产生记忆B细胞提供持久的免疫力。相比之下,上一代的疫苗只能刺激B细胞识别并较弱结合一种病毒的RBD。
研究人员希望使用马赛克纳米颗粒能够产生丰富的抗体,从而能够识别并与多种病毒的RBD区域紧密结合。(见图7)。
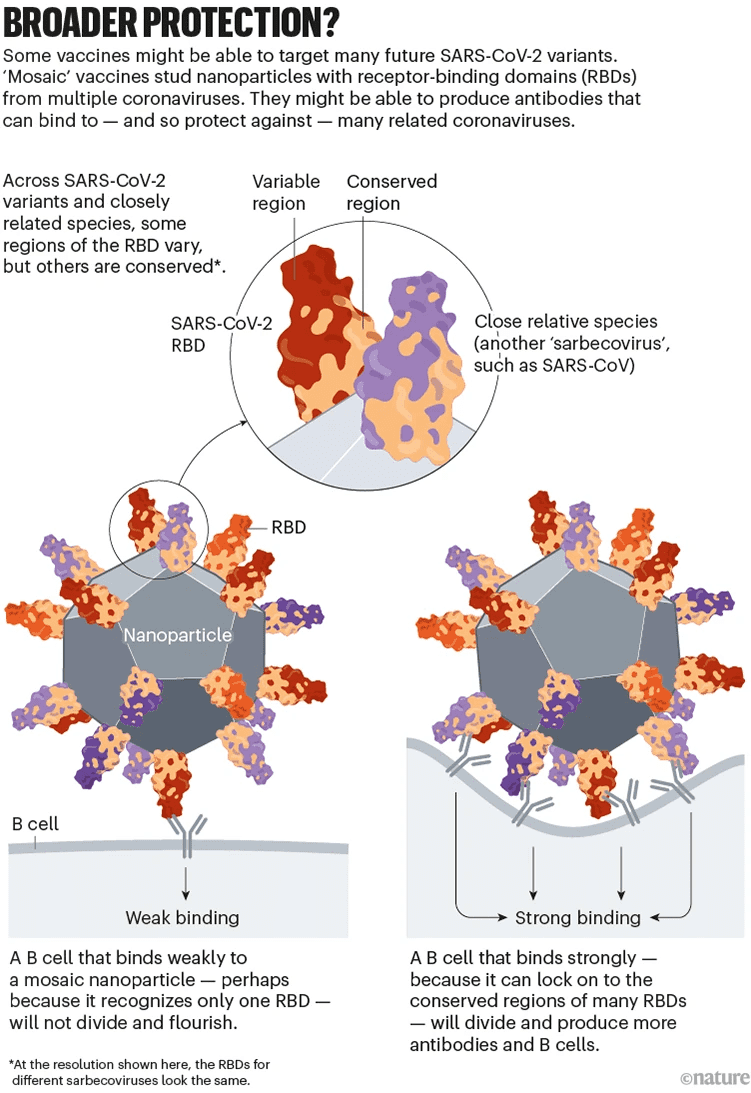
目前,动物实验研究表明,该疫苗的确可以引起针对不同SARBE冠状病毒的免疫反应,并计划在未来两年内开展临床试验。
不止于刺突蛋白
许多第一代的COVID-19疫苗,都是针对SARS-CoV-2的刺突蛋白产生免疫反应,但下一代疫苗也可以通过传递其他病毒蛋白来产生更多样化的免疫反应,从而引发类似感染的保护作用,该方法还可以缓解新病毒刺突蛋白变种的影响。
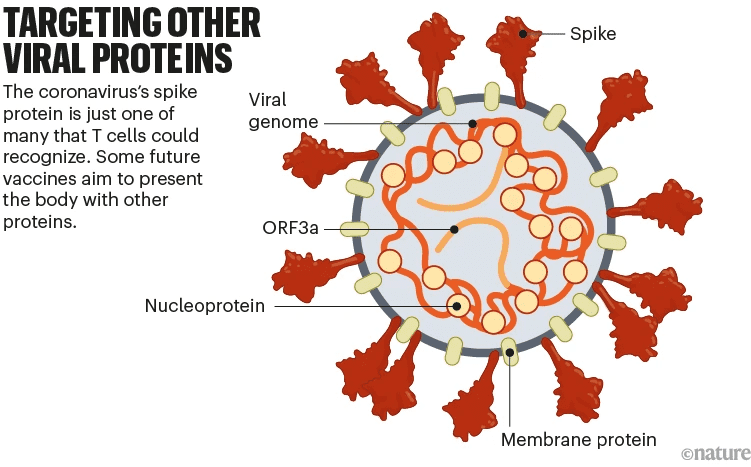
刺突蛋白是B细胞(产生抗体)的主要目标。但是T细胞可以识别多种其他SARS-CoV-2蛋白,从而为免疫系统抗体反应较差的人群提供保护。而非刺突蛋白在各病毒变体之间的差异往往较小,也因此,该类疫苗也可能对病毒进化更具弹性。
美国生物技术公司Gritstone,正在开发一种同时提供多种新冠病毒蛋白信息的mRNA疫苗。同时,得克萨斯州生物技术公司Vaxxinity正在开发一种包含多种抗原蛋白质的疫苗,该公司表示计划今年申请英国和澳大利亚的授权,此前已通过 III 期试验证明了该疫苗的安全性,及作为加强针时的有效性。
新平台设计
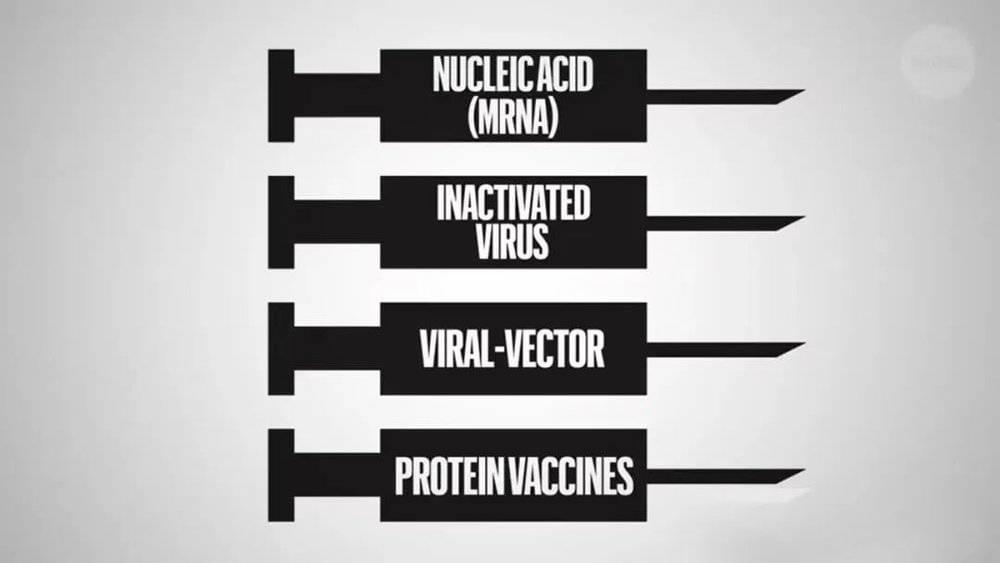
现有疫苗主要分为以下四种类型:核酸疫苗(主要是mRNA,通过递送mRNA在体细胞内产生病毒的刺突蛋白刺激免疫)、灭活疫苗(使用病毒本身刺激免疫反应)、蛋白疫苗(由刺突蛋白或其RBD组成)、病毒载体疫苗(使用通过修饰的腺病毒将刺突蛋白递送至细胞)。
下一代疫苗可能通过调整或修改以上四种策略的递送机制以提高疫苗效力。
自复制RNA
mRNA 疫苗在对抗新冠疫情中起到了举足轻重的作用,在部分发达国家中尤为显著。该技术的升级更有希望提供更便宜、更有效,同时副作用更少的疫苗。
辉瑞/BioNTech和Moderna开发的疫苗通过脂质纳米颗粒包裹编码刺突蛋白的mRNA,而下一代RNA疫苗技术自复制RNA(saRNA)疫苗中还包括一种酶,该酶可以疫苗中的RNA在细胞复制,以产生更多数量的刺突蛋白(见图9)。
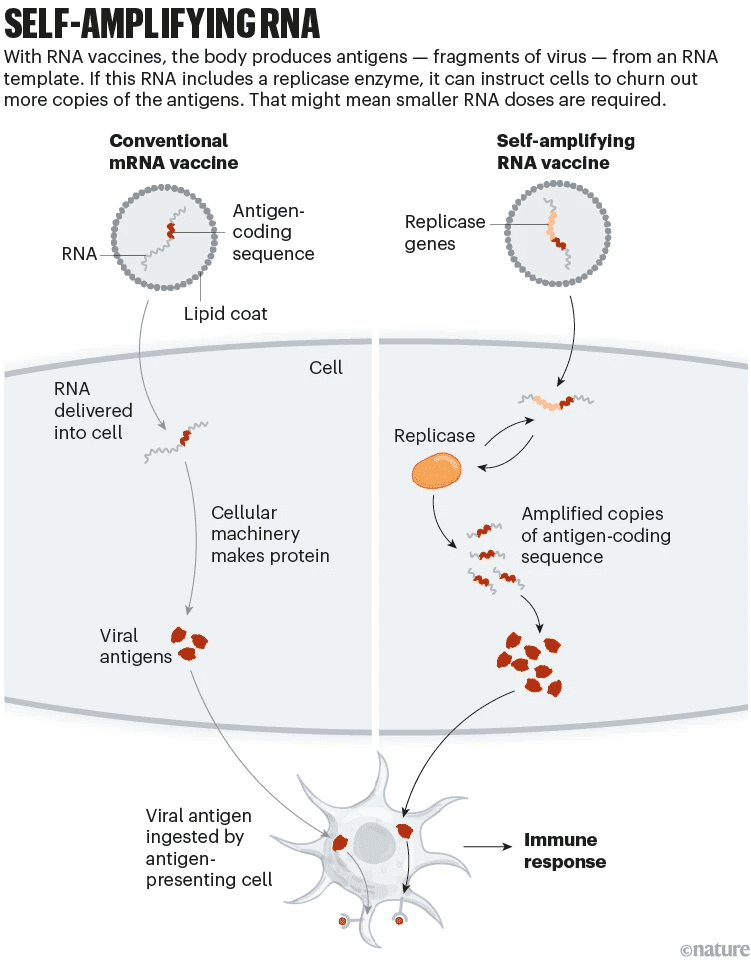
也就是说,与传统的mRNA疫苗相比,低剂量且可能成本更低的saRNA疫苗可以实现与传统mRNA疫苗相同甚至更强的免疫反应,而较低的剂量也可能有助于减少副作用。
由美国公司Arcturus Therapeutics开发的一种saRNA疫苗于2022年4月完成了 III 期试验;该公司现在已在日本开展了另一项 III 期试验。
Gritstone正在使用saRNA技术研发T细胞疫苗,用以递送额外的新冠病毒蛋白,该候选疫苗已经完成了 I 期临床试验。
纳米颗粒蛋白疫苗
几种基于蛋白的新冠重组蛋白疫苗已在全球获批,其中包括美国生物技术公司Novavax生产的新冠疫苗,该疫苗成本低和且易于生产使是主要优势。该疫苗通常由完整的SARS-CoV-2刺突蛋白或其RBD的保守区域生产。
新一代的蛋白疫苗由表面点缀着刺突蛋白及RBD的蛋白组装成的足球结构构成,以类似真病毒的重复排列方式,以产生更加有效的免疫反应。加州理工学院和华盛顿大学开发的“马赛克”疫苗(镶嵌着来自多种冠状病毒的RBD)是其中之一。
另一种纳米粒子疫苗已经于2022年4月获得韩国监管机构批准,该疫苗也是由华盛顿大学开发的,疫苗成分包括原始SARS-CoV-2毒株的RBD。该疫苗的一项 III 期试验表明,该疫苗抗体反应是阿斯利康病毒载体疫苗的几倍。但开发该疫苗的韩国公司SK biosciences在2022年底表示,由于韩国对该疫苗的需求较低,该疫苗现已停产。
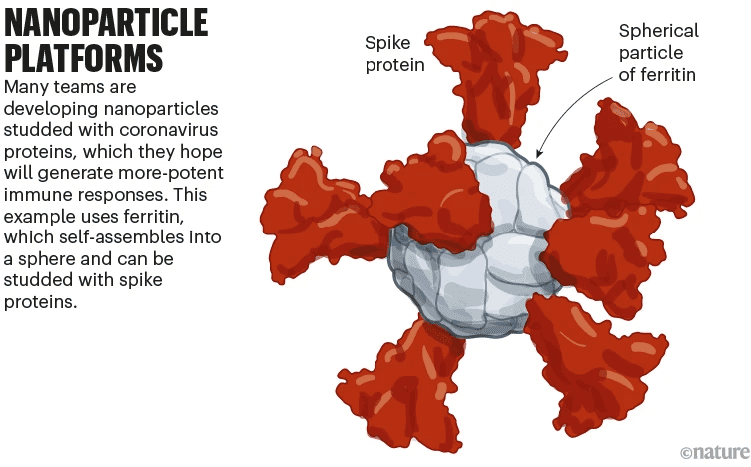
位于马里兰州银泉的美国沃尔特里德陆军研究所的研究团队,正在开发另一种蛋白质纳米颗粒疫苗,该疫苗使用一种被称为铁蛋白的运铁蛋白,该蛋白自组装成一个球形颗粒,表面镶嵌完整的SARS-CoV-2刺突蛋白,目前正处于早期测试阶段(见图10)。
鼻腔疫苗
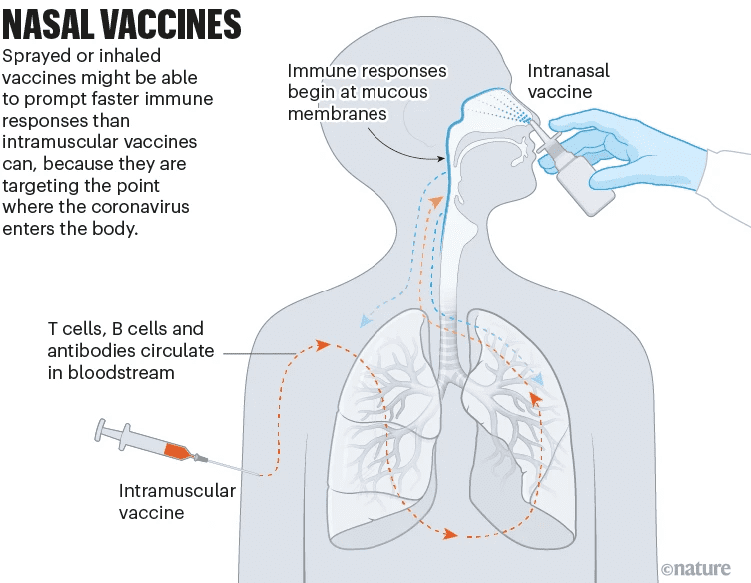
目前,部分新冠疫苗以雾状通过鼻腔或口腔吸入,或以滴鼻剂的形式诱发免疫。通过在SARS-CoV-2 进入人体第一道关卡——呼吸道黏膜激发免疫反应,黏膜疫苗理论上可以阻止病毒的传播(见图11)。
鼻腔疫苗的有效性已通过动物实验证明,目前世界上已有至少5中鼻腔疫苗已经获准使用——中国有两种,印度、伊朗和俄罗斯各有一种。但目前尚无数据表明该疫苗可以减少病毒感染或传播方面优于注射疫苗。
流行病防范创新联盟是一家位于奥斯陆的基金会,是下一代新冠疫苗的主要赞助方。该机构的疫苗研发执行主任梅兰妮·萨维尔(Melanie Saville)说,开发鼻腔疫苗及其他下一代新冠疫苗的关键挑战是证明它们比现有的疫苗具有更突破性的进展。
激烈的竞争
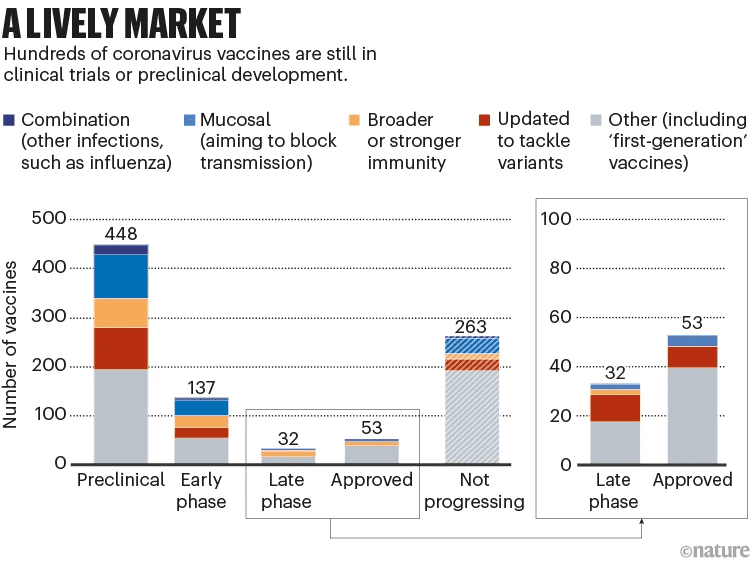
目前,世界范围内已有50多种疫苗获批,还有数百种处于早期和晚期临床试验阶段。此外还有数百个疫苗项目流产。所以,所有的下一代疫苗都必须在激烈的全球竞争中争夺市场份额。(见图12)。
在已批准的疫苗中,少数几种疫苗占有多数的市场份额。
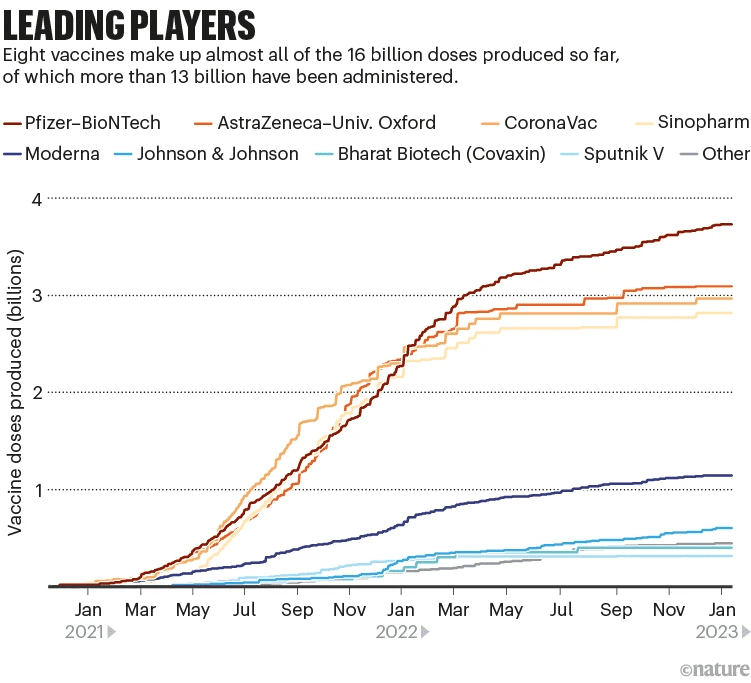
伦敦生命科学信息公司Airfinity的分析总监马特·林利(Matt Linley)表示,尽管研究如火如荼,但目前疫苗市场的主导地位仍会由mRNA疫苗(如Moderna和辉瑞/BioNTech疫苗)占据主导地位。
含有Omicron的二价mRNA疫苗的快速开发,证明了mRNA疫苗可以快速研发和适应新毒株的能力。“如果病毒出现了新的变种,mRNA疫苗将通过其高速的反应力迅速进入并领导市场。”Linley 说。
Saville 补充说,新冠不再像过去那样被视为全球卫生紧急事件,对疫苗的需求不再迫切,所以开发商和监管机构对于新冠疫苗的推进紧急程度也不如从前。但是,即使新疫苗技术的研究不再应用于与新冠的对抗中,该技术平台仍可以用于对抗其他疾病,例如CEPI为不同病毒谱系开发的“疫苗库”,为未来可能出现的疫情威胁做好准备。
本文来自微信公众号:RNAScript(ID:RNAScript),作者:RNAScript

