但在这片混乱中也是有迹可循的。这个“变异群”帮助科研人员发现了有利于变异株扩散的数个免疫逃逸突变。全球范围内,好几个“重量级”选手已经陆续登场,这些变异株在不同地区有着不同的命运——至少目前来看如此。

图片来源:Pixabay
在欧洲、北美和非洲,尽管感染总数看似在下降,但Omicron BQ.1家族的变异株流行率却在迅速上升。在亚洲国家,包括新加坡、孟加拉国和印度,名为XBB的支系引发了新的感染潮。科研人员正在密切关注这两类变异株同时传播的多个地区,看看哪个的优势更大。
瑞士巴塞尔大学的计算生物学家Cornelius Roemer说:“某些变异株最终可能会占据主导地位,但其决定性肯定不如从前。”
一个大家族
引发之前疫情的变异株,如Alpha和Delta,全部来自新冠病毒家谱树的不同分支。但自从Omicron在2021年底出现之后,它不断酝酿出各种亚型,包括BA.2和BA.5,这些亚型在全球掀起多轮疫情。许多国家在今年年中已经对国内的BA.5疫情不再关注,但大部分科研人员认为,另一个亚型杀出重围只是时间问题。
过去几个月里,变异株追踪者一直在梳理新冠病毒的全球测序数据,筛选出有潜力的变异株。但他们发现,快速崛起的亚型不只有两三个,而是有十几个。
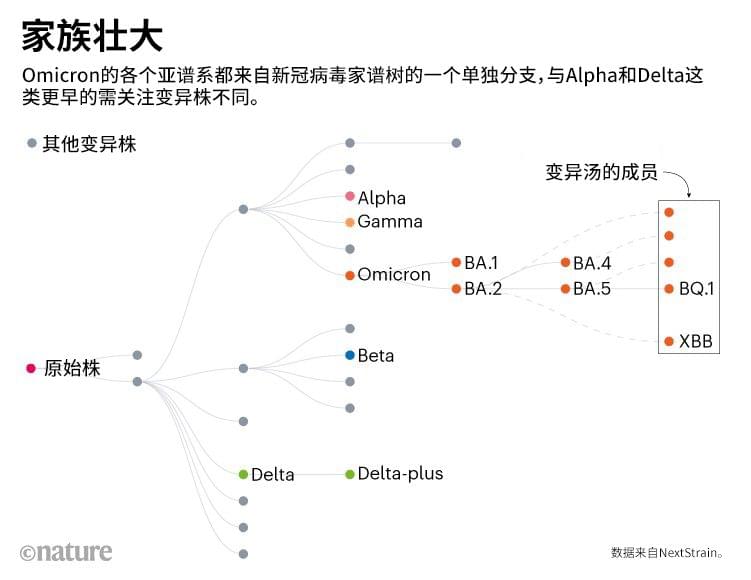 来源:Nextstrain
来源:Nextstrain北京大学免疫学家曹云龙(Yunlong Richard Cao)说:“这是一个变异株集合,或称群、汤——和我们之前见过的不一样。”曹云龙团队一直在研究这些变异株的免疫逃逸能力。
虽然这个群的成员来自Omicron家谱树的不同部位,但它们的崛起似乎都能归结到少数几个共同的基因突变上,其中大部分突变都会让名为“受体结合结构域”(RBD)的病毒刺突蛋白部位发生氨基酸改变。刺突蛋白的这个部位是病毒感染细胞所必需的,也是能形成强效免疫应答的抗体的作用目标。
曹云龙团队10月发布的研究[1]显示,这些RBD突变能帮助新冠病毒逃逸新冠疫苗和之前Omicron其他亚型(包括BA.2和BA.5)感染所诱导的阻断感染的“中和性”抗体。(该研究尚未经过同行评审。)
又变异了
Roemer和其他人发现,这些RBD突变越多,一个变异株的崛起速度(以全球数据库上传的序列数量为衡量标准)就越快。比如,像BQ.1这种有5个关键RBD突变的变异株(相较于BA.2),其崛起速度似乎比有6个突变的变异株要慢。BQ.1的后代BQ.1.1有6个此类突变,正在欧洲、北美等地迅速蔓延。
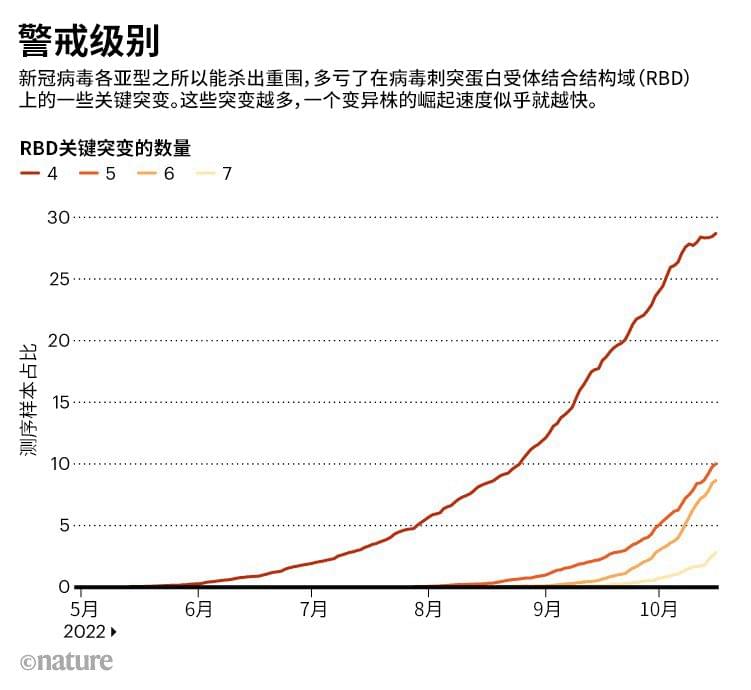 来源:Cornelius Roemer, Cov-Spectrum.org and GISAID
来源:Cornelius Roemer, Cov-Spectrum.org and GISAID第7个RBD突变似乎能让变异株更快突围(不过科学家提醒这些估算数据只是大概,尤其是当有记录的序列数量很少时)。科学家正在监测的一个主要“7级”变异株是XBB。这个变异株是两个Omicron亚型的混合或重组——这两个亚型都是BA.2的后代。
在这个变异群中,BQ.1.1和XBB似乎有登顶之势。BQ.1家族已经在法国成为了主导,而且可能会在欧洲和北美入冬后掀起新一轮疫情。它还同时存在于南非、尼日利亚、非洲其他地区的“变异汤”中。相比之下,XBB看起来会在亚洲称王称霸,而且近期已经在新加坡引发了一轮感染。
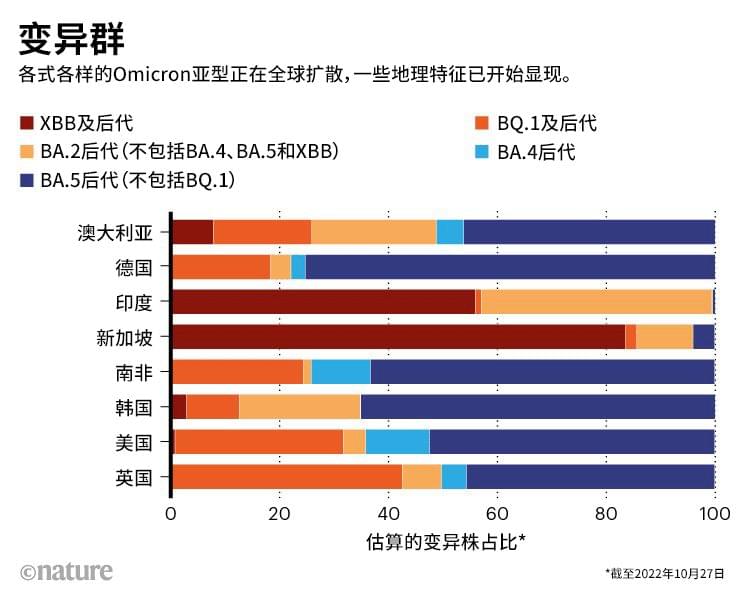 来源:Moritz Gerstung, Cov-Spectrum.org and GISAID
来源:Moritz Gerstung, Cov-Spectrum.org and GISAID研究人员还在监测BQ.1.1和XBB同时传播的国家,看看哪个传播速度更快。Roemer说,澳洲的早期迹象表明,XBB更有优势。印度似乎也是相同的状况,协调印度马哈拉施特拉邦新冠病毒基因测序工作、来自普纳BJ政府医学院的微生物学家Rajesh Karyakarte说,“我们将能看到哪个会在这里存活下来。我们猜测是XBB。”
曹云龙说,XBB超过BQ.1家族的优势可能部分源于它在刺突蛋白RBD外部的突变。这个变异株在编码刺突蛋白N端结构域(NTD)的基因组区段中也有突变。来自曹云龙实验室的初步数据显示,人体免疫系统也会派中和抗体攻击刺突蛋白的这一部位,而且已经康复的BA.2和BA.5感染者能对NTD产生非常强的免疫应答。
曹云龙还表示,XBB逃逸靶向NTD的抗体的能力,使其能感染对BQ.1及其近亲免疫的人群。他说,不过“BQ.1获得NTD突变的速度也快得惊人”。他的团队在未发表的研究中指出,这类突变会极大地增强这些变异株逃逸疫苗接种和既往感染诱导的中和抗体的能力。
BQ.1.1或许会导致病例数激增,使得XBB只能在部分地区取而代之,Roemer说,“如果最后我们发现XBB在全球占据了主导,欧洲和北美可能会出现某种程度的双重疫情。”
双重免疫?
一个主要决定因素将是感染BQ.1谱系能在多大程度上预防XBB。曹云龙团队目前正在研究这个问题。“我有一种感觉,就是如果你感染了BQ.1,你可能有针对XBB的一些保护力,”他说,“但我们现在还没有数据。”
无论是XBB、BQ.1.1,还是这个变异群的其他成员,一旦引发大规模感染,就会破坏社会秩序;就算再轻的轻症也会对健康带来长期影响。不过,研究人员正在密切关注接下来的感染潮是否会导致很高的住院率和死亡率。
在一篇尚未发表、针对28名XBB感染者的初步研究中,Karyakarte的团队发现,这些人中没有重症。Karyakarte说他在孟加拉国的同事也报道了类似的现象。新加坡在XBB暴发期间出现了COVID-19住院率的小幅上升,但这种严重影响比过去几轮疫情都要小一些。
然而,季节性——北半球冬季可能会迎来新冠病毒传播加速,加上之前的疫情和防疫政策这类因素,意味着新加坡的疫情或许不能用来预测其他国家,Roemer说,“那里的情况可能不能看作是将来的预演。”
参考文献:
1. Cao, Y. et al. Preprint at bioRxiv https://doi.org/10.1101/2022.09.15.507787 (2022).
原文以COVID ‘variant soup’ is making winter surges hard to predict为标题发表在2022年10月28日《自然》的新闻版块上

