本文来自微信公众号:量子位(ID:QbitAI),作者:明敏,原文标题:《未老先呆,这锅熬夜真的要背:生物钟影响阿尔茨海默症的机制被发现》,头图来自:视觉中国
不得不说,在让我们好好睡觉这件事上,科学家们真的费心了。
这不,他们再一次论证当人们作息规律紊乱时,大脑中与阿尔茨海默症(老年痴呆)密切相关的淀粉样蛋白Aβ42将不能被及时清除。
这种蛋白大量积累将会导致神经元发生损伤,进一步损害大脑。
而调节这种变化的关键,是一种蛋白聚糖——它会附着巨噬细胞表面,影响Aβ42被清理的情况。
当蛋白聚糖附着量越高,巨噬细胞就越不能正常工作。
科学家发现,在睡眠条件下,这种蛋白聚糖的含量会降低,Aβ42可以被很好清理。
也就是说,你熬的每一个夜里,脑子里积累的“痴呆诱导素”就越多一些。
熬夜越猛,痴呆越早?
所以,还熬吗?
一、蛋白聚糖是“计时器”
此次的研究大致可分为两部分。
科学家们首先从分子机制层面论证,Aβ42在人体内的水平确实会随着昼夜节律发生变化。
然后,他们找到了控制这种变化的“计时器”是两种蛋白聚糖。
我们先来看实验的前半部分。
此前研究已经发现,熬夜和阿尔茨海默症之间存在双向关系,比如许多阿尔茨海默症患者在患病多年前已经出现睡眠障碍。
这可能是吞噬Aβ42的巨噬细胞受到了昼夜节律调节。
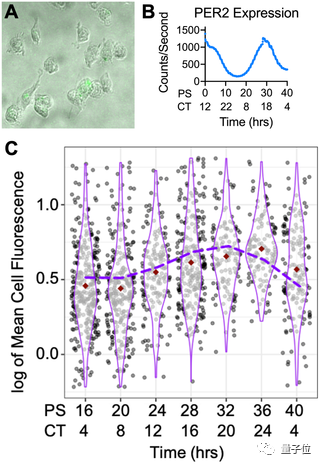
研究人员为了论证这一理论,采用BMDM吞噬作用测定法,对Aβ42进行荧光标记,以此来确定生物钟是否会起到调节作用。
BMDM是从小鼠骨髓内提取出的一种巨噬细胞,实验设计为模拟昼夜交替、在培养皿中观察40小时内Aβ42沉淀量变化情况。
结果表明,在实验开始后16-20小时之间,Aβ42的沉淀量最高;在30小时左右时,沉淀量最低。
由此不难看出,Aβ42被吞噬是在随着昼夜节律波动。
接下来,科学家们对这些巨噬细胞进行了详细分析。
结果发现,有两种蛋白聚糖的含量变化与这一规律相关,它们分别是硫酸肝素蛋白聚糖(HSPG,heparan sulfate proteoglycan)和硫酸软骨素蛋白聚糖(CSPG,chondroitin sulfate proteoglycan)。
数据显示,在Aβ42沉淀多时,HSPG和CSPG的含量更高;反之,在Aβ42被大量清理时,HSPG和CSPG的含量很低。
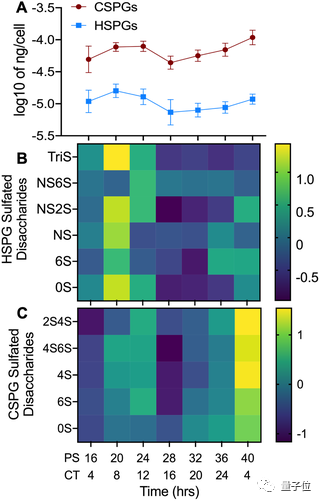
通过进一步研究,科学家发现这是由于蛋白聚糖HSPG会随着生物钟的变化在吞噬细胞表面聚集。
从下图中可以看到,模拟白天的情况下,HSPG的含量一直居高不下,对应Aβ42的沉淀量也很高。
在处理时间为12小时(CT12)、进入夜间后,HSPG含量降低,对应Aβ42的沉淀量也在降低。
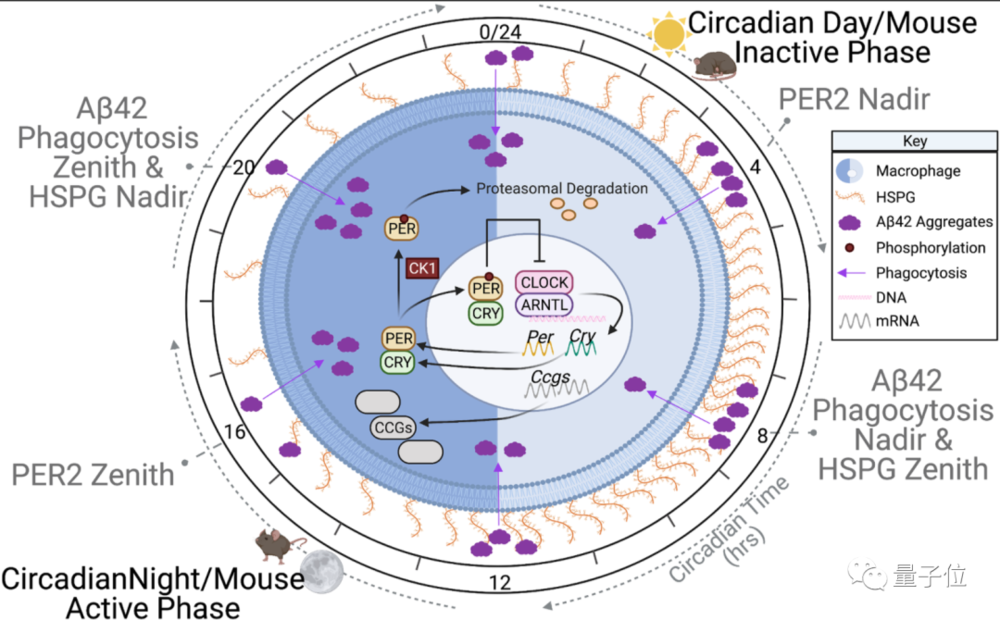
此项研究的通讯作者Jennifer Hurley表示,显然Aβ42的积累是随着昼夜节律变化的。
不过,目前研究还未能揭示为什么这些蛋白聚糖会影响巨噬细胞清理Aβ42。
但它还是为治疗阿尔茨海默症提供了一种新的治疗思路:
是不是人为提高昼夜节律的频率,就能增强Aβ42蛋白的清理了呢?
二、大脑:求求你别熬了
如果说这一项研究结果,还是无法阻拦你熬夜的心。
那么,下面还有许多研究都能表明,熬夜这件事代价极大。
此前,Science上曾发表一篇论文表示,深度睡眠是大脑“清理垃圾”的重要途径。
波士顿大学团队通过对十余名23岁~33岁之间的受试者观察研究,结果发现在睡眠期间,人体血液会节奏性地从脑部流出,每当有大量血液流出时,脑脊液就会趁机进入大脑,代谢出脑部沉积下的“垃圾”。
我们如上提到的Aβ42蛋白就是其中之一。
另一方面,熬夜还会影响DNA损伤的修复。
要知道,DNA损伤得不到修复,就很有可能引发基因突变甚至癌变。
Cell子刊《Molecular Cell》上的一项研究指出,人在内的多种生物平时积累的DNA损伤,会在睡眠状态下被加速修复。
为了能够修复这些损伤,我们的身体甚至有一套机制来喊你睡觉。
……
当然,如果你坚持长期熬夜,也不一定会得老年痴呆——
因为长期熬夜很可能没有机会活到老年(doge)。
论文地址:https://journals.plos.org/plosgenetics/article?id=10.1371/journal.pgen.1009994
参考链接:
[1]https://news.rpi.edu/content/2022/02/10/clearance-protein-linked-alzheimer%E2%80%99s-controlled-circadian-cycle
[2]https://www.science.org/doi/pdf/10.1126/science.aaz5191
本文来自微信公众号:量子位(ID:QbitAI),作者:明敏

