本文作者:陈阳,题图来自:视觉中国
6月13日欧洲杯小组赛中,丹麦队球员埃里克森心脏骤停突然倒地。37秒后,医务人员携带AED冲进场地实施急救,成功将埃里克森从死神手里拉了回来,整个抢救过程也为全球观众直播与普及了猝死急救的“黄金4分钟”。
2019年11月27日,某演员在录制节目奔跑时突然心脏骤停减速倒地,现场未及时除颤与CPR急救,后续到医院抢救2个多小时无效,最终因心脏性猝死离世。这两个新闻事件当时都广受关注,一时间将“心源性猝死”、“AED”、“CPR”等词引入公众视野。2例猝死抢救公众事件的结果截然不同,关于猝死防治的思考也绝不仅仅是“黄金4分钟”这一点。
据《中国心血管病报告》估计,我国每年猝死者近60万人,每分钟就有1人因心脏骤停突然倒地,但抢救成功率仅为1%。想拯救庞大的猝死高风险人群,我们要做的还有很多。
一、 猝死与存活率
1. 什么是猝死
猝死占工业化国家总死亡率的5%-15%,但无论中国还是美欧猝死的确切发病率都相对模糊。美国心脏性猝死在年死亡数中占5.6%,1999年美国心脏性猝死估计量为450,000例,心搏骤停的发病率估算为180,000-450,000例以上。在北美和欧洲,一般人群中的估计发病率为50-100/10万人。
其中,2/3的心搏骤停患者尝试了复苏,生存情况差异较大——院外情况下的生存率为1%-6%;院外心搏骤停患者的出院生存率中,经急诊治疗的患者生存率为5%-10%;而当患者基础的心律失常为室颤时,生存率为15%。
来自国家心血管病中心发布的《中国心血管病报告》显示,据估计我国每年死于心脏性猝死有54.4万人。
中国医学科学院阜外心血管病医院相关课题在2005-2006年对东中西部四个城市超过67万人随访,一年共发生心脏性猝死 284例,由此推断中国心脏性猝死发生率为41.8/10万人,其中男性心脏性猝死发生率为44.6/10万人,女性为39/10万人。
目前媒体报道的“猝死”或“心源性猝死”是一种笼统性描述,其包含了心搏骤停(sudden cardiac arrest, SCA)与心脏性猝死(sudden cardiac death, SCD),两者都指心脏的机械活动突然停止,伴血流动力学衰竭,导致患者无反应、没有正常呼吸也无循环体征,若不迅速予以纠正会发展为猝死。通常是由持续性室性心动过速(VT)/心室颤动(VF)引起(图1)。大多数发生心搏骤停的患者会因为脑血流量不足,而在数秒至数分钟内丧失意识。
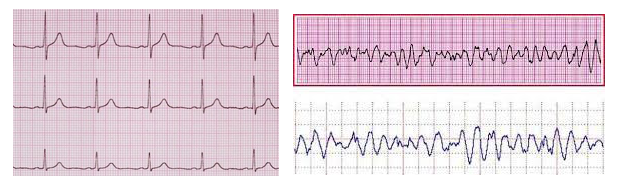
如上图,左侧的心脏的规律心电节律使得心肌规律收缩、正常搏动泵血,当室颤发生时,右侧的心肌电活动紊乱、心室的心肌抽搐、心腔无法有效收缩(心脏的机械活动突然停滞)、泵血,造成全身瞬间血流停滞、脑血流不足,人意识丧失、瞬间倒地。
通常急救干预方法包括心肺复苏(CPR)和/或除颤、心脏复律;心脏起搏,如果干预或自发性逆转恢复循环,称为心搏骤停(或心脏性猝死未遂);如果患者死亡则称为心脏性猝死。院外心搏骤停与心脏性猝死很难区别,因为仅2/3猝死发生时有目击者,很多患者在发病时的心律是否为室颤状态未知。
心搏骤停事件之前常有“预警”症状,出现时间在心搏骤停前1小时到1个月不等:51%患者在心搏骤停前的4周内有预警症状,80%和34%的患者分别在心搏骤停发生至少1小时和24小时前出现过症状。
其中,胸痛(46%)和呼吸困难(18%)是最常见的症状,在女性中呼吸困难比胸痛更常见(31% vs 24%)。但由于症状大多为非特异性且未必发作前都会出现,也尚未确定症状和猝死之间的因果或时间关系,所以在预防方面意义不大。49%的心脏性猝死发生在日常活动期间,23%发生于睡眠中,23%与运动有关。
2. 存活率的外因与内因
尽管近年来急救手段进步,但心搏骤停者的结局仍然不良,仅1/3院外心搏骤停患者的复苏成功,并且所有患者中仅约10%最终出院,其中很多患者存在神经功能损伤。有很多因素都会对结局有影响:旁观者心肺复苏(CPR)延迟、心脏除颤延迟、老龄、表现为室颤(VF)的患者比例降低等,其中,发病至有效复苏(即建立有效脉搏)的时间间隔可能最关键。
(1) 外因:发病至有效复苏的时间间隔
①急救体系的可及性
即使在急救体系较成熟的国外,近年来紧急复苏培训较成熟、接受目击者心肺复苏(CPR)的患者比例增加、发病至除颤的间隔有所缩短,但是随着人口增长和都市化,基础生命支持(basic life support, BLS)和高级生命支持(advanced life support, ALS)服务到达现场所需的时间依然有所增加。国外研究显示,心搏骤停的发病率和结局存在明显的地区差异,并强调各地急救系统对心搏骤停结局的重要性。
②室颤持续时间
心搏骤停患者的生存情况取决于是否迅速实施了有效的CPR,电除颤是重新建立规律性电活动和心肌收缩的唯一治疗方法。
室颤持续时间增加会造成两个主要不良反应:①降低终止心律失常的可能性;②如果VF持续超过4分钟,中枢神经系统和其他器官开始出现不可逆损伤——“黄金4分钟”的由来。心搏骤停的持续时间越长,复苏的可能性或生存率就越低。
研究表明,在未行CPR的情况下,除颤每延迟1分钟,VF所致心搏骤停的生存率约降低10%;在未行CPR超过12分钟后,生存率仅2%-5%。
(2)内因:病因
心搏骤停的机制与初始复苏的结局之间具有相关性,室性快速性心律失常导致的心搏骤停患者存活率往往更高。
①室性快速性心律失常:结局好
猝死最常见的病因是室颤,当初始心律是持续室性快速性心律失常(如室颤、室速等)时,患者的结局会相对较好。
室颤(VF): 25%-40%的VF所致心搏骤停患者可存活。国外获得救治的心搏骤停患者中有38%为有旁观者目击的VF。具有旁观者目击的VF患者与其他心律的心搏骤停患者相比,在出院时仍存活的可能性明显更高(34% vs 6%)。急性心肌梗死或心肌缺血是导致VF的主要潜在原因,存活的患者中约47%- 51%有急性心肌梗死。
室速(VT): 出现血流动力学不稳定性VT的患者生存率约为65%-70%。单形性VT患者的预后可能更好,因为此类心律失常较为规律,可能存在一定程度的体循环灌注。而且VT患者的既往心肌梗死发病率比室颤患者低,心功能更好(射血分数往往更高)。
②心搏停止:结局差
当最初观察到的心律是心搏停止(即使在心搏停止之前是VT或VF) 或室性自主心律非常慢导致心动过缓的患者,成功复苏的可能性低。仅10%的院外停搏和初始心搏停止患者能存活至入院,低于5%的患者存活至出院且神经功能良好。这类患者结局较差可能由于心搏骤停的持续时间长(通常超过4分钟),存在严重且不可逆的心肌损伤。
③无脉电活动:结局差
无脉电活动(pulseless electrical activity, PEA)也称为心电机械分离,所导致的心搏骤停患者结局也较差。被复苏且在入院时存活的患者占23%,出院时存活的患者仅11%。
④非心源性心搏骤停:结局差
1/3的心搏骤停为非心源性,创伤、非创伤性出血、中毒、近乎淹溺和肺栓塞最常见。40%获得了成功复苏并住院治疗,仅11%的患者出院,6%的患者神经功能完好。
二、 “追赶”解决外因——公共卫生与猝死的分秒赛跑
基于上述分析,提高心脏性猝死患者抢救成功率的关键在于尽早实施有效抢救,在最佳抢救时间的“黄金4分钟”内对患者进行心肺复苏和除颤有很大的概率能救活患者,10分钟后能抢救回来的人少之又少。
由于我国有87.7%的猝死发生在医院外,由目击者首先进行心肺复苏是最及时的方法,可以为医务人员到现场抢救赢得时间。目击者急救至关重要——与急救中心的专业人员救治相比,由非专业第一施救者用自动体外除颤仪(automated external defibrillator, AED)早期除颤可使患者生存率增至2倍。如果晕倒3分钟内给予除颤,74%有目击者的室颤患者可以存活。从骤停至除颤的间隔时间每延迟1分钟,生存率就会降低约5%-10%。目击者心肺复苏在欧洲可达到60%,但我国公众心肺复苏普及率很低,现场目击者实施心肺复苏非常少见,复苏质量更是难以保证。
1. 存活关键——时间窗与复苏质量
基础复苏,包括CPR和AED除颤。心搏骤停后存活的关键是早期识别和治疗,患者生存率主要取决于是否立即启动高质量CPR和早期除颤。
目前复苏指南强调的关键点在于:①通过观察到无反应或无呼吸/喘息样呼吸而立即识别心搏骤停;②立即开始实施高质量CPR(适当的用力+快速按压),并持续关注胸外按压质量和通气频率;③尽可能减少CPR的中断;④对于医疗专业施救者,检查有无脉搏的时间不应超过10秒;⑤对于未经训练的单人施救者,鼓励其实施高质量的单纯胸外按压CPR(CO-CPR);⑥如有AED,则尽快应用;⑦尽快呼叫急救中心。
(1)时间窗
复苏的时间窗主要分3阶段:前4-5分钟需要立即除颤,4-10分钟胸外按压+除颤,10分钟后很少有患者存活。这主要和心搏骤停的进展机制有关:
①电阶段:室颤所致心搏骤停的4-5分钟内。此时需立即除颤,以尽可能增加这些患者的生存率。准备除颤仪期间进行高质量的胸外按压也会提高生存率。
②血流动力学阶段(循环阶段):心搏骤停后第4-10分钟,在此期间患者可能仍有心室颤动,早期除颤对发现为心室颤动患者的生存仍然至关重要。一旦确定为心搏骤停应立即开始高质量胸外按压,并一直持续到实施除颤。实操上应该在有效按压期间给除颤器充电,只有在确认节律和给予电击时才暂停按压,实施电击后立即重新开始CPR。血流动力学阶段的患者会获益于高质量胸外按压产生充足的脑和冠状动脉灌注以及立即除颤。
③代谢阶段:在脉搏消失10分钟后,到这一阶段很少有患者存活。其治疗主要基于复苏后措施,如低温疗法。此阶段的患者如果不能快速恢复成有灌注的心脏节律,通常无法存活。
(2)复苏质量
①识别
快速识别心搏骤停是成功复苏至关重要的第一步。施救者目击有人突然倒下或者偶遇看起来无反应的人员时,在接近该患者之前应确保该区域安全,然后拍其肩部并大声呼喊以确认是否无反应。如果确认无反应,施救者应立即开始胸外按压并呼叫急救中心。需要注意的是,即使专业人员也难确定是否有脉搏或呼吸是否充分,目击者不应尝试评估脉搏而应假设患者已停止呼吸,即使检查颈动脉脉搏也不应超10秒。关键的原则是不能延迟CPR。
②按压
CPR中最重要的部分是胸外按压 ,因为冠状动脉灌注和自主循环恢复(ROSC)都与按压相关。关键指标:①频率:胸外按压的速度维持在每分钟100-120次。胸外按压频率不足会降低心搏骤停后ROSC和存活且神经系统完好的可能性;②深度:每次向下按压胸部的深度为至少5cm、但不超过6cm;③回弹:每次按压胸部后,要让胸廓完全回复。回弹会使胸内压降低,从而增加心脏前负荷以及达到较高的冠状动脉灌注压;④持续:应尽量减少任何中断的频率和时长。
尽可能减少中断:如果CPR过程中胸外按压中断(无论时间多短),都会导致冠状动脉和脑的灌注压下降并进一步使患者结局更差。
③通气
当非专业的目击者施救时,单纯胸外按压CPR(CO-CPR)可能优于胸外按压加通气。目前指南提倡对心搏骤停的按压—气道—呼吸(compressions-airway-breathing, C-A-B)方法,原理在于心搏骤停初期肺泡很可能还含有足量水平的氧,且肺血管和心脏可能含有足量的氧合血可以满足机体明显下降的需氧量,开始高质量胸外按压是改善氧输送至组织的第一步,这时胸外按压比通气更重要。
但是,伴随缺氧的心搏骤停患者,其氧储备可能已经耗尽,这时就需要实施有通气的高质量CPR。随着脉搏消失持续,恰当实施通气越来越重要。关键指标:①若对患者未建立高级气道,每30次胸外按压后通气2次;②每次通气持续时间不超过1秒;③给予的潮气量仅足以观察到胸廓上抬即可(500-600mL)。
④除颤
早期除颤对室颤患者的生存率十分关键。对于成人建议除颤时使用可用的最大能量水平,在AED完成充电之前不要停止按压,使用AED给予一次电击后应立即恢复胸外按压。
2. 针对时间窗——AED的配置密度与半径
心搏骤停发生频率高的特殊场所包括公共交通设施、购物中心、公共体育场馆等,急救人员到达之前可由目击者使用这些场所的AED除颤,这就是“公众除颤”(public access defibrillation, PAD),极大地扩大了能够提供早期除颤的潜在施救者群体。
(1)AED配置直接影响猝死生存率
公众除颤能够有效提高心搏骤停后生存率和神经系统结局。国外研究显示,公共场所中发生心搏骤停的患者配置AED者生存率(23.4%)要显著高于没有配置AED (14.0%),神经系统功能正常存活者比例更高(50% vs 14%)。日本在2005-2013年间在全国公共场所广泛配置AED,非专业人员使用AED对有目击者的VF停搏进行电击的比例从1.1%升至16.5%。随着公众启动除颤的增加,停搏至电击时间从3.7分钟缩短至2.2分钟,神经系统功能良好生存率显著提高2倍(从18.2%升至38.5%)。
(2)进一步缩短AED可及半径
心源性猝死发生的黄金救援时间是4分钟之内开始心肺复苏及除颤,以正常人的跑动距离结合现有AED覆盖率测算,目前我国的AED尚处于“有却不可及”的阶段。
而活动AED的覆盖效率是固定式AED的6倍,以本次欧洲杯为例,急救队医背AED进场速度与效率之高为移动AED的典范——0秒,运动员无接触倒地;5秒,裁判招呼医务人员进场;13秒,队医到现场;37秒,携带急救设备AED的医务人员冲进场地;52秒,AED开始工作;1分36秒,医务人员开始心肺复苏。如果在体育场内固定位置放置AED,是不可能以如此之快的速度完成急救的。移动AED的行动方向是单向的,覆盖面积是固定式AED的4倍(单向跑动距离是来回双向跑动距离的2倍);同时,节约了判断寻找及取用等一系列操作,责任人任务清晰、分工明确。研究显示,移动AED抢救覆盖效率是固定AED的6倍左右,大大提高了AED的潜在救治范围。
(3)中国AED普及落后,2020年开始追赶
目前,我国的AED普及和使用相关的科普教育都还有很大差距。中国AED配置率只有0.2台/10万人,而美国2017年已达317台/10万人,日本394台/10万人,荷兰695台/10万人。与之相应的,我国院外猝死救治成功率仅1%,而美国救治成功率已接近40%。
近年来,随着公众人物猝死事件频频发生,AED逐渐得到人们的关注与重视,政府也逐渐加速公共场所AED的普及。2006年,中国正式投放AED,北京首都机场是国内第一家引进AED的公共场所,在T2航站楼安装了11台。2008年北京奥运会让AED在国内的普及达到一个小高潮,但奥运会结束后又冷了下来。2019年,国务院颁布的《健康中国行动(2019-2030年)》明确提出心肺复苏培训人员比例要求,并指出完善公共场所急救设施设备配备标准,在学校、机关、企事业单位和机场、车站、港口客运站、大型商场、电影院等人员密集场所配备急救药品、器材和设施、配备AED。
十三届全国人大常委会第十五次会议通过《中华人民共和国基本医疗卫生与健康促进法》审议,其增加了AED相应规定:公共场所应按规定配备必要的急救设备、设施。希望在考虑规模、人员情况、设置意愿等综合条件基础上,在公共场所合理投放配置AED,逐步形成网络。
2020年是AED普及的关键节点,全国多个城市陆续开始在公共场所尤其是交通枢纽配置或增加AED,标志着AED在中国的普及迈出了一大步。全国多个城市都在推动AED的投放,为加快AED普及的落实,制定了AED配置计划。
行动较早的是深圳,目前AED覆盖率全国第一。2017年深圳已启动公众场所配备AED计划,截至2021年3月,深圳已在公共场所配置5500多台AED,并配备“AED导航”系统,未来5-10年争取达到100台/10万人配置率的国际建议标准。
2020年12月,三个城市同时完成AED规模投放:东莞地铁2号线实现AED全站点覆盖,广州地铁首批试点的59台AED完成安装使用,昆明市投放1100台AED于地铁站、大型商场超市、景区、机场等公共场所。从2016年开始,在中国的一些城市,AED 已经在公共场所发挥作用。2020年10月27日, AED首次进入了北京的地铁站。截至2020年12月底,北京地铁安装了58台AED,分别在1号、2号、13号线。
同时,各城市还在持续指定未来配置计划:南京市制定了在2021年前布置1000台AED的计划,地铁站点实行AED全覆盖;北京宣布2022年底前重点公共场所(轨道交通车站)AED设施全覆盖;杭州计划到2022年全市公共场所配置AED总数达到4200台;云南将在全省配置4800台AED设备。
2020年10月,《杭州市公共场所自动体外除颤器管理办法》通过,自2021年1月1日起施行,成为全国首个以地方立法形式规范公共场所AED(自动体外除颤器)配置和使用的城市。同时,计划3年内全市范围内增加3596台AED,保证配置率42台/10万人。
随着AED的普及,今年上半年已有很多例地铁猝死AED施救成功的新闻报道,国内公众除颤施救有了可喜的开始。
3. 伸出手——最可能救命的“旁观者”负担解除
AED一开始在国内推广不顺利的原因还有公众的顾虑,公共场所中如果心搏骤停者突然倒地,周边围观者畏于法律风险很少敢上前抢救。由于一些广为流传的不利判例,很多人担心事后与患者或家属有法律纠纷。担心救命后民事责任的顾虑不仅个人有,很多公众场合的管理部门也有。尽管《中华人民共和国民法典》第184条规定,因自愿实施紧急救助行为造成受助人损害的不承担民事责任。但现实中想改变公众对于施救的恐惧还需要很长的时间,不过随着相关政策和许可的推行,越来越多公众场合抢救成功的案例宣传,距离心跳骤停者最近的“旁观者”的负担会逐渐减小。
4. 针对复苏质量——CPR培训
除了AED配置密度与旁观者法律责任问题,我国急救普及率低也是心搏骤停抢救率低的主要原因。很多目击者在猝死现场不会、不敢CPR也是问题,只能拨打120而错失“黄金4分钟”的抢救时间。发达国家的急救培训覆盖率非常高,法国的急救培训普及率为其总人口的40%、德国80%、美国30%,但是我国急救培训率仅为1%。 目前,普及急救知识已有制度性安排,《健康中国行动(2019-2030年)》鼓励支持红十字会等社会组织和急救中心等医疗机构开展群众性应急救护培训,普及全民应急救护知识,使公众掌握基本必备的心肺复苏等应急自救互救知识与技能。
安排国家卫生健康委牵头,教育部、财政部、中国红十字会总会等按职责分工负责。并明确提出中小学健康促进行动,把学生健康知识、急救知识,特别是心肺复苏纳入考试内容,把健康知识、急救知识的掌握程度和体质健康测试情况作为学校学生评优评先、毕业考核和升学的重要指标。
而最终如何落实,尚需要卫生行政部门指导、教育部门培训、公益组织配合的多部门协作,多环节衔接才能补齐目前公共服务短板,最终使我国的猝死救治生存率有效提高。
5. 进一步提高生存质量——ECPR
目前,院外心脏骤停的常规CPR复苏后的神经功能良好率仅为5%~10%,患者因其得不到及时高效的抢救措施,经常丧失了良好神经功能预后的机会。虽然常规CPR因其方便快捷,目前仍为心肺复苏广泛推广的基本方法,但其循环支持作用相对较弱。
心搏骤停后机体处于血流停滞、重要器官处于无灌流状态,常规CPR在高质量按压下实际为低血流状态(心输出量可达到心脏骤停前的30%~40%,冠脉灌注压达20-25 mmHg),能够满足一定的自主循环的恢复需求。但如果患者心脏骤停超过30 分钟不能持续维持自主循环,称为难治性心脏骤停,此类患者由于重要器官(脑、肾等)长时间灌注不足,良好神经功能预后的几率更低。
体外心肺复苏(extracorporeal cardiopulmonary resuscitation,ECPR) 是指对经过选择的病因可逆的心脏呼吸骤停患者、已使用传统心肺复苏不能恢复自主心律的患者,快速实施体外膜氧合,提供暂时的循环及呼吸支持的技术。
ECPR是近年新开展的复苏技术,可缩短心脏骤停后低血流时间,使难治性心脏骤停患者的神经功能良好预后达到30%~40%。2015年美国心脏协会心肺复苏指南提出:可以考虑在特定的心脏骤停患者中应用ECPR,但是必须有快速、专业的团队。国际体外生命支持组织(ELSO)报告显示,近10年来成人ECPR快速增长,2018年达到1197例总体存活率为2 9.5%,我国ECPR总体存活率为26%。
据部分中心报道,ECPR患者中CPR持续时间低于60 分钟建立ECMO循环的患者良好神经功能预后率达到50%,超过60 分钟的患者良好神经功能预后率23.1%。
ECPR成功取决于及时的CPR、强有力的ECMO团队及后续的ICU加强治疗,我国目前的急救体系与重症临床联动尚需进一步加强:
(1)体系:急救网络联动与ECPR响应区域覆盖
需要注意到ECPR同样具有明显的抢救时间窗——当CPR持续进行15分钟以上未恢复自主心跳,应立即使用ECMO进行紧急循环及氧合支持。如果想在院外心搏骤停的患者15分钟内可以及时应用上ECMO,必然依赖现有的急救体系。在院前环节,目击者呼救120时尽可能同时通知区域内医院的ECPR团队提前准备,急救人员到达现场后评估患者、告知ECPR团队患者即将送达的医院,然后ECPR团队携带设备立即出发。
在120转运时,需要同时考虑与ECPR可行的医院的运输半径与时间,这与ECPR的成功率直接相关。进院后,院内配套ECPR绿色通道,患者可及时进入ECPR临床路径。ECPR配套的复苏室需要必须的设备与物品完备。
(2)人员:ECPR技术与ECMO培训
由于ECPR时间极其重要,因此距离不宜过远。在距离允许的情况下,患者可转运至综合救治能力较强的区域ECPR中心,进行多学科协作救治。为进一步缩短转运半径,建立ECPR分中心完成不同区域覆盖,以保证心脏骤停患者的及时救治势在必行。ECPR要进一步规模性开展,涉及到ECMO培训,依赖当地经验丰富的区域ECPR中心提供技术指导以保证复苏质量与ECPR技能。
(3)设备与现场ECPR:移动ECMO缩短循环恢复时间
传统边复苏边转运至院内的方式,不可避免碰到转运途中复苏质量的下降,目前欧美部分院前急救系统直接携带ECMO设备至现场实施ECPR,缩短了低血流灌注时间,增加了自主循环恢复率。但我国急救体系与资源尚有限,现场ECPR处于发展早期。近年来,随着急救意识进步,我国高端急救车开始配备ECMO设备。
由于转运期间的环境与ICU环境不同,用于急救转运的ECMO性能有特殊要求——耐受转运中的颠簸撞击且要求便携性。由于技术壁垒高,尚未国产化,目前国内ECMO均为进口,主要为Maquet(迈柯唯)、Medtronic(美敦力)、LivaNova(理诺珐)等进口厂家占据。其中,用于急救转运的ECMO由于性能要求高,目前只有Maquet独家产品Cardiohelp,作为高端产品线定价近300万元尚未大规模配置。国内目前研发急救ECMO的公司有苏州心擎医疗等。
三、 “超越”解决内因——向前一步,临床的预防重任
心脏性猝死的发作突然且难以预测,绝大多数发生在医院外。虽然AED可有效抢救,但需要旁观者来应用和操作。据统计仅50%的心搏骤停有人目击,当心搏骤停患者身边没有目击者发现时,就不可能有效施救。所以在群体层面,发生了心脏性猝死后通过救治来挽救生命是来不及的,降低猝死死亡率的关键还在于心脏性猝死防治的有效性。
1. 猝死的“上游”——心血管慢病进展
(1)猝死原理:心肌“结构”异常→“电短路”→“动力”停止
心搏骤停常发生于存在某些基础器质性心脏病的患者,最主要是冠状动脉性心脏病(冠心病),70%的心搏骤停可归因于冠心病。在冠心病患者中,心搏骤停既可见于急性冠脉综合征(ACS)期间,也可见于慢性稳定性冠心病患者。慢性冠心病患者通常存在既往的心肌损伤和可能诱发心搏骤停的心肌瘢痕。
那么心肌损伤又如何影响到电传导,从而导致心脏骤停呢?可导致心脏性猝死的心律失常类型中,25%-35%由室颤和无脉室速引起,25%由PEA引起。而室颤与室速的发生与心肌的缺血或心肌梗死后瘢痕导致的电传导异常有很大的关系:
室颤(VF)的机制——心肌异质性:旋转的螺旋波是其最可能的机制,几乎总是发生于通常呈弥漫性的基础心肌病变(图3),从而导致除极的异质性及复极的离散趋势。这种电生理特性的不一致性是折返的前提。多个局部心电微折返区导致室颤,室颤时无任何有序的电活动。传导和复极参数的差异(心肌异质性)导致冲动在经心肌传导的过程中碎裂,从而形成多个局部折返区或多个心肌激活螺旋小波。因为不存在有序的电活动和心肌除极,所以没有均一的心室收缩,从而使心脏无法产生心输出量。
室速(VT)的机制:在大约80%的VT/VF患者中,持续性室性心律失常之前会出现心室异位起搏增加以及反复性室性心律失常,特别是发生多次非持续性VT,这些自发性心律失常在发生VT/VF前的持续时间不一。持续性多形性VT可进展成VF,这最常是由基础缺血所致。VF也可以是心脏性猝死的原发性事件。
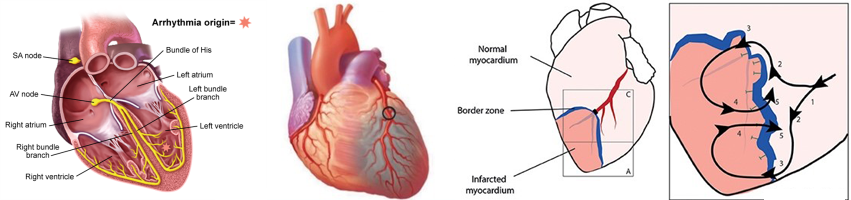
(2)庞大的潜在患者群体——慢病进程中的冠心病、心衰患者群体
猝死的病因
心脏性猝死病因与年龄、人群有关: 40岁以下心脏性猝死患者(既往均无基础心脏病)73%为心源性,15%为非心脏性的(最常为颅内出血)。35岁以下更可能是非冠心病原因。两性猝死发生率均随年龄增长而增加,但男性比女性更易发生猝死——男性是女性的2-3倍。
是否有基础心脏病,发生心搏骤停风险也有显著不同:存在心脏病时心搏骤停风险增至6-10倍,存在冠心病危险因素时心搏骤停风险增至2-4倍。其中,猝死的几类主要病因包括:
①冠状动脉性心脏病 :最常见病因,70%的心搏骤停可归因于冠心病(大于30岁患者中为58%,30岁以下患者中为22%)。在冠心病患者中,心搏骤停既可见于急性冠脉综合征(ACS)期间,也可见于慢性稳定性冠心病患者(通常存在既往心肌损伤和可能诱发心搏骤停的瘢痕)。实际上心脏性猝死更常见于没有可识别急性心脏事件的患者,超过50%的心搏骤停为先前未知或未识别心脏疾病的首发表现。
②其他器质性心脏病 :占院外心搏骤停病例的10%。①心力衰竭(心衰)和心肌病,约1/3的死亡由心脏性猝死导致。②由高血压或其他原因导致的左心室肥厚(高血压导致的心肌肥厚通常伴有心肌纤维化,可能为室性心律失常创造条件);③心肌炎;④肥厚型心肌病(30岁以下患者中为13%);⑤致心律失常性右室心肌病;⑥先天性冠状动脉异常;⑦二尖瓣脱垂。
③无器质性心脏病 :45岁以下的心搏骤停病例中占10%-12%。①Brugada综合征;②特发性VF;③长QT综合征;④家族性多形性VT;⑤原因不明的家族性心脏性猝死;⑥WPW综合征;⑦心震荡。
其中,两大患者群体需要引起注意:
①冠心病
65%-70%的心脏性猝死可归因于冠心病,并且30%-50%的冠状动脉性死亡由心脏性猝死引起。冠脉造影显示71%的心搏骤停幸存者患者存在有意义冠脉狭窄(其中48%存在冠状动脉闭塞),其余患者亦不能排除急性冠脉综合征或心肌缺血。在30-40岁以下的心脏性猝死病例中约24%病因为冠心病。心脏性猝死的发生率与冠心病的临床表现有关:在有既往心肌梗死的患者中最高,在无既往心肌梗死的心绞痛患者中居中。但心脏性猝死可发生于存在无症状性缺血的患者中,并可为冠心病的初始表现。
急性心梗:在表现为急性心肌梗死而非心脏性猝死的患者中,VF的发生率因梗死的类型和时间而异:急性ST段抬高型心肌梗死的VT/VF的总体发生率为10.2%,80%-85%的此类心律失常发生在最初48小时。非ST段抬高型急性冠脉综合征的VT/VF的总体发生率为2.1%。发生心律失常的中位时间为78h(四分位间距为16h和7d)。
多个研究显示急性心肌梗死后最初48小时内VF的发病高峰,据推测可能由缺血所致,而之后发生的VF可能与梗死愈合形成瘢痕(和单形性VT的风险增加)有关,且可增加晚发性心脏性猝死的风险。晚发性心脏性猝死最常发生在第1年,大多数发生在最初几个月内,由室性快速性心律失常引起。ST段抬高型和非ST段抬高型梗死患者发生晚发性VT/VF的风险似乎相同。这些数据不包括入院之前已经死亡的心脏性猝死患者。据估计,超过50%的急性心肌梗死所致死亡发生于院外,多数发生于症状出现1小时内。
心肌缺血:存在不稳定的冠脉病变,这些病变可能导致急性缺血事件(没有梗死),并可导致电活动不稳定。76%的心搏骤停患者有明显冠脉病变、痉挛或不稳定病灶,近1/2的患者有冠脉闭塞。不在心肌梗死急性期的患者即使成功进行了血运重建,仍可能持续存在较高的VT/VF复发风险。
②心衰
心衰是心脏性猝死相对常见的一个病因。30%-50%的心衰患者死亡由心脏性猝死所致,并且在心衰症状加重期间心脏性猝死的发生率有增加。心衰患者的心脏性猝死发生率是无心衰患者的5倍,其中女性患者的绝对危险度是男性患者的1/3。
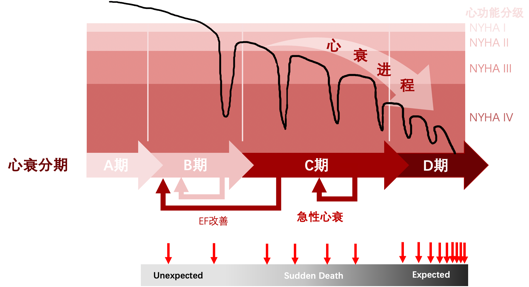
心衰患者的死亡原因中,进行性泵衰竭、意外心脏性猝死(通常由室性快速性心律失常引起,有时也可由心搏停止和无脉性电活动导致)和心衰临床恶化发作期间发生的心脏性猝死分别约占心衰死亡总数的1/3。39%心衰患者的猝死被认为是由心律失常引起,VT发展为VF是心脏性猝死最常见的病因,5%-33%的病例是由缓慢性心律失常或PEA引起。急性冠脉事件可能是一些心衰患者发生猝死的诱因。心衰患者有显著冠状动脉疾病的患者中,54%的猝死患者和32%死于心衰的患者有急性冠脉病变。
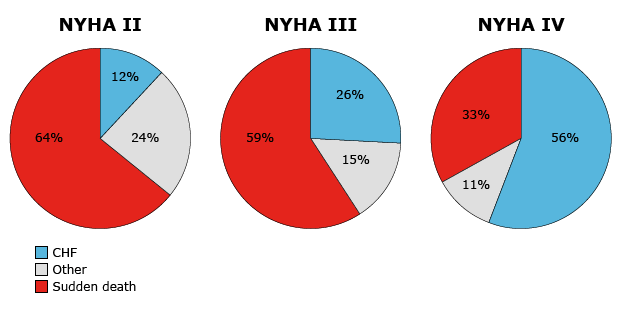
心衰越严重总体死亡率和心脏性猝死绝对发生率越高(图4)。心衰患者的死亡率和方式因心衰等级和心肌病类型不同而异, NYHA Ⅱ级或Ⅲ级心衰患者的死亡方式更可能是“突然”的猝死,而NYHA Ⅳ级心衰患者的死亡方式更可能与“泵”衰竭有关(图5),其中VT和VF仍是最常导致心脏性猝死的心律失常。MERIT-HF研究显示,患者心衰的等级越高(NYHAⅡ、Ⅲ和Ⅳ级)在1年时发生心脏性猝死的几率就越高(分别为6.3%、10.5%和18.6%),但是归因于心脏性猝死在总死亡病例所占的比例却有下降(分别是64%、59%和33%)。
“扳机”——急性触发因素
除基础器质性心脏病外, 一些短暂或可逆的病因可能诱发心律失常和心脏性猝死,识别这些病因对于治疗基础疾病和判断心脏性猝死复发概率至关重要。可能可逆的心脏性猝死触发因素包括:①急性心脏缺血和心肌梗死:冠心病是心脏性猝死最常见的病因,因此所有心脏性猝死幸存者都应考虑急性冠脉缺血;②心衰:在心衰症状恶化期间,心脏性猝死的发生率可能会增加;③自主神经系统兴奋,特别是交感神经,如突然的情绪激动;④其他:抗心律失常药、毒素、电解质异常、酸中毒、严重低氧血症。
2. “救”永远来不及,“防”才能跑在死神前面
基于上述,各种心脏疾病均有发生心脏性猝死的可能,甚至很多冠心病患者以猝死为首发表现,针对庞大的心血管病猝死高风险患者的预防格外重要。目前根据心血管病防治指南,我国已有针对心脏性猝死的一、二级预防标准和措施。
一级预防是通过临床诊断,发现存在高危因素的患者并尽早植入心律转复除颤器(ICD)。二级预防是对已发生过心脏猝死的患者实施预防,通过植入ICD防治心脏性猝死。但是二级预防手段只针对已经发生过心脏性猝死的患者,难以覆盖整个心脏性猝死高危人群。目前在欧美普遍接受并应用的是一级预防,即针对未发生过心脏性猝死的高危人群的预防。
(1)适应症维度:分层策略与逻辑
虽然ICD对室性快速性心律失常的治疗和心脏性猝死预防非常有效,但其费用昂贵、需要持续随访、植入时以及装置使用寿命期间存在很多风险(如,出血、气胸、穿孔,以及感染、装置和导线故障等),而且仅部分心肌病患者发生持续性室性快速性心律失常或心脏性猝死。因此,应在ICD治疗之前对患者进行风险分层,对心脏性猝死风险最高患者提供治疗,并最大程度减少不太可能受益患者的ICD植入数量。进行心脏性猝死风险分层以便植入ICD一级预防的主要指标主要包括:①左心室功能障碍的病因;②左心室射血分数(LVEF);③心衰症状分级;④期望寿命超过1年;⑤可诱导性持续性室性心动过速;⑥心电图监测显示有非持续性室性心动过速。
其中主要指标涉及两大方面:①LVEF明显降低的患者风险似乎最大,可从植入ICD一级预防得到的获益也最大;②急性心肌梗死后心脏性猝死风险因素包括:左室功能障碍或LVEF降低;心衰症状和心衰的程度;左室室壁瘤;体表心电图上的Q波;室内传导延迟等。
推荐植入ICD以进行心脏性猝死的一级预防的患者如下(图6):
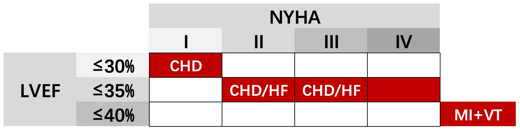
①存在缺血性心脏病所致心肌病、LVEF≤35%和NYHA Ⅱ级或Ⅲ级状态心衰的患者,在心肌梗死后至少40日并且在血运重建及使用指南指导的药物治疗后3个月以上接受ICD评估。
②存在缺血性心脏病所致心肌病、LVEF≤30%和NYHAⅠ级状态的患者,在心肌梗死后至少40日并且在血运重建及使用指南指导的药物治疗后3个月以上接受ICD评估。
③存在既往心肌梗死相关NSVT、LVEF≤40%,以及电生理检查(EPS)时可诱导持续性VT或VF的患者。患者应处于心肌梗死的急性期之后,在使用指南指导的药物治疗,而且预计生存期至少有1年。心肌梗死导致LVEF降低的患者,发生心脏性猝死的风险增加,最常是因为室性快速性心律失常。对于特定的缺血性心肌病患者,预防性植入ICD进行心脏性猝死一级预防可降低死亡率。
④对于非缺血性扩张型心肌病、LVEF≤35%和NYHA Ⅱ级或Ⅲ级心衰的患者,ICD能非常有效地降低总死亡率和心脏性猝死所致死亡率。所有接受ICD作为心脏性猝死一级预防的患者都应在ICD植入前进行至少3个月基于指南的药物治疗。
⑤对于LVEF≤35%、NYHA Ⅲ或Ⅳ级心衰和QRS间期≥120毫秒的患者,推荐植入CRT-D联合装置(双心室起搏联合ICD),而非单纯植入ICD。对于左束支阻滞(LBBB)QRS形态的患者、QRS间期≥150毫秒的患者以及因房室传导阻滞而依赖心室起搏的患者,最应该考虑行CRT。
(2)一级预防:防尚未猝死人群
①一般人群:风险分层与减少危险因素
筛查及风险分层:对于已知心搏骤停风险升高的人群(如既往心梗),通过检查做进一步风险分层识别能获益于ICD的患者。对于无已知心血管疾病的一般人群,指南建议筛查心血管疾病的危险因素,视情况在部分患者中筛查冠心病。
生活方式干预:许多与冠心病发生有关的传统危险因素也与心搏骤停有关,所以针对性干预这些危险因素也可降低心搏骤停的发生率。干预措施包括:有效治疗高胆固醇血症、高血压;采用心脏健康饮食;规律锻炼;戒烟;适量饮酒;有效治疗糖尿病。虽然,尚无确切证据显示在一般人群中减少危险因素可降低心搏骤停发生率,但由于大多数冠心病死亡由心脏性猝死导致,研究证实减少危险因素的干预措施可以降低心血管和冠状动脉相关的总死亡率,从而降低心搏骤停的发生率。
②缺血性心脏病(冠心病)患者
存在缺血性心脏病的患者发生心搏骤停的风险增加,特别是有心肌梗死病史的患者。心肌梗死后的心搏骤停风险会因一些因素而显著增加。预防这类患者发生心搏骤停的方法:①标准药物治疗。β受体阻滞剂和血管紧张素转化酶抑制剂可降低心肌梗死后总体死亡率,可常规使用。这些药物也可以降低心脏性猝死发生率。②应进行风险分层以识别心搏骤停风险最高的患者。③对经选择的患者植入ICD。
关于缺血性心肌病中植入ICD一级预防的研究显示ICD可显著提高生存率:MADIT-Ⅰ试验(Multicenter Automatic Defibrillator Implantation Trial)是证实ICD在某些高风险、无症状患者中对心脏性猝死一级预防有作用的首个临床研究。这些患者存在既往心肌梗死伴LVEF降低(≤35%)、心电图监测显示NSVT,以及EPS期间出现可诱导性持续性单形性VT(在静脉给予普鲁卡因胺后也可诱导)。与药物治疗组患者相比,ICD治疗组患者总体死亡率、心脏性死亡率和心律失常性死亡显著减少(图 7左图)。MADIT-Ⅱ试验:入组前30日天以上发生既往心肌梗死且LVEF降低(≤30%)的患者。ICD组患者较药物治疗组的全因死亡率降低(ICD组14.2% vs 常规治疗组19.8%,HR 0.65,95%CI 0.51-0.93)(图 7右图)。
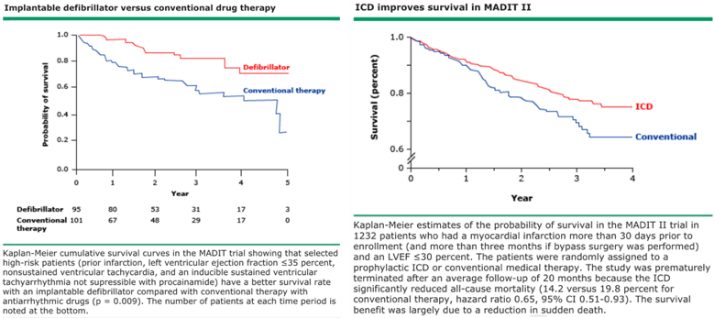
③心衰和心肌病患者
心脏性猝死风险随着左室收缩功能障碍和临床心衰严重程度的增加而升高,且不论何种病因,有心衰和左室收缩功能障碍的患者心搏骤停风险都有增高。对于心衰和心肌病患者,ICD在心脏性猝死一级预防中的作用取决于几个因素:左室收缩功能障碍的严重程度;临床心衰的严重程度;左室功能障碍的病因(缺血性vs非缺血性心肌病);影响寿命和ICD并发症风险的竞争性共存疾病(慢性肾脏病、慢性阻塞性肺疾病等)。同时,其他原因(进行性心衰)导致死亡的风险也会随心衰和左室收缩功能恶化而增加,所以植入ICD一级预防前恰当选择患者格外重要。
④与心搏骤停风险增加相关的先天性疾病(如Brugada综合征、先天性长QT综合征和WPW)。
(3)1.5级预防:中国国情下的目标人群充分必要干预
由于我国符合一级预防适应证的患者显著多于二级预防者,但利用防治器械进行心脏性猝死预防的患者较少——目前我国ICD的植入率仅1.4个/百万人,且现有医疗资源难以满足庞大的人口基数下心脏性猝死患者的一级预防需求。医保政策、循证医学数据缺失、患者对于植入式ICD不了解甚至恐惧心理,是不少患者拒绝接受ICD植入等都是一级预防难以落实的原因。
为了进一步提高患者、医生等对ICD疗法预防心脏性猝死的认知,更有针对性的加强对极高危患者猝死的预防,中华医学会心电生理和起搏分会提出针对中国患者的1.5级预防,在国际上一级预防的适应症基础上进一步增加四大高危因素之一——LVEF <30%、频发室早、非持续性室速、晕厥及晕厥前兆。1.5 级预防概念的提出对推动心脏性猝死的预防和治疗具有实际意义,1.5级预防涉及的人群是充分必要进行ICD植入的人群,相对一级预防的范围缩小、更有针对性和必要性,间接减少了医保及患者负担。
3. 预防时间窗
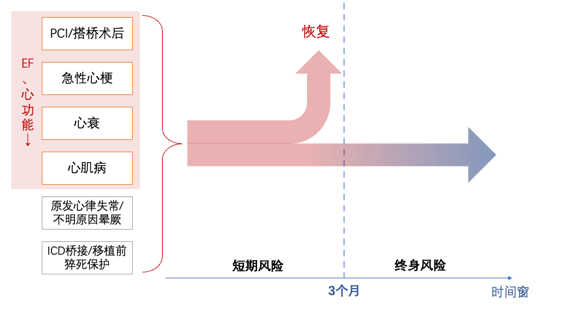
目前,猝死一级预防(如上文)的时间窗在患者血运重建3个月以后才评估考虑植入ICD,而3个月内患者依然是高风险期,根据美国的大型全国心血管数据注册研究(NCDR)和胸外科医师协会(STS)成人心脏外科数据库研究显示,左心室功能不全患者(如LVEF≤30%)在PCI或CABG术后早期的死亡率显著更高。左室明显功能不全者在CABG术后30日的死亡率显著高于左室功能正常者,这些患者不仅因室性心律失常发生心脏性猝死的风险增加,其因非心律失常事件死亡的风险也会增加。
同时,在实际临床中国内外都碰到了短中期的ICD植入预防猝死的挑战:美国报销不覆盖CABG或PCI术后3个月内植入ICD用于一级预防的费用。而在国内,由于ICD的植入性和费用问题,临床医生常常要花很长的时间说服患者,这个时间的跨度很可能长于高风险患者的时间窗。如何在3个月内以患者易于接受的方式(无创伤性与价格适中)来预防猝死是其中的关键。
对于心脏性猝死高危患者的临时治疗,可以用WCD作为替代措施来预防心脏性猝死。可穿戴式心脏转复除颤器(wearable cardioverter-defibrillator, WCD)是一种体外背心式除颤装置,能够自动检测室性心动过速(VT)、室颤(VF)并无创性除颤。2016年美国心脏协会(American Heart Association, AHA)科学建议、美国心律协会(Heart Rhythm Society, HRS)和2017年AHA/美国心脏病学会(American College of Cardiology, ACC)/HRS指南的推荐中,以下患者临时使用WCD可能获益:
①心肌梗死后40日内LVEF≤35%:NYHAⅡ-Ⅲ级或LVEF<30%、NYHAⅠ级的积极患者使用WCD,因为此类患者在40日后可能需要植入ICD。心肌梗死后1-3个月应重新评估LVEF,如果给予适宜药物治疗后再次评估LVEF仍≤35%,则患者需要植入ICD,应考虑植入。
②LVEF≤35%、过去3个月内行冠状动脉搭桥手术(CABG)血运重建:WCD作为心脏性猝死的一级预防。同时,应在CABG后3个月重新评估LVEF,如果发生了持续性室性快速性心律失常,或者LVEF仍≤35%,则通常需要植入ICD。
③新诊断的非缺血性心肌病:对于部分重度但有可能逆转的心肌病患者,如心动过速性或心肌炎相关心肌病患者,WCD可能有助于在等待左室功能改善、ICD植入或必要时的心脏移植期间预防室性心律失常引起的心脏性猝死。
④过渡到心脏移植:等待心脏移植的重度心力衰竭患者心脏性猝死风险特别高,一般推荐植入ICD。WCD可能是合理的无创性替代方法,特别是对于尚未植入ICD且预计等待时间较短的患者。
⑤桥接到有指征的或中断的ICD治疗:部分具有ICD植入指征的患者可能因共存疾病(如感染、术后恢复、缺乏血管通路)而需要推迟植入ICD。此外,部分装有ICD的患者因感染而需取出装置,对于这些患者,WCD可以对抗室性快速性心律失常,直到患者可以植入或再次植入ICD为止。
四、 展望
1. 公卫与临床的更密切的合作,从一线急救到前端预防的全体系联动
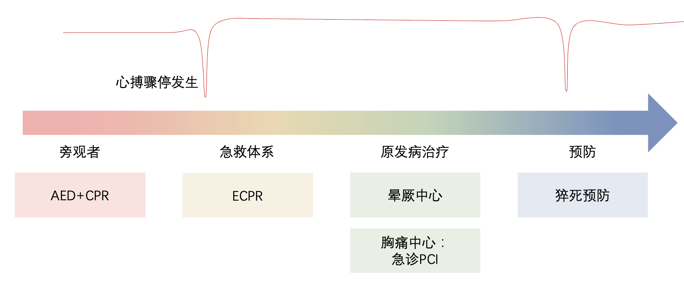
(1)一线急救——旁观者CPR与AED
我国人口密度大,相对猝死人员基数大。最能有效解决一线急救问题的方式就是“公众除颤”方式——在公共交通设施、购物中心、公共体育场馆等场所配备AED,急救人员到达之前可由目击者使用AED除颤,扩大了能够提供早期除颤的潜在施救者群体,最大限度解决我国人口基数下的潜在猝死患者的急救问题。同时,由于历史上受舆论关注广为流传的对于见义勇为等不利判例,我国公众有特殊的民事责任顾虑,解除“旁观者”的负担还需要做出更正面的舆论宣传。
心脏骤停下,仅除颤还不足以恢复患者的自主循环,有效而高质量的CPR是复苏的关键,相对应的急救培训也亟待加强。急救培训如何落实,尚需要卫生行政部门指导、教育部门培训、公益组织配合的多部门协作、多环节衔接才能补齐目前公共服务短板,将公共卫生资源最大化利用,最终使我国的猝死救治生存率有效提高。
(2)高级生命支持——ECPR
当心脏骤停超过30 分钟不能持续维持自主循环时,为尽可能缩短心脏骤停后低血流时间、减少复苏后重要器官灌注不足引起的并发症,患者需要体外心肺复苏(ECPR)给予充分循环灌注有效保障重要器官(脑、肾、肝等)尤其是关键的神经功能。但是,ECPR成功依赖强有力的ECMO团队及后续的ICU治疗,我国目前的急救体系与重症临床联动尚需进一步加强:一方面通过完善急救网络联动与ECPR响应区域覆盖,另外加强专业团队的ECPR技术与ECMO培训,如果条件允许,可进一步通过移动ECMO推进现场ECPR以最大限度降低可及半径。
(3)解决原发病——胸痛中心、晕厥中心建设
由于近70%的心脏性猝死由冠心病引起,且猝死是很多冠心病的首发表现,因此在猝死急救同时兼顾复苏与原发病治疗双时间窗的治疗格外重要。目前我国为了提高急性胸痛患者的早期诊断和治疗,建立了全国胸痛中心体系,2015年成立至今全国已达上千家。 胸痛中心有急诊绿色通道,可完成快速准确的诊断、危险评估和治疗,导管室可365天/24小时开放,随时可进行急诊PCI治疗,有效降低胸痛患者死亡率。
另外,在心脏骤停幸存者的症状中,晕厥可能作为一种预警信号出现。晕厥是脑供血不足导致的意识障碍,病因主要包括心源性晕厥、神经介导的反射性晕厥、直立性晕厥。由于晕厥的诊断涉及心血管与神经等多学科领域,准确诊断的难度较大,缺乏规范化管理下诊断率低误诊率高。 为此专家建议在三甲医院成立晕厥中心开设晕厥门诊,对短暂意识丧失患者进行集中、规范管理。2019年我国首批72家医院挂牌启动了晕厥中心建设,由经过培训的医生和护士专职负责,统一诊断标准与处理流程、负责患者管理和随访,强调对晕厥患者危险分层,积极治疗心脏疾病、预防恶性心律失常的发生。
(4)猝死预防——高风险分层与ICD
一级预防依赖相关亚专科心血管医生对患者做风险分层。二级预防依靠门诊或晕厥门诊详细评估后,尽快进行干预。
一级预防强调无已知心脏疾病的一般人群进行冠心病危险因素筛查和管理,并注重生活方式调整与干预。对于心搏骤停风险增高的心脏病患者,如既往心肌梗死、心肌病或心力衰竭患者,主要预防措施为标准药物治疗,确定心搏骤停风险分层后对经选择的患者植入ICD,短期风险患者可考虑非植入型的WCD。
当心脏停搏发生时已经进入猝死的二级预防范畴,重点对心搏骤停幸存者进行综合评估和二级预防。经过心肺复苏后,心搏骤停幸存者的需要识别并治疗急性可逆性病因、评估有无器质性心脏病和/或原发性心电疾病、评估神经系统及对特定病例评估家庭成员。心脏性猝死的二级预防通常采用ICD,适合大多数心搏骤停幸存者。
2. 针对临床需求的技术趋势
(1)AED可及性
可移动AED缩短半径:除提高AED部署密度外,进一步提高黄金4分钟之内的AED覆盖效率可通过移动AED实现,后者抢救覆盖效率是固定AED的6倍,可显著扩大AED的潜在救治范围。
APP监测心搏骤停患者并通知附近的志愿者就近急救:可考虑开发手机APP应用,感知发生心搏骤停的患者并自动通知120急救系统,由急救中心分派心搏骤停患者附近距离事件发生地点4分钟内可移动距离的志愿者,根据APP相关地图定位前往患者位置施救。对于某些公共区域和家中停搏患者,这种方式也许可增加早期CPR和生存率。
家中配置AED:由于约3/4的心搏骤停发生于家中,配置AED供家中使用可能降低死亡率。
(2)ECPR可及性
与AED不同,ECMO不适合常规公共区域配置,所以不可能通过大规模区域投放增加配置密度。目前ECPR尚依赖区域内中心医院给予技术支持,如果想提高ECPR可及性,其中一个重要方向是ECMO设备的可移动性与小型化。便携性ECMO,相对常规ICU内的ECMO小巧轻便,一个人就可轻松手持到直升机或救护车上。考虑到长途转运的特殊情况,产品需要同时兼顾转运中的高稳定性、防碰撞保护和长时间电池续航的特性。
(3)除颤微创与无创化:WCD与SICD
目前ICD是预防心脏性猝死的首选治疗方式。传统ICD植入通过外周静脉送入电极至右心室,与脉冲发生器链结构埋藏于左胸部皮下。虽然ICD普遍使用,但其并发症一直困扰临床,尤其是静脉导线相关并发症。由于除颤电极导线故障频现,加之经静脉途径植入其相关并发症较多,近年来S-ICD开始应用于临床,其导线和脉冲发生器均位于皮下,除颤导线不直接接触心脏及静脉,很好地解决了长期猝死预防需求。
尽管如此,临床上仍有部分SCD发生高风险的患者不符合现有指南的植入适应证,且很大部分患者都属于心肌缺血及相关血运重建手术出院后的短期高风险状态,短期猝死预防的的需求更强烈,需要无创性除颤。WCD因无创且穿戴简单方便,很好地解决了上述患者SCD的预防难题。
作者简介:陈阳博士于北极光创投负责创新医疗器械投资,拥有十余年临床工作与医疗早期投资经验,拥有北京协和医学院医学硕士和博士学位、上海交通大学医学院临床医学学士学位。

